Развитие химии тритерпеноидов - широко распространенных в природе вторичных метаболитов высших растений привело в последнее десятилетие к открытию ряда перспективных противовирусных, противоопухолевых, антимикробных и антигликемических агентов среди производных олеаноловой, урсоловой, глицирретовой, мороновой и бетулиновой кислот. Глицирретовая кислота (ГЛК) (1) – основной пентациклический тритерпеноид корней солодки голой (Glycyrrhiza glabra L.) и уральской (Gl. uralensis Fisher) обладает различными видами биологической и фармакологической активности (противовоспалительной, противоязвенной, антиоксидантной, гепатопротекторной, антиаллергической, противораковой, противовирусной и др.) [1]. Синтез новых производных ГЛК и родственных тритерпеноидов представляет интерес для изучения зависимости структура-активность.
Нами осуществлен синтез 2-замещенных производных (циано-, хлор-, бром-) на основе 3-кето-производных тритерпеноидов (1-3). Проведены новые скелетные и окислительные превращения 11-дезоксо-ГЛК (2) и олеан-9,12-диен-30-овой кислоты (3) по кольцу А с получением 1,2-енов, 2,3-секо-производных и 1-гидрокси-2-енов (диосфенолов). Предложен метод стереоселективного гидроксилирования 3-кетонов тритерпеноидов мета-хлорпербензойной кислотой в 2α-гидрокси-3-кетоны. Впервые проведен исчерпывающий озонолиз олеан-9(11),12(13)-диен-30-овой кислоты (3) с получением смеси продуктов окисления, содержащей эпокси-, окси - и кето-производные.
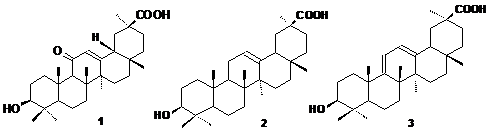
Работа поддержана РФФИ (грант 2011-03-00462а) и Роснаукой (ГК 14.740.11.0367).
Список литературы:
1 , , Толстикова : биоразнообразие, химия, применение в медицине. Новосибирск: Академическое изд-во «Гео», 2007. 311 с.
УДК 547.995.15’491.6.057
1, 1, 2, 3, 1
МОДИФИКАЦИЯ ГИАЛУРОНОВОЙ КИСЛОТЫ С ЦЕЛЬЮ СОЗДАНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ ДЛЯ ОФТАЛЬМОЛОГИИ
1Российская академия наук Уфимский научный центр Федеральное государственное бюджетное учреждение науки Институт Органической химии
E-mail:*****@***ru
2ГУ Уфимский НИИ глазных болезней АН РБ
3 Башкирский государственный университет
Во многих случаях при проведении операций на глазах или сердечнососудистой системе возникает необходимость локального закрепления на определенное время лекарственного средства по месту раневой поверхности. Эффективность многих лекарственных препаратов значительно возрастает при использовании специальных лекарственных форм, обеспечивающих пролонгирование действия лекарственного препарата, его адресную доставку к системам и органам, а в некоторых случаях и заметный синергетический эффект действия препарата и фармакопейной основы. Особый интерес в этом смысле представляют биополимеры гликозаминогликанового ряда, в том числе - гиалуроновая кислота (ГК), обладающая сама по себе спектром биологической активности и проявляющая высокую биосовместимость. Одним их аспектов использования ГК является создание на ее основе лекарственной формы совместно с цитостатиками, такими как митомицин или фторурацил.
Однако в организме, под действием ферментов и свободных радикалов, нативная ГК подвергается быстрой деградации, что ограничивает ее использование в случаях, требующих длительного лечебного эффекта. Поэтому возникает необходимость разработки различных способов изменения физико-химических свойств ГК при сохранении ее биосовместимости.
Целью данной работы являлась разработка способов модификации ГК и создания композиции на основе модифицированной ГК и митомицина С (ММС), для использования в качестве лекарственного средства при проведении операций глаукомы.
ГК модифицировали эпихлоргидрином в аммиачно-щелочном растворе при различных исходных соотношениях реагентов. Реакцию останавливали диализом, продукт осаждали метанолом и сушили под вакуумом. Полученные образцы исследовали методами УФ-, ИК - и ЯМР-спектроскопии.
Далее исследовалось взаимодействие между модифицированной ГК и ММС в физиологическом растворе. В раствор модифицированной ГК вводили ММС в антибатных соотношениях и выдерживали при повышенной температуре в течение 2ч. Полученные растворы исследовали методом УФ-спектроскопии (рис. 1).
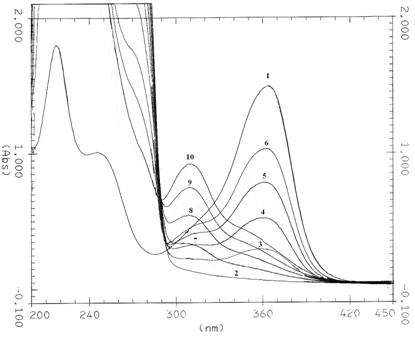
Рисунок 1 - УФ-спектры в физиологическом растворе: ММС (1); МГК (2); смеси ММС:МГК состава 1:4 (3, 7); 2:3 (4, 8); 3:2 (5, 9); 4:1 (6, 10) после выдержки в течение 2 ч. при температуре 250С (1 - 6), 450С (7 -10). [ММС] = [МГК] = 2·10-3 моль/л.
Видно, что после прогрева смеси МГК и ММС в растворе имеет место появление нового пика в области 310 нм и уменьшение интенсивности пика в области 363 нм, что свидетельствует о взаимодействии компонентов. При комнатной температуре подобного взаимодействия не происходит. Полученные композиции исследуются в институте глазных болезней на эффективность использования в качестве лекарственного средства при операциях глаукомы.
Работа выполнена при финансовой поддержке ФЦП «Научные и научно-педагогические кадры инновационной России» на 2009 – 2013 годы (мероприятие 1.1), номер заявки 2012-1.1-12-000-1015-027
УДК 664.162.036.29
,
ГИДРОЛИЗ ХЛОПКОВОЙ ВАТЫ РАСТВОРАМИ ФОСФОРНОЙ КИСЛОТЫ
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail:bio2@rusoil.net
Отходы биомассы растительного сырья сельскохозяйственной и деревообрабатывающей промышленности необходимо рационально утилизировать. Одним из перспективных способов является гидролиз целлюлозосодержащих материалов химическим способом и использование растворов гидролизатов в биотехнологическом производстве.
Исследование возможности гидролиза целлюлозы растворами фосфорной кислоты являлось целью нашей работы.
Апробирован гидролиз хлопковой ваты водными растворами 20, 60 и 70% фосфорной кислоты.
Глубину гидролиза определяли по содержанию редуцирующих веществ в пробе методом Макэна и Шоорля (МШ) и титрометрическим методом с гексацианоферратом калия (ТМ) (табл.).
Таблица – Выход редуцирующих веществ (РВ) при гидролизе хлопковой ваты водными растворами 20, 60 и 70% H3РO4 при температуре кипения реакционной смеси
Время гидролиза, ч | Концентрация H3РO4 , % | Выход РВ, % | |
Метод МШ | Метод ТМ | ||
1 | 2 | 3 | 4 |
4 | 20 | 3,7 | 2,0 |
4 | 60 | 27,6 | 31,9 |
3 | 70 | 48,4 | 50,1 |
Полученные результаты показывают, что с увеличением концентрации фосфорной кислоты выход редуцирующих веществ в реакционной смеси возрастает, однако уже при концентрации кислоты 70% наблюдается повышенное смолообразование.
УДК 677.11.116
ХИМИЧЕСКИЙ СОСТАВ СОЛОМЫ ЛЬНА-МЕЖЕУМКА – ПЕРСПЕКТИВНОГО СЫРЬЯ ДЛЯ ПОЛУЧЕНИЯ ЦЕЛЛЮЛОЗЫ
Федеральное государственное бюджетное учреждение науки
Институт проблем химико-энергетических технологий
Сибирского отделения Российской академии наук, г. Бийск
E-mail: julja. *****@***ru
В настоящее время наметилась тенденция к использованию недревесного целлюлозосодержащего сырья [1]. В России для промышленного освоения производства целлюлозы из недревесных источников наибольший интерес представляет лен-межеумок. Вопрос производства выращивания однолетних целлюлозосодержащих растений принят «Большой семеркой» наиболее развитых стран как одна из приоритетных задач XXI в.
Лен может произрастать в различных климатических зонах страны. Гарантированная урожайность льна, многовариантность его переработки могут существенно поднять доходность и занятость населения аграрно-промышленных регионов России. Уже сейчас лен в растениеводстве страны, в частности в Нечерноземье, Сибири и Алтайском крае, занимает особое место — он дает до 70 % дохода и служит основой формирования в аграрно-промышленном секторе большого числа рабочих мест.
Целлюлоза изо льна обладает очень высоким качеством и может использоваться в производстве сигаретной бумаги, гигиенических изделий и даже банкнот. Выход биомассы льна очень высок. Он превышает данный коэффициент у древесины на 2,0-2,5 единицы [3, 4].
В данной работе рассматривается перспектива получения целлюлозы из соломы льна-межеумка.
В качестве первого объекта исследования использовали солому льна-межеумка урожая августа 2011 года, собранную в Алтайском крае в мае 2012 года, в качестве второго – солома льна-межеумка урожая 2012 года (время сбора – сентябрь). Следует отметить, что в литературных источниках отсутствует информация о химическом составе соломы льна-межеумка, раздельно имеются данные о составе волокна и костры [4, 5].
Солома льна-межеумка без разделения на волокно и костру была измельчена, усреднена и направлена на определение химического состава по общепринятым методикам [6].
В соломе льна-межеумка урожая 2012 года имелись толстые стебли, отличающиеся по внешнему виду от общей массы, было принято решение дополнительно определить и их химический состав.
Химические составы образцов соломы льна-межеумка (2011-2012 гг.) и стеблей (2012 г.) приведены в таблице 1.
Таблица 1 – Химические составы образцов соломы льна-межеумка (урожаев 2011г. и 2012 г.) и стеблей в соломе льна-межеумка урожая 2012 года
Наименование сырья | Влаж ность, % | Золь ность*, % | Лигнин*, % | Целлюлоза по Кюршне ру*, % | Пентозаны*, % | Жировосковая фракция*, % | |
Солома | 2011 г. | 11,1 | 2,82 | 20,69 | 50,05 | 18,87 | 9,33 |
2012 г. | 10,8 | 2,37 | 16,85 | 53,29 | 22,27 | 10,40 | |
Стебли в соломе (2012 г.) | 10,3 | 1,82 | 23,10 | 46,90 | – | 6,48 | |
Примечание: * – в пересчете на а. с.с. |
Полученные результаты, а именно: содержание целлюлозы по Кюршнеру в пределах 46,90 % - 53,29 %; зольность на уровне 1,82 % - 2,82 %; кислотонерастворимый лигнин 16,85 % - 23,10 % свидетельствуют о возможности получения целлюлозы из соломы льна-межеумка [7].

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 |





