Из таблицы 1 видно, что наиболее качественный образец силоса получили при внесении смешанной закваски бактерий L. plantarum и «Иммуннеле», взятых в соотношении 1:1 (по объему).
Список литературы:
1 Электронный ресурс: Карпов, силосования/ . Режим доступа: http://www. fermer/zhivoth
547.269.352’853.7
, ,
ФУНКЦИОНАЛИЗАЦИЯ СУЛЬФОНИЛИМИНОВ ПОЛИХЛОРАЦЕТАЛЬДЕГИДОВ 2-АМИНОПИРИМИДИНОМ
Федеральное государственное бюджетное учреждение науки
Иркутский институт химии им. СО РАН, г. Иркутск,
E-mail: *****@***irk. ru
Для разработки эффективных подходов к получению функционализированных производных сульфонамидов, содержащих в структуре фармакофорные сульфонамидные и аминопиримидиновые фрагменты, мы изучили взаимодействие арилсульфонилиминов фенилдихлорацетальдегида и хлораля 1, 2 с аминопиримидином. Активированные имины 1, 2 могут быть легко получены реакцией
N, N-дихлораренсульфонамидов с фенилацетиленом или трихлорэтиленом по ранее разработанным методам [1,2].
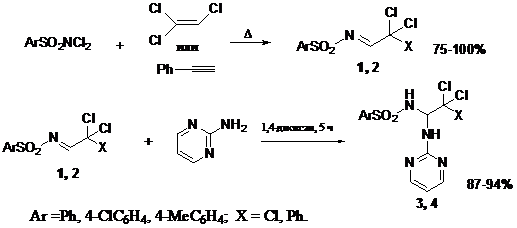
Установлено, что реакция протекает хемоселективно с образованием
N-[1-(пиримидин-2-ил)амино-2-полихлорэтил]аренсульфонамидов 3, 4 – продуктов нуклеофильного присоединения гетероциклического амина к активированным азометиновым группам.
Из-за наличия в структуре сульфонамидной группы, эндоциклических аминогрупп и полихлорметиленового фрагмента соединения 3, 4 представляют интерес в качестве объектов для физико-химических исследований, изучения биологической активности и перспективны для последующей гетероциклизации в имидазопиримидиновые производные.
Работа выполнена при поддержке РФФИ № 12-03-31762 мол_а.
Список литературы:
1 , , ЖОХ, 2008, 78(7), 1135.
2 Krivdin L. B., Chernyshev K. A., Rosentsveig G. N., Ushakova I. V., Rosentsveig I. B., Levkovskaya G. G. Magnetic Resonance in Chemistry, 2007, 45, 980.
УДК 547.541.1
,
ПОЛУЧЕНИЕ ТЕТРАГИДРОЦИКЛОПЕНТА[b]ИНДОЛОХИНОНОВ
Институт органической химии УНЦ РАН, г. Уфа
E-mail: dos01@ya.ru
Некоторые представители соединений ряда индолохинонов проявляют биологическую активность, благодаря чему привлекают внимание исследователей [1-3]. Структуры подобного типа могут быть получены как непосредственно из хинонов [4], так и последовательными трансформациями производных индола.
С целью выхода к подобным соединениям мы исследовали их синтез исходя из пара-толуидина (I). По методикам [5] были получены индолины (IIa, б), нитрование которых проводили смесью нитрата аммония и (F3CCO)2O в дихлорметане в мягких условиях. Нагреванием соединений (IIIa, б) со свежеприготовленным Fe(OH)2 в аммиачном растворе синтезировали 5-аминопроизводные (IVa, б), окисление которых солью Фреми приводит к образованию индолохинонов (Vа, б). При попытке введения азиридинового фрагмента в положение 6 соединения (Vа) произошло восстановление хиноидной структуры до гидрохиноновой с образованием гетероцикла (VI).
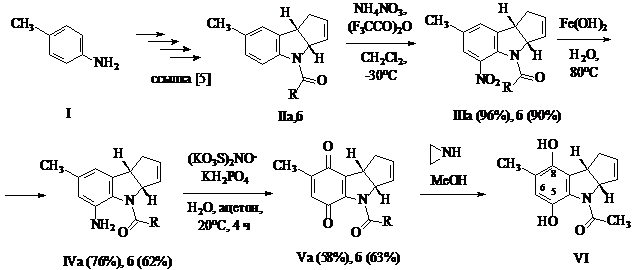
Список литературы:
1 Wang C., Sperry J. J. Org. Chem. 2012, 77, 2584.
2 Xing С., Wu Р., Skibo E. B., Dorr R. T. J. Med. Chem. 2000, 43, 457.
3 Skibo E. B., Xing С., Dorr R. T. J. Med. Chem. 2001, 44, 3545.
4 Luly J. R., Rapoport H. J. Org. Chem. 1984, 49, 1671.
5 , , ЖОрХ. 2012, 48, 962.
УДК 573.6.086.83:550.7
, ,
БИОВЫЩЕЛАЧИВАНИЕ СУЛЬФИДНЫХ МИНЕРАЛОВ КОНСОРЦИУМОМ УМЕРЕННО-ТЕРМОФИЛЬНЫХ ОРГАНИЗМОВ В УСЛОВИЯХ ПОВЫШЕННОЙ КОНЦЕНТРАЦИИ ИОНОВ Fe3+
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
Е-mail:*****@***net
Биовыщелачивание сульфидных минералов заключается в разрушении их кристаллической структуры и высвобождении металлов и серы в виде растворимых форм с участием микроорганизмов. Чаще всего выщелачивание протекает в кислых условиях и достигается за счёт протонных атак на минерал и окисления его компонентов [1]. Микроорганизмы могут принимать участие в биовыщелачивании непосредственно за счёт ферментативного разрушения минерала или опосредованно – за счёт регенерации выщелачивающих агентов, таких как ионы Fe3+ или Н+ [2], а также облегчать химическое выщелачивание минерала ионами Fe3+ благодаря слою внеклеточных полимеров [1]. В настоящее время считается, что основной вклад микроорганизмов в процессы биовыщелачивания заключается в регенерации ионов Fe3+ [1, 3].
Технологии биовыщелачивания являются перспективными поскольку благодаря низким капитальным и эксплуатационным затратам позволяют извлекать металлы из бедных руд, а также отвалов отработанных месторождений, переработка которых традиционными пирометаллургическими методами нерентабельна.
С одного из таких месторождений – отработанного месторождения пирита Куль-Юрт-Тау – нами была выделена накопительная культура микроорганизмов, способная окислять сульфидные минералы. Данная культура продемонстрировала устойчивость к высоким концентрациям железа в среде.
Было обнаружено, что процессы биовыщелачивания пирита и медного концентрата с помощью полученной накопительной культуры интенсифицируются с увеличением концентрации химического окислителя сульфидов (ионов Fe3+) до 40 г/л. Показано, что даже при таких концентрациях происходит не только активное выщелачивание металлов, но и регенерация ионов Fe3+. Обнаружено, что в исследуемых системах не происходит повышения концентрации Fe2+. Полученные данные свидетельствуют о том, что найденный консорциум способен сохранять свою активность даже при концентрациях Fe3+ 75 г/л, что делает его перспективным для применения в процессах биовыщелачивания, поскольку при высоких концентрациях выщелачивающего агента скорость выщелачивания также возрастает.
Список литературы:
1 E. R. Donati, W. Sand Microbial Processing of Metal Sulfides. – Dordrecht, The Netherlands – 2007. – 314 p.
2 Y. Rodríguez, A. Ballester, M. L. Blázquez, F. González, J. A. Muñoz // Hydrometallurgy. – 2003. – Vol. 71. – P.47 – 56
3 D Barrie Johnson, Tadayoshi Kanao, Sabrina Hedrich // Frontiers in microbiology. – 2012. – Vol.3: Art.96.
УДК 547.824:542.91:548.737
,1 ,2 Х. До Тхи Тху,3 1
ОЗОНОЛИЗ ДАММАРАНОВОГО ТРИТЕРПЕНОИДА ДИПТЕРОКАРПОЛА ИЗ DIPTEROCARPUS ALATUS
1Федеральное государственное бюджетное учреждение науки Институт органической химии Уфимского научного центра Российской академии наук,
г. Уфа,
E-mail: *****@***ru
ФГБОУ ВПО Башкирский государственный университет, инженерный факультет, г. Уфа
3Институт химии Вьетнамской академии наук и технологий, г. Ханой, Вьетнам
Тритерпеноиды даммаранового типа, в том числе диптерокарпол, обладают различными видами активности (противораковой, противовирусной, иммуностимулирующей). Учитывая высокие перспективы даммарановых тритерпеноидов как фармакологически ценных агентов (в основном благодаря метаболитам корня женьшеня и листьев березы), а также сырьевую доступность диптерокарпола, нами начаты исследования по его целенаправленной химической модификации.
Одним из путей модификации природных метаболитов является озонолиз. нами осуществлен озонолиз диптерокарпола 1 в среде хлористого метилена, ацетона и спиртах при -40ºС без восстановления перекисных продуктов. В результате взаимодействия диптерокарпола 1 с 1 экв. озона в растворе CH2Cl2 получили триснорлактол 2. Взаимодействие соединения 1 c 2 экв. озона в СН2Сl2 привело к образованию смеси триснорлактола 2 и триснорлактона 3, выделенных колоночной хроматографией с выходами 20 и 68%, соответственно.
Реакция диптерокарпола 1 c 2 экв. озона в ацетоне завершилась образованием триснорлактона 3 с выходом 87%. Взаимодействие индивидуального триснорлактола 2 с 1 экв. озона в растворе CH2Cl2 или ацетона приводило к образованию лактона 3 с количественным выходом.
Озонолиз диптерокарпола 1 в метаноле, этаноле или изопропаноле привел к образованию алкоксилактолов 4, 5 или 6 в виде смеси рацематов по С-24 центру. Структура всех соединений подтверждена спектрами ЯМР 1Н и 13С.
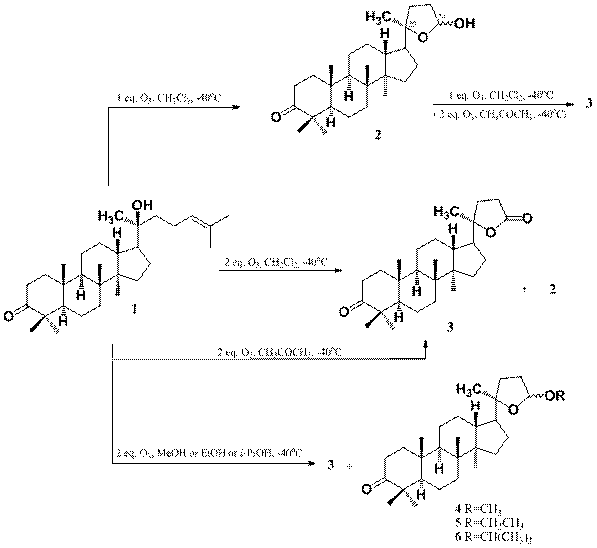
Таким образом, в ходе проведенных реакций наблюдается участие С-20 гидроксигруппы во внутримолекулярной циклизации и взаимодействие с молекулой растворителя по механизму нуклеофильного замещения, что приводит к соединениям с фрагментами лактона, лактола или алкоксилактолов.
Работа выполнена финансовой поддержке гранта РФФИ №10-03-90303.
УДК 378.147:579
, ,
ИССЛЕДОВАНИЕ ВЛИЯНИЯ ПРЕДОБРАБОТКИ ЛИГНОЦЕЛЛЮЛОЗНОГО СЫРЬЯ ГЛИЦЕРИНОМ
НА ЕГО ГИДРОЛИЗ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: *****@***net
Лигноцеллюлозные отходы являются перспективным сырьем для получения практически важных веществ, в том числе биотоплив и биологически активных веществ с помощью микроорганизмов. Вместе с тем гемицеллюлозы и лигнин, содержащиеся в лигноцеллюлозе, являются лимитирующими факторами для ферментативного гидролиза целлюлозы, использующейся микроорганизмами в качестве источника углерода и энергии, поэтому многие исследования направлены на решение вопроса предварительной обработки субстрата для удаления этих нежелательных компонентов без разрушения целлюлозы. Предобработка глицерином, являющимся основным побочным продуктом производства биодизеля, рассматривается как перспективное направление для делигнификации целлюлозного сырья.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 |





