Одними из наиболее опасных промышленных отходов являются фенолы, которые попадают в окружающую среду в районах действия нефтехимических предприятий. Фенолы оказывают существенное влияние на почвенные ферменты (Киреева 1997): в одних случаях стимулирующее (полифенолоксидаза, пероксидаза), в других - угнетающее (каталаза, дегидрогеназа, протеаза, уреаза). Чувствительность ферментативных реакций позволяет использовать их в качестве биотеста на загрязнение почв фенольными соединениями [2, с. 179, 182].
Распад нефти и нефтяных углеводородов в почве связан с окислительно-восстановительными процессами, происходящими при участии различных ферментов. Уровень активности окислительно-восстановительных ферментов – один из критериев самоочищающейся способности почвы от углеводородов нефти. При загрязнении почвы нефтью активность этих ферментов резко изменяется [3, с.103].
В загрязненных нефтью почвах ингибируется дегидрогеназная активность. Почвенные дегидрогеназы ингибируются в наибольшей степени не самими углеводородами, а продуктами их деградации, которые могут аккумулироваться в почве и длительное время оказывать токсическое влияние, несмотря на снижение в почве содержания углеводородов. Загрязнение почв нефтью стимулирует активность оксидоредуктаз, участвующих в процессах гумусонакопления в почве. Значительно снижается активность окислительно-восстановительных ферментов азотного обмена (нитрит - и нитратредуктаз) [3, с. 104].
Загрязнение нефтью, обусловливая микробную сукцессию, определенным образом влияет на биохимические процессы почв, меняя ее ферментативную активность. Низкие концентрации нефти могут стимулировать биологическую активность почвы, а повышенные дозы загрязнения приводит к снижению этого показателя. Полученные данные по активности различных ферментов свидетельствует о возможности применения метода ферментативных реакций для биодиагностики и индикации различных типов почв.
Список литературы:
1 Экологические проблемы нефтедобычи»: Тезисы докладов международной молодежной конференции / отв. ред. . – Уфа: РИЦ БашГУ, 2012.
2 «Экотоксикология»: Материалы Всероссийской молодежной конференции. – Уфа: РИЦ БашГУ, 2012.
3 и др. Экологический менеджмент.- Уфа: РИЦ БашГУ, 2008. – 166 с.
УДК 547.954.681.3.06
, ,
КИНЕТИЧЕСКИЕ ЗАКОНОМЕРНОСТИ РЕАКЦИИ ПОЛИФУНКЦИОНАЛЬНЫХ ОРГАНИЧЕСКИХ КИСЛОТ С ОЗОНОМ
ФГБОУ ВПО «Башкирский государственный университет», г. Уфа
E-mail: xajrullina_1990@mail.ru
Очистка воды от органических соединений всегда являлась актуальной темой. Использование озона в качестве окисляющего агента в процессах очистки воды показало его безопасность с экологической точки зрения, способность глубоко окислять органические вещества, снижать цветность воды, дезинфицировать и улучшать ее вкус и запах. В данной работе были исследованы кинетические закономерности и механизм реакции озона с органическими кислотами в водной среде, что представляет собой существенный практический интерес, так как многие важные процессы с участием О3 (атмосферные процессы, очистка сточных вод) протекают либо в водных растворах, либо в присутствии значительных количеств водяных паров.
За кинетикой процесса следили спектрофотометрически по изменению концентрации О3 в реакционной смеси. В качестве объектов исследования были выбраны масляная, молочная, малоновая, янтарная, яблочная, лимонная и галактуроновая кислоты. Опыты проводили при 40-80ºC. Начальные концентрации кислот [S] в реакционной смеси изменяли в диапазоне (0,1¸1,0)×10–3 моль/л, озона – (3,2¸4,9)×10–4 моль/л. При этом в проводимых экспериментах всегда выполнялось условие: [S]0 >> [O3]0.
Исследования показали, что скорость расходования озона в реакции с полифункциональными кислотами подчиняется следующему кинетическому закону:
υ= k·[S]·[O3],
где k – константа скорости реакции озона с изученными кислотами.
Согласно полученным данным, наблюдается следующий порядок реакционной способности органических кислот по отношению к озону (70ºС): янтарная < масляная < лимонная < малоновая < яблочная < молочная < галактуроновая.
Исследуя зависимость между lgA и Е, выявили линейную корреляцию - компенсационный эффект:
lgA = (3.35 ± 1.30) + (0.58 ± 0.11)×Е,
(коэффициент корреляции r = 0.99).
Приведенная корреляционная зависимость кинетических параметров свидетельствует о едином механизме лимитирующей стадии окисления полифункциональных кислот озоном.
УДК 547.94:834.2
2, 1, 1
СИНТЕЗ 3- И 5-N-ЭТИЛОКСИПРОИЗВОДНЫХ НЕКОТОРЫХ ХИНОЛИЗИДИНОВЫХ АЛКАЛОИДОВ
1 ФГБУН Институт органической химии Уфимского научного центра Российской академии наук, г. Уфа
E-mail: tsipisheva@anrb.ru
2 ГОУ ВПО «Башкирский государственный университет», г. Уфа
Известно, что 12-N-этилоксипроизводное хинолизидинового алкалоида
(-)-цитизина обладает высокой антиаритмической активностью [1]. С целью изучения взаимосвязи «структура – антиаритмическая активность» получены производные метилцитизина 2 и термопсина 3 с N-этилоксифрагментом в
2-пиридоновом ядре. Синтез целевых соединений был осуществлен путем сочетания соответствующих галоидпроизводных с моноэтаноламином в присутствии соли одновалентной меди.
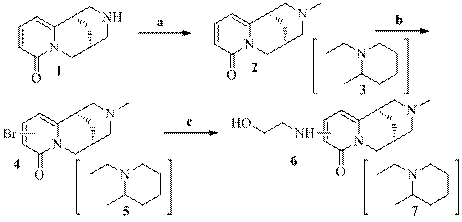
Реагенты и условия: а) MeI, K2CO3, ацетон, 56 oC; б) KBr, H2O2, H2SO4, 20 oC; c) моноэтаноламин, CuCl, KOH, 90 oC.
Соответствующие 3-, 5-бром и 3,5-дибромпроизводные общих формул 4 и 5, получены согласно [2] и разделены методом колоночной хроматографии на SiO2. Последующие стадии сочетания с моноэтаноламином в указанных условиях привели к соответствующим N-этилоксипроизводным 6 и 7 с выходами от 43 до 61%.
Работа выполнена при поддержке гранта РФФИ № 12-03-97027-р_поволжье_а.
Список литературы:
1 D. V. Shishkin, A. R. Shaimuratova, A. N. Lobov, N. Z. Baibulatova, L. V. Spirikhin, M. S. Yunusov, N. S. Makara, N. Zh. Baschenko, V. A. Dokichev, Chemistry of Natural Compounds, 43, 190, (2007).
2 A. V. Kovalskaya, A. N. Lobov, I. P. Tsypysheva, V. I. Vinogradova, J. V. Vakhitova, M. S. Yunusov, Organic Chemistry:an Indian Journal, 8, 3, 117 (2012).
УДК 547.917
, ,
ЛЕВОГЛЮКОЗЕНОН В СИНТЕЗЕ ПРОИЗВОДНОГО ДЕКАНОЛИДА И ЕГО ПРЕВРАЩЕНИЕ В ЭФИР N-МЕТИЛУРОКАНОВОЙ КИСЛОТЫ
Федеральное государственное учреждение науки
Институт органической химии Уфимского научного центра РАН; г. Уфа
E-mail: *****@***ru
С целью изучения возможностей синтеза оптически активных лактонов среднего размера цикла мы использовали в качестве хирального источника левоглюкозенон.
Так, взаимодействием левоглюкозенона с морфолинцигексеном в EtOH получили аддукт Михаэля 2a,b. Обработка диастереомерных пар 2a,b HCl-MeOH сопровождается их превращением в три - 3а и тетраметилкетали 3b.
Расщепление пиридинийхлорхроматом (РСС) мостиков с кетальной функцией в голове моста соединений 3a,b привело к образованию среднециклического лактона 4.
Для синтеза потенциального цитотоксического N-метилуроканата действием NaBH4 восстановили деканолид 4 в спирт. Реакция сопровождается раскрытием лактонного кольца и этерификацией карбоксильной группы в этиловый эфир. Полученный дигидроксиэфир 5 ввели в реакцию этерификации с N-метилурокановой кислотой в описанных выше условиях. При этом произошла этерификация более активной первичной ОН-группы с образованием N-метилуроканата 7, представляющего собой ациклическую форму N-метилуроканата деканолида 4.
Схема 1
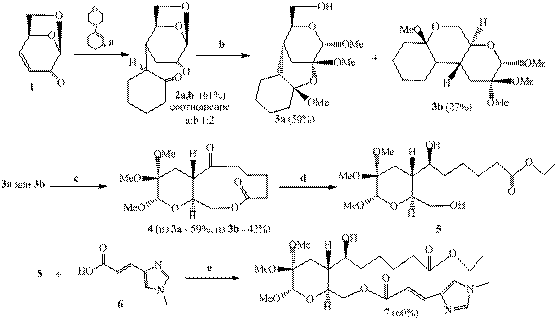
Реагенты и условия: a) 1. EtOH, 2. 3%-ный HCl в H2O; b) HCl-MeOH; с) PCC, CH2Cl2; d) NaBH4, EtOH; е) DCC, DMAP, CHCl3, кипячение.
Работа выполнена при финансовой поддержке гранта РФФИ-Поволжье “11-03-97024-р_поволжье_а”
УДК 573.6.086:582.28
, ,
ИССЛЕДОВАНИЕ ВЛИЯНИЯ ЛИГНОЦЕЛЛЮЛОЗНОГО СЫРЬЯ
НА ЛАККАЗНУЮ АКТИВНОСТЬ ГРИБОВ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: bio@rusoil.net
Лакказа (КФ 1.10.32, дифенол:кислород-оксидоредуктаза), катализирующая окисление различных органических соединений с одновременным восстановлением кислорода воздуха до воды без образования пероксида водорода, часто обнаруживается у грибных микроорганизмов.
Лакказа грибов играет важную роль в разложении растительных лигнинсодержащих материалов, гумификации органических остатков, а также выполняет функции образования плодовых тел, образования пигментов, детоксификации ксенобиотиков. Большинство грибов продуцирует несколько изоформ и изоферментов лакказ.
В качестве эффективных индукторов синтеза лакказы могут выступать их естественные субстраты, например, лигноцеллюлоза.
Целью работы являлось исследование влияния лигноцеллюлозного сырья (древесных опилок, травяной соломы, пшеничных отрубей) на лакказную активность грибов.
В работе исследованы условия культивирования базидиомицетов Russula vesca (сыроежка), Pleиrotus ostreatus (вешенка устричная), Agaricus arvensis (шампиньон) на жидких питательных средах в присутствии 2 % масс. опилок, соломы, отрубей в течение 20 сут.
Обнаружено, что исследуемые грибы проявляют максимум лакказной активности (42-37 ед/мл для Pleиrotus ostreatus и 16-22 ед/мл для Russula vesca) при росте на отрубях на 14-18 сутки.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 |





