Биологические методы очистки можно подразделить на два типа:
- методы микробиодеградации загрязнителей;
- методы биопоглощения и перераспределения загрязнителей.
Методы микробиодеградации основаны на деструкции загрязнителей различными видами микроорганизмов. Эффект достигается за счет активизации аборигенной микрофлоры или внесения в грунт определенных культур микроорганизмов, а также всевозможных комплексных препаратов. В результате этого микроорганизмы начинают активно поглощать загрязнитель и вызывать его деструкцию. Ускоряют биодеградацию нефти целлюлозосодержащие отходы — солома, опилки. Эффективно внесение опилок со стимуляторами разложения нефти.
Технология микробиологического обезвреживания органических экотоксикантов основаны на активации аборигенной микрофлоры или внесении в грунт культур определенных микроорганизмов и создании оптимальной среды для их развития.
Идеальной для биоразложения является нейтральная среда. Для нейтрализации щелочных грунтов вносят гипс, для нейтрализации кислых грунтов — известь.
Одним из методов, обеспечивающих диспергирование нефтяных загрязнений и улучшающих контакт с микроорганизмами, является внесение поверхностно-активных веществ (ПАВ). Сочетание применения ПАВ с внесением минеральных удобрений ускоряет биодеструкцию.
Внесение культур микроорганизмов используется только при аварийных загрязнениях или при отсутствии развитого естественного биоценоза. Однако иногда происходит вырождение микроорганизмов до достижения требуемого уровня очистки. Их применение также может нарушать естественные биоценозы.
Обычно для очистки используют сообщества бактерий Bacterium, Actinomyces, Artrobactes, Thiobacterium, desullfotomasilium Pseudomons, Hydiomonas, Bacillus и другие, а также низшие формы грибов.
В России для очистки от нефтепродуктов используют бактериальные препараты «Деворойл», «Олеоворин», «Путидойл», «Сойлекс», «Фаерзайн» и др.
Биопрепараты содержат в своем составе удобрения и микроорганизмы, выделенные из природных биоценозов, обладающие повышенной окислительной способностью по отношению к нефти, прошедшие адаптацию в естественных условиях.
Используют либо один штамм, либо смесь штаммов углеводородоокисляющих бактерий, в основном аэробов.
Препараты эффективно окисляют нефтепродукты, ароматические углеводороды в температурном диапазоне от –5 до +45 °C при значительных начальных концентрациях загрязнений в грунтах.
Биологическая очистка находит широкое применение во всем мире и продолжает усовершенствоваться и развиваться.
Список литературы:
1 , Башин допустимое содержание нефтепродуктов в почвенных экосистемах Пермской области// Известия вузов. Нефть и газ. 2004. №2. С.91-96.
2 , "Химия воды и микробиология" М: Стройиздат, 1983
3 Протасов , здоровье и природопользование в России /, - М.: Изд-во Финансы и статистика, 1995. –
528 с.
УДК 622.276.64
О ПРИМЕНЕНИИ БИОПАВ ПРИ РАЗРАБОТКЕ НЕФТЯНЫХ МЕСТРОЖДЕНИЙ
ФГБОУ ВПО «Башкирский государственный университет», г. Уфа
E-mail:dodger86@ya.ru
Большинство крупных месторождений в России находятся на поздней стадии разработки, как следствие наблюдается ухудшение качества остаточных запасов нефти с переходом их в разряд трудноизвлекаемых. Повышению коэффициента извлечения нефти способствует применение методов увеличения нефтеотдачи. Одним из таких методов являются химические методы, основанные на повышении коэффициента вытеснения нефти водными растворами поверхностно-активных веществ (ПАВ).
При выборе ПАВ, используемого при заводнении, внимание уделяют их физико-химическим свойствам, стоимости ПАВ, наличию источников сырья и экологической безопасности. Проблема синтеза хорошо биоразлагаемых ПАВ приобрела в настоящее время особенную актуальность [1].
Перспективным направлением при заводнении пластов является применение ПАВ биологического происхождения (биоПАВ). Их преимущество перед синтетическими – биодеградабельность при высоких температурах, рН, концентрации солей в пластовой воде. Данные ПАВ могут быть разделены на две основные группы:
1) низкомолекулярные соединения, называемые собственно биоПАВ, представленны гликолипидами (глюколипиды, рамнолипиды, трегалозолипиды, софоролипиды) и липопептидами (сурфактин, стрептофактин, полимиксин, грамицидин). Они эффективно снижают поверхностное и межфазное натяжение на границе «вода-нефть»;
2) высокомолекулярные соединения, называемые биоэмульгаторами, представленны полисахаридами, липополисахаридами, липопротеинами, протеинами, и их комплексами [2]. Данная группа объединяет полимеры, которые эффективны для стабилизации эмульсий типа «масло в воде».
Масштабное внедрение технологий повышения нефтеотдачи с применением биоПАВ было осуществлено в . Использовался биоПАВ КШАС-М, который представляет собой природную композицию гликолипидной природы, продуцируемую культурой микроорганизмов Pseudomonas aeruginosa S-7. Растворы биоПАВ КШАС-М могут снижать поверхностное натяжение воды до 30 мН/м, обладают высокой эмульгирующей Е24 до 60-80%, где E24 - устойчивость эмульсии в течение 24 часов.
В 1995 г. проведены опытно-промысловые работы по применению биоПАВ на Северо-Сергеевской площади Сергеевского месторождения республики Башкортостан. Была осуществлена обработка нагнетательных скважин с БКНС № 3. После закачки биоПАВ среагировали 29 добывающих скважин. Дополнительная добыча нефти по этим скважинам составила за шесть месяцев около 2,5 тыс. т. Удельный технологический эффект составил 54 т дополнительной нефти на 1 т биореагента [3].
Список литературы:
1 Петров анионных и катионных ПАВ для применения в нефтяной промышленности / , , : Учеб. пособие/ УГНТУ.– Уфа, 2008. – 54с.
2 и др. Образование нефтевытесняющих соединений микроорганизмами из нефтяного месторождения Дацин (КНР) / , , -Ф., , // Микробиология, 2003, №2. – C.206-211.
3 Сафонов извлечения остаточной нефти на месторождениях Башкортостана. – Уфа: РИЦ АНК "Башнефть", 1997. – 247 с.
УДК 547.94:834.2
2, 1, 1
Восстановительное алкилирование
3-аминометилцитизина
1 ФГБУН Институт органической химии Уфимского научного центра Российской академии наук, г. Уфа
E-mail: tsipisheva@anrb.ru
2 ГОУ ВПО «Башкирский государственный университет»,г. Уфа
Ранее нами показано, что производные хинолизидинового алкалоида
(-)-цитизина, несущие в 2-пиридоновом ядре карбоксамидные группы проявляют высокую ноотропную активность [1]. С целью расширения круга тестируемых соединений получен новый скаффолд производных 2-14 путем восстановительного алкилирования 3-аминометилцитизина 1.
В реакцию вовлечены метокси-, гидрокси - замещенные бензальдегиды, пиридин-3-бензальдегид, терефталевый и коричный альдегиды, а также фурфурол, тиофен-, имидазол - и тиазолкарбальдегид.
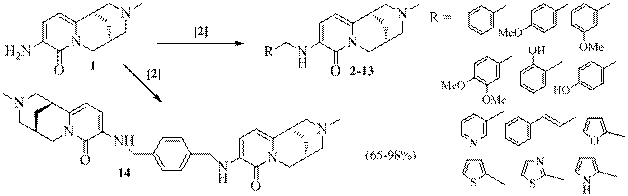
Структура вторичных аминов 2-13 установлена на основании данных спектроскопии ЯМР 1Н и 13С.
Работа выполнена при поддержке гранта РФФИ № 12-03-00724-а.
Список литературы:
1 , , Химия природных соединений, 4, 565 (2012).
2 Sh. B. Rakhimov, V. I. Vinogradova, Yu. R. Mirzaev, N. L. Vypova, D. S. Kazantseva, Chemistry of Natural Compounds, 42, 462 (2006).
УДК 547.94:834.2
2, 1, 1
Формилирование N-метилцитизина
1 ФГБУН Институт органической химии Уфимского научного центра Российской академии наук, г. Уфа
E-mail: tsipisheva@anrb.ru
2 ГОУ ВПО «Башкирский государственный университет», г. Уфа
Известно, что продукты функционализации 2-пиридонового ядра хинолизидинового алкалоида (-)-цитизина проявляют высокую нейрофизиологическую активность [1]. Стратегия синтеза этих соединений практически во всех случаях базируется на синтетической последовательности «электрофильное галогенирование – кросс-сочетание», что позволяет ввести в 2-пиридоновое ядро арильные, алкильные, алкенильные и алкинильные фрагменты [2].
Описан способ синтеза 3-формильного производного 3 путем карбонилирования магнийорганического соединения полученного из соответствующего галогенида 2 [2a].
Нами реализовано прямое формилирование N-метилцитизина по методу Даффа с выходом 82%.
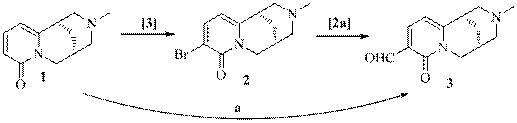
Реагенты и условия: а) уротропин, CF3COOH, 70 оС.
Структура альдегида 3 установлена на основании данных спектроскопии ЯМР 1Н и 13С. Физико-химические константы 3 соответствуют литературным данным [2a].
Работа выполнена при поддержке гранта РФФИ № 12-03-00724-а.
Список литературы:
1 E. G. Pérez, C. Méndez-Gálvez, B. K. Cassels, Nat Prod Rep, 29, 55 (2012)
2 a) WO 1998/018798; b) WO 2007/100430 A2; c) WO 2007/115092 A2.
3 A. V. Kovalskaya, A. N. Lobov, I. P. Tsypysheva, V. I. Vinogradova, J. V. Vakhitova, M. S. Yunusov, Organic Chemistry:an Indian Journal, 8, 3, 117 (2012).
УДК 543.422.25
1, 2, 2,
2, 1, 2
СТРУКТУРА ПРОДУКТОВ ОКИСЛЕНИЯ 2,3-ИНДОЛО-28-ОКСОАЛЛОБЕТУЛИНА ПО ДАННЫМ ЯМР СПЕКТРОСКОПИИ.
1 Башкирский государственный университет, г. Уфа
2 Институт органической химии Уфимского научного центра РАН, г. Уфа, e-mail:lobovan@anrb.ru

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 |





