Известен также способ получения пластификатора из кубового остатка производства бутиловых спиртов и кубового продукта дистилляции фталевого ангидрида в присутствии металлоорганического или кислотного катализатора [2]. Себестоимость этого пластификатора невысокая, однако темный цвет, относительно низкая температура вспышки (1850С) и наличие в продукте тяжелых не эфирных примесей ухудшают его пластифицирующие свойства.
Сложные эфиры терефталевой кислоты и спиртов С4-С10 составляют группу пластификаторов, наиболее близких по свойствам к о-фталатным пластификаторам. Причем, по сравнению с последними эфиры терефталевой кислоты аналогичного строения имеют меньшую летучесть, улучшенные эластичность при низкой температуре (при равной твердости) и стабильность, пониженную вязкость пластизолей, хорошие электрические свойства. В промышленности используется диоктилтерефталат (ДОТФ), получаемый этерификацией терефталевой кислоты 2-этилгексанолом, однако объемы его производства и потребления несравнимо ниже, чем у ДОФ. Известен импортный аналог ДОТФ под торговой маркой «неортофталат».
Известен способ получения ДОТФ переэтерификацией 2-этилгексанолом метиловых эфиров терефталевой и других фталевых кислот, содержащихся в побочном продукте производства диметилтерефталата [3]. К недостаткам этого способа получения следует отнести относительно высокую стоимость пластификатора вследствие использования чистого 2-этилгексанола и выделение метанола в процессе реакции, что усложняет технологический процесс и требует дополнительных затрат на его утилизацию.
Целью работы является получение недорогого пластификатора для ПВХ композиций с хорошими пластифицирующими свойствами на основе многотоннажных промышленных и бытовых отходов. Ранее в работе [4] рассмотрен способ получения пластификатора ДОТФ на основе технической ТФК (отход производства ТФК, ) и кубового остатка ректификации 2-этилгексанола (отход производства 2-этилгексанола, нефтехим Салават»).C целью расширения сырьевой базы проекта проведено исследование применимости вторичной ТФК вместо технической ТФК.
Работа проводилась в 2 этапа: получение вторичной ТФК, смесь соединений (1) и (2), путем химического разложения ПЭТФ-бутылкии синтез на её основе с 2-этилгексанолом (3) ДОТФ(4) (рис.1):
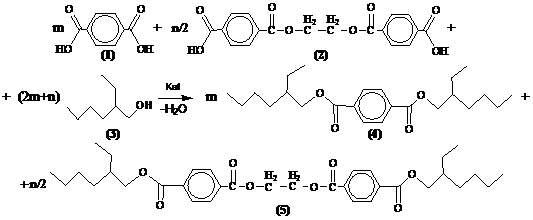
Рисунок 1 - Реакция получения пластификатора на основе вторичной ТФК
Процесс осуществляется в 3 стадии: азеотропная осушка ТФК 2-этилгексанолом, синтез ДОТФ с использованием катализатора тетрабутоксититана, отгонка непрореагировавшего 2-этилгексанола под вакуумом. Следует отметить, что использование в синтезе вторичной ТФК приводит к увеличению времени реакции с 7 до 17 часов, что скорее всего объясняется худшей растворимостью исходного компонента (2).
Полученный пластификатор в ходе исследований показал хорошую совместимость с ПВХ и обладает температурой вспышки 1970С.
Список литературы:
1 Пат. 2171267 Россия, МКИ С08К5/10. Пластификатор для поливинилхлоридных композиций / , , - Заявл. 15.07.99, Опубл. 27.07.01.
2 Пат. 2235716 Россия, МКИ С08К5/12. Способ получения пластификатора / - Заявл. 07.05.03, Опубл. 10.09.04.
3 Пат. 98748 ПНР, МКИ С08К5/10. Способ получения пластификаторов / PenczekP., MatyniaT. - Заявл. 23.04.76, Опубл. 31.08.78.- РЖХ.- 1979.- 14Т55П.
4 , , // Пластификатор диоктилтерефталат из отходов производства и . Баш. хим. ж. - 2010. - Т.17, №4. - С. 85
УДК 661.744.24, 66.063.72
, ,
ХИМИЧЕСКИЙ РЕЦИКЛИНГ ВТОРИЧНОГО ПЭТФ С ПОЛУЧЕНИЕМ ВОСТРЕБОВАННОЙ НА РЫНКЕ ПРОДУКЦИИ
ФГБОУ ВПО Уфимский государственный нефтяной технический университет, г. Уфа
E-mail: *****@***ru
В 2011 году глобальное потребление полиэтилентерефталата (ПЭТФ) выросло на 6,4% до 17,7 млн. т., при таком потреблении актуальной технологической и коммерческой задачей, учитывая дороговизну первичного ПЭТФ, становится эффективная утилизация ПЭТФ-отходов. Однако в Восточной Европе и России собирается только 10% отходов [1]. С 2000 г. в России наблюдается формирование рынка по переработке использованных ПЭТФ-бутылок с наиболее распространенным механохимическим способом. В работах [2,3] показаны возможности применения различных растворов (кислотных, щелочных, в аминах) отходов ПЭТФ, в производстве пенополиуретанов. В [4] рассмотрен способ химического термолиза полиэтилентерефталата, основным продуктом которого является бензойная кислота, выход которой зависит от природы и концентрации катализатора и составляет от 9 до 25,5%.Также известна глубокая химическая переработка ПЭТФ – сольволиз, ПЭТФ подвергается деполимеризации при взаимодействии с химическими веществами. Эти методы достаточно энергоемки, требуют высокотехнологичного оборудования и поэтому весьма дорогостоящи, однако они дают возможность использовать сырье более низкого качества. Продукты деструкции ПЭТФ из устаревших отходов широко используют снова в синтезе ПЭТФ, для получения пластификаторов, лаков, материалов для покрытий и др.[5].Такой химический рециклинг стимулирует исследования по применению получаемых продуктов в качестве сырья, что способствует расширению сырьевой базы и экономии первичных сырьевых ресурсов и как следствие позволяет снизить нагрузку на природу.
Работа посвящена исследованию применимости вторичной ТФК, полученной в результате химической переработки ПЭТФ-бутылки, для получения пластификатора ДОТФс целью расширения сырьевой базы проекта. Ранее в работе [6] рассмотрен способ получения пластификатора ДОТФ на основе технической ТФК (отход производства ТФК, ) и кубового остатка ректификации 2-этилгексанола (отход производства 2-этилгексанола, нефтехим Салават»).
Переработка ПЭТФ проводилась в несколько этапов: подготовка сырья (сортировка, измельчение, отмывка), гидролиз в среде этиленгликоля в присутствии щелочи натрия, нейтрализация полученной массы разложения, фильтрация, промывка и сушка ТФК. Предполагаемая реакция представлена на рис.1.

Рисунок 1 - Гидролиз ПЭТФ
В результате был получен мелкодисперсный порошок молочного цвета, который был исследован для идентификации на ИК-Фурье спектрометре. Полученный спектр сравнивался с ИК-спектром чистой терефталевой кислоты, на основании этого сделан вывод, что полученный продукт преимущественно содержит терефталевую кислоту. Полученная смесь вторичной ТФК находит свое применение в качестве сырья для получения пластификатора, рис.2.

Рисунок 2 - Реакция получения пластификатора на основе вторичной ТФК
Список литературы
1 ПЭТФ 2008: отчет о конференции/newchemistry. ru: новые химические технологии. 2012.URL:http://www. newchemistry. ru/ letter. php? n_id=3122&cat_id=0&page_id=1 (датаобращения: 29.02.12)
2 , , Кольцов отходов ПЭТФ путем использования их кислотных и щелочных растворов при получении пенополиуретанов // Пластические массы №2, 2008, с. 42-46.
3 , , Кольцов отходов ПЭТФ с использованием их их растворов в аминах при получении пенополиуретанов // Пластические массы №3, 2008, с. 48-50.
4 , , // Исследование термического разложения полиэтилентерефталата. Известия вузов. Химия и химическая технология – 2010.-Т.53, №2. – с.94-97
5 , , Сазонов : новые направления рециклинга // Доклады участников семинара «Экологические проблемы современности», ФГБОУ ВПО Майкопский государственный технологический университет, 2012. URL: http://mkgtu. ru/print/a1189/ (дата обращения 14.03.2012)
6 , , // Пластификатор диоктилтерефталат из отходов производства и . Баш. хим. ж. - 2010. - Т.17, №4. - С. 85
УДК 546.215: 661.882
, ,
Активность титаносиликатов в разложении пероксида водорода
Институт нефтехимии и катализа РАН, г. Уфа
Е-mail: *****@***ru
Ранее в лаборатории приготовления катализаторов ИНК РАН по запатентованной методике [1,2] была синтезирована серия микро-мезопористых титаносиликатов [3] с целью использования их в качестве катализаторов жидкофазного окисления алкилфенолов пероксидом водорода. Для оценки эффективности использования окислителя в реакции окисления алкилфенолов, синтезированные титаносиликаты первоначально исследовали в реакции разложения пероксида водорода. Эффективность использования пероксида водорода в реакциях жидкофазного окисления (селективность по Н2О2) органических соединений является важной характеристикой каталитического процесса и оценивается по соотношению скоростей расходования Н2О2 в целевой реакции окисления органического субстрата и в реакции непродуктивного разложения Н2О2 на данном катализаторе [4]. Кроме того, известно, что реакцию разложения H2O2 в отсутствии субстрата можно использовать для первоначальной оценки активности титаносиликатных катализаторов в реакциях окисления [5].
Целью данной работы являлось изучение реакции разложения водных растворов пероксида водорода в присутствии аморфных и кристаллических микро-мезопористых титаносиликатов в сравнении с алюмосиликатом, диоксидом кремния и диоксидом титана.
Изучено влияние текстурных характеристик катализаторов и таких параметров реакции как исходная концентрация Н2О2, температура, концентрация катализатора, продолжительность реакции на степень разложения пероксида водорода.
Эксперименты проводили с использованием 1, 3, 5 и 10 %-ного водного раствора Н2О2 в присутствии 1, 5 и 10 мас.% катализатора в термостатируемых вращающихся реакторах при 30, 50 и 70оС в течение 0,5-2ч. В качестве катализаторов использовали титаносиликаты (соотношение Ti/Si составляет 1/45, 1/30, 1/20, 1/10) с различными текстурными характеристиками в сравнении с TS-1, SiO2, TiO2 и Al2O3-SiO2. Остаточное количество Н2О2 в реакционной массе определяли методом йодометрического титрования.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 |





