Биохимическое исследование крови проводят для уточнения активности воспалительного процесса. Определяют содержание общего белка и его фракций, а также СРВ, сиаловых кислот и серомукоида в сыворотке крови. Повышение их уровня характерно для воспалительного процесса любой локализации. Решающая роль в оценке степени активности воспаления в бронхах принадлежит данным бронхоскопической картины, исследованию содержимого бронхов и мокроты.
При неконтролируемом прогрессировании процесса следует проводить иммунологическое исследование крови и/или бронхиального содержимого.
Исследование мокроты и бронхиального содержимого помогает установить выраженность воспаления. При выраженном воспалении содержимое преимущественно гнойное или гнойно-слизистое, содержит много ней-трофилов и единичные макрофаги, скудно представлены дистрофически измененные клетки мерцательного и плоского эпителия.
Для умеренно выраженного воспаления характерно содержимое ближе к слизисто-гнойному; количество нейтрофилов увеличено незначительно. Растет количество макрофагов, слизи и клеток бронхиального эпителия.
При слабо выраженном воспалении бронхиальное содержимое преимущественно слизистое, преобладают слущенные клетки эпителия бронхов; макрофагов и нейтрофилов мало.
53
Обнаружение эозинофилов свидетельствует о местных аллергических реакциях. Наличие в мокроте атипических клеток, микобактерий туберкулеза, эластических волокон играет существенную роль в пересмотре существовавшей ранее диагностической концепции соответственно в пользу бронхогенного рака, туберкулеза, абсцесса легкого.
Микробиологическое исследование мокроты и содержимого бронхов важно для выявления этиологии обострения хронического бронхита и выбора антимикробной терапии.
Критерием этиологической значимости возбудителя при количественном микробиологическом исследовании служат:
а) выявление возбудителя (пневмококк или гемофильная палочка) в
мокроте в концентрации 106 в 1 мкл и выше при отсутствии антибактери
альной терапии;
б) обнаружение в 2 — 3 исследованиях с интервалом в 3 — 5 дней
условно-патогенных микроорганизмов в концентрации 106 в 1 мкл и
выше;
в) исчезновение или значительное уменьшение количества микроорга
низмов при динамическом исследовании на фоне клинически эффективной
антибактериальной терапии.
Осложнения. Все осложнения ХБ можно разделить на две группы:
1) непосредственно обусловленные инфекцией: а) пневмония, б) брон-
хоэктазы, в) бронхоспастический (неаллергический) и астматический (ал
лергический) компоненты;
2) обусловленные эволюцией бронхита: а) кровохарканье, б) эмфи
зема легких, в) диффузный пневмосклероз, г) легочная недостаточность,
д) легочное сердце — компенсированное и декомпенсированное с развити
ем правожелудочковой сердечной недостаточности. Тяжелейшим осложне
нием обструктивного бронхита является острая дыхательная недостаточ
ность с быстро прогрессирующими нарушениями газообмена и развитием
острого респираторного ацидоза.
Диагностика. Распознать ХБ на первоначальном этапе исследования несложно по данным анамнеза и наличию трех основных симптомов: кашля, мокроты и одышки. Учитывают также характер дыхания и наличие хрипов.
Необходимо исключение других болезней, которые могут протекать с теми же симптомами (туберкулез, рак бронха, бронхоэктазии и Др.).
Результаты лабораторно-инструментальных исследований используют в основном для уточнения фазы активности воспалительного процесса, формы заболевания и дифференциальной диагностики.
Диагностическая значимость различных симптомов позволяет выделить диагностические критерии первичного ХБ.
• «Кашлевой анамнез» (не менее 2 лет по 3 мес подряд; кашель сухой
или с выделением мокроты).
• Отсутствие другой патологии бронхолегочного аппарата (туберку
лез, бронхоэктатическая болезнь, хроническая пневмония, бронхи
альная астма, рак легкого и др.), обусловливающей «кашлевой
анамнез».
54
• Воспалительные изменения в бронхах (при отсутствии бронхоэкта-
зов) по данным исследования мокроты, содержимого бронхов,
бронхоскопической картины.
• Выявление обструкции дыхательных путей (ее обратимого и необ
ратимого компонента) для диагностики хронического обструктивно-
го бронхита.
Формулировка развернутого клинического диагноза хронического бронхита осуществляется с учетом следующих компонентов: 1) клинический вариант, 2) форма ХБ, 3) фаза процесса (обострение — ремиссия), 4) осложнения. При формулировке диагноза хронического необструктив-ного бронхита термин «необструктивный» может быть опущен.
Лечение. Цель лечения — снижение темпов прогрессирования диффузного повреждения бронхов, ведущего к нарастающей дыхательной недостаточности, снижение частоты обострений, удлинение ремиссии, повышение толерантности к физической нагрузке, улучшение качества жизни.
Основным направлением лечения и профилактики прогрессирования ХБ является устранение воздействия вредных примесей во вдыхаемом воздухе (запрещение курения, устранение воздействия пассивного курения, рациональное трудоустройство. Само же лечение ХБ должно быть дифференцированным и зависеть от формы болезни и наличия тех или иных осложнений.
Лечение ХБ состоит из комплекса мероприятий, несколько различающихся в периоде обострения и ремиссии болезни. Выделяется два основных направления лечения в период обострения: этиотропное и патогенетическое.
Этиотропное лечение направлено на ликвидацию воспалительного процесса в бронхах и включает терапию антибиотиками, антисептиками, фитонцидами и пр. Антибиотики назначают с учетом чувствительности флоры, высеянной из мокроты или бронхиального содержимого. Если чувствительность определить невозможно, то следует начинать лечение с антибиотиков пенициллинового ряда (пенициллин, ампициллин). В случае их непереносимости вводят антибиотики группы цефалоспоринов (це-фамезин, цепорин). В последние годы назначают макролиды новых генераций (сумамед, рулид), обладающие особой эффективностью. К ним чувствительны основные возбудители обострения катарального или гнойного бронхита (палочка инфлюэнцы, пневмококки, марокселла). Эти препараты применяют внутрь. При отсутствии эффекта — антибиотики группы резерва (гентамицин и др.). Наиболее предпочтительный способ введения — интратрахеальный (заливка гортанным шприцем или через бронхо-скоп). При выраженной активности воспалительного процесса в бронхах и гнойном его характере местное (интратрахеальное) введение антибиотиков должно сочетаться с парентеральным.
При простом (катаральном) хроническом бронхите основным, а в большинстве случаев и единственным методом лечения является использование отхаркивающих препаратов, направленных на нормализацию мукоцилиар-ного клиренса и профилактику присоединения гнойного воспаления.
Патогенетическое лечение направлено на улучшение легочной вентиляции; восстановление бронхиальной проходимости; борьбу с легочной гипертензией и правожелудочковой недостаточностью.
55
Улучшению (восстановлению) нарушенной легочной вентиляции, помимо ликвидации воспалительного процесса в бронхах, способствуют ок-сигенотерапия и занятия ЛФК.
Основное в терапии ХБ — восстановление проходимости бронхов, что достигается путем улучшения их дренажа и ликвидации бронхо-спазма.
Для улучшения бронхиального дренажа назначают отхаркивающие (горячее щелочное питье, отвары трав, мукалтин и др.), муколитические препараты — ацетилцистеин, бромгексин, амбраксол (лазолван, ласоль-ван).
Недопустимо практиковавшееся ранее применение в качестве муколи-тиков протеолитических ферментов. С успехом используется лечебная бронхоскопия. Перспективно применение низкочастотной ультразвуковой бронхоскопической санации [Овчаренко СИ. и др., 1985].
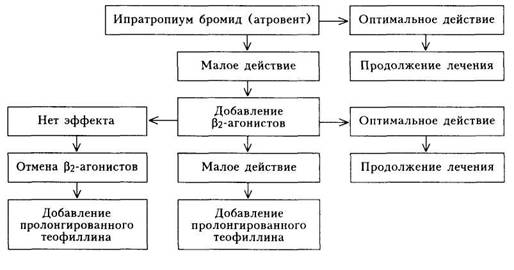
С целью ликвидации бронхоспазма применяют бронхорасширяющие препараты. Бронхолитическая терапия является основной (базисной) в лечении больных хроническим обструктивным бронхитом. Используют антихолинергические препараты (ипратропиум бромид — атровент, отечественный препарат — тровентол); комбинация атровента и фенотерола (беродуал) и метилксантины (эуфиллин и его производные). Наиболее предпочтителен и безопасен ингаляционный путь введения лекарственных веществ. Эффективны также препараты пролонгированного эуфиллина (теопэк, теодур, теобиолонг и пр.), которые назначают внутрь всего 2 раза в сутки.
На схеме 6 представлен алгоритм формирования бронхорасширяю-щей терапии больных хроническим обструктивным бронхитом.
При отсутствии эффекта такой терапии вводят небольшие дозы кор-тикостероидов внутрь (10—15 мг преднизолона в сутки) или интратрахе-ально (суспензия гидрокортизона — 50 мг), ингаляции ингакорта по 500 мкг 2 раза в сутки.
Для борьбы с легочной гипертензией используют длительные (несколько часов) ингаляции кислорода, по показаниям — блокаторы кальциевых каналов: верапамил (финоптин, кордафен и т. п.) и пролонгированные нитраты (нитросорбид, нитронг и др.).
Лечение правожелудочковой недостаточности проводят по общим принципам лечения сердечной недостаточности (сердечные гликозиды, мочегонные средства и пр.; более подробно см. «Легочное сердце»).
В качестве дополнительной терапии назначают:
1) лекарственные средства, подавляющие каш левой рефлекс: при
малопродуктивном кашле — либексин, тусупрекс, бромгексин, при над
садном кашле — кодеин, дионин, стоптуссин;
2) лекарственные средства, повышающие сопротивляемость организ
ма: витамины А, С, группы В, биогенные стимуляторы.
В настоящее время при лечении ХБ (особенно затяжных обострений, часто рецидивирующих и гнойных форм) все шире применяют иммуно-корригирующие препараты: Т-активин или тималин (по 100 мг подкожно в течение 3 дней); внутрь — с успехом применяют бактериальные иммуно-корректоры: рибомунил (рибосомально-протеогликановый комплекс из четырех наиболее распространенных возбудителей), бронхомунал (лио-филизированный лизат восьми основных возбудителей), бронховаксон.
56
|
Схема 6. Алгоритм формирования базисной бронходилатирующей терапии хронического бронхита |
Назначают физиотерапевтическое лечение: диатермию, электрофорез хлорида кальция, кварц на область грудной клетки, массаж грудной клетки и занятия дыхательной гимнастикой.
Вне периода обострения при бронхите легкого течения ликвидируют очаги инфекции (тонзиллэктомия и пр.); начинают проводить закаливание организма. Занятия ЛФК (дыхательная гимнастика) проводятся постоянно.
При бронхите средней тяжести и тяжелом наряду с противорецидив-ным и санаторно-курортным лечением (Южный берег Крыма, сухая степная полоса) многие больные вынуждены постоянно получать поддерживающее медикаментозное лечение. В среднетяжелых случаях течения ХБ обязательны постоянные занятия дыхательной гимнастикой.
Поддерживающая терапия направлена на улучшение проходимости бронхов, снижение легочной гипертензии и борьбу с правожелудочковой недостаточностью. Назначают те же препараты, что и в период обострения, только в меньших дозах, курсами.
Прогноз. Прогноз в отношении полного выздоровления неблагоприятен. Наименее благоприятен прогноз при обструктивных ХБ и ХБ с преимущественным поражением дистальных отделов бронхов, которое быстро приводит к развитию легочной недостаточности и формированию легочного сердца. Наиболее благоприятный прогноз при поверхностном (катаральном) ХБ без обструкции.
Профилактика. К мероприятиям первичной профилактики относятся запрещение курения в учреждениях и на предприятиях, оздоровление внешней среды, запрещение работы в загрязненной (запыленной и загазованной) атмосфере, постоянная профилактика ОРЗ, лечение патологии носоглотки и др.
Мероприятиями вторичной профилактики являются все действия, направленные на предотвращение развития обострений заболевания.
57
БРОНХИАЛЬНАЯ АСТМА
Бронхиальная астма (БА) — «хроническое заболевание, основой которого является воспалительный процесс в дыхательных путях с участием разнообразных клеточных элементов, включая тучные клетки, эозинофилы и Т-лимфоциты. У предрасположенных лиц этот процесс приводит к развитию генерализованной бронхиальной обструкции разной степени выраженности, полностью или частично обратимой спонтанно или под влиянием лечения. Воспалительный процесс вызывает также содружественное усиление ответа дыхательных путей в виде бронхиальной обструкции на различные внешние и внутренние стимулы» (определение экспертов ВОЗ, 1993).
Появление этого определения Б А стало возможным в связи с тем, что за последние 10 лет существенно изменилось представление о Б А, ее этиологии, патогенезе, клинике, лечении и профилактике. Таким образом, в' основе БА (независимо от степени ее тяжести) лежит хронический неинфекционный воспалительный процесс в дыхательных путях. Гиперактивность бронхов, изменяющаяся со временем бронхиальная обструкция и тесно связанные с ними клинические симптомы БА являются следствием персистирующего воспаления в бронхах.
Этиология. За последние 30 — 40 лет БА стала очень распространенным заболеванием и занимает видное место в общей структуре заболеваемости. Распространенность Б А колеблется от 3 до 8 %.
В возникновении БА имеет значение наследственная предрасположенность. Выявлена связь некоторых антигенов гистосовместимости (HLA) с тяжестью течения БА; нарастание тяжести заболевания особенно часто отмечается у носителей антигенов А2, В7, В12, В13, В27, В35, DR2, DR5 и их комбинации.
В развитии болезни играют роль внутренние и внешние факторы. Внутренние факторы — это биологические дефекты иммунной, эндокринной систем, вегетативной нервной системы, чувствительности и реактивности бронхов, мукоцилиарного клиренса, эндотелия сосудов легких, системы быстрого реагирования (тучные клетки и др.), метаболизма арахидоновой кислоты и т. д.
Внешние факторы, способствующие клинической реализации биологических дефектов, включают: 1) аллергены (пыльцевые, пылевые, пищевые, лекарственные, производственные, аллергены клещей, насекомых, животных и пр.); 2) инфекцию (вирусы, грибы; некоторые виды бактерий); 3) механические и химические раздражители (металлическая, древесная, силикатная, хлопковая пыль; пары кислот, щелочей; дымы и пр.); 4) метеорологические и физико-химические факторы (изменение температуры и влажности воздуха, колебания барометрического давления, магнитного поля земли, физические усилия и пр.); 5) стрессовые нервно-психические воздействия и физическую нагрузку; 6) фармакологические воздействия (р-адреноблокаторы, нестероидные противовоспалительные препараты и т. д.).
Инфекционные агенты, помимо их аллергизирующего действия, могут играть также иную роль: а) снижать порог чувствительности организма к неинфекционным (атопическим) аллергенам, повышать проницаемость для них слизистой оболочки органов дыхания; б) формировать неиммунологическим путем изменение реактивности клеток-мишеней (туч-
58
ные клетки, базофилы, моноциты и др.) и эффекторных систем. Известно, что некоторые вирусы и бактерии оказывают р-адреноблокирующее действие и способны воздействовать на эфферентные зоны вагусного бронхоконстриктивного механизма.
Как правило, при Б А у одного и того же больного можно заподозрить или выявить сочетание нескольких этиологических факторов.
Чем продолжительнее течение болезни, тем большее значение приобретают различные неспецифические раздражения и психогенные факторы. Первоначально вызвавший бронхиальную астму аллерген может со временем утратить свое значение, исчезнув из зоны окружения больного, а обострения болезни обусловливаются иными причинами.
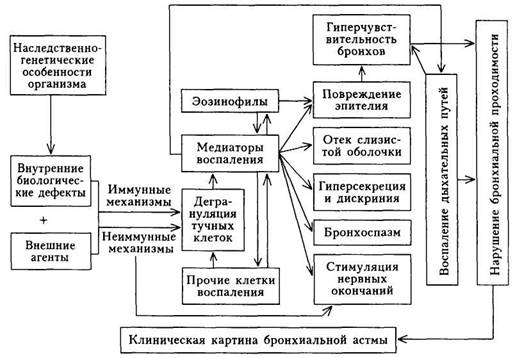
Патогенез. Центральным звеном патогенеза Б А является неинфекционный воспалительный процесс в бронхах, который вызывается воздействием различных воспалительных клеток и выделяемых ими биологически активных веществ — медиаторов. В свою очередь воспаление бронхов ведет к развитию их гиперчувствительности и гиперреактивности, предрасполагая таким образом бронхиальное дерево к сужению в ответ на различные стимулы (схема 7).
В большинстве случаев Б А является аллергической болезнью, поэтому главным механизмом формирования патологического процесса является иммунный. У значительной части больных БА нарушения иммуноком-петентной системы протекают по I, III и IV типам реакций гиперчувствительности (по классификации, разработанной R. Coombs и P. Gell). Развитие реакций II (цитотоксического) типа при БА пока не описано.
|
59 |
Схема 7. Патогенез бронхиальной астмы
Чаще других главную роль играют механизмы гиперчувствительности I (анафилактического, или атопического) типа. К этому типу аллергии относят немедленные реакции, развивающиеся вследствие взаимодействия аллергена (антигена) со специфическим IgE. Реакция антигена с IgE происходит преимущественно на поверхности субмукозных тучных клеток дыхательных путей и циркулирующих в крови базофилов. В результате наблюдается их дегрануляция с высвобождением биологически активных молекул, среди которых преобладают медиаторы воспаления. Уже через несколько секунд после реакции клетки секретируют ранее синтезированные вазоактивные амины: гистамин, серотонин. Более отдаленным последствием активизации тучных клеток является запуск продукции метаболитов арахи-доновой кислоты (простагландинов, лейкотриенов), тромбоксанов и цито-кинов, которые также секретируются тучными клетками и участвуют в поддержании воспалительной реакции в тканях (интерлейкины 3, 4, 5, 8; ней-трофильный хемотаксический фактор, фактор агрегации тромбоцитов, грану лоцитарно-макрофагальный колониестимулирующий фактор и др.).
Секретируемые тучными клетками медиаторы и цитокины вызывают интенсивный приток эозинофилов и других клеток воспаления (грануло-цитов, моноцитов, Т-лимфоцитов) к месту проникновения аллергена. Через 6— 12 ч развивается поздняя стадия аллергической реакции, при которой доминирует клеточная инфильтрация. Эозинофил рассматривается как «ключевая» клетка в повреждении эпителия дыхательных путей вследствие продукции и секреции им эозинофильного катионного белка, а также выделения фактора активации тромбоцитов и так называемого «большого основного протеина». В свою очередь повреждение эпителия бронхов эозинофильным «большим основным протеином» приводит к развитию неспецифической гиперреактивности и гиперчувствительности.
Медиаторы тучных клеток привлекают в зону воспаления нейтрофилы и способствуют выделению ими активных форм кислорода. Активированные нейтрофилы в свою очередь стимулируют дегрануляцию тучных клеток, что замыкает «порочный круг».
В развитии хронического воспаления в бронхах велика роль лимфоцитов, выделяющих интерлейкины с последующей активацией тучных клеток и эозинофилов. Кроме того, вещества, обладающие мощным брон-хоспастическим действием и потенцирующие воспаление, вырабатываются макрофагами и моноцитами.
Под влиянием всех вышеописанных изменений повышается проницаемость микроциркуляторного русла, развиваются отек, гипер - и дискриния, бронхоспазм и прочие проявления неинфекционного воспаления дыхательных путей. Клинически это выражается острым нарушением проходимости бронхов и развитием приступа Б А.
В возникновении реакции I типа большая роль отводится избыточному синтезу реагинов, дефициту секреторного IgA и, главное, снижению Т-супрессорной функции лимфоцитов.
Реакция III типа (иммунокомплексный тип, или феномен Артюса) происходит в зоне избытка антигена с участием преципитирующих антител. Реакция развивается под воздействием экзоаллергенов (микроорганизмы, ферменты, пыль, антибиотики и др.) и эндоаллергенов [инфекционное и(или) аллергическое воспаление, различные раздражители и другие факторы могут приводить к денатурации белков бронхиол и альвеол с последующим формированием эндоаллергенов —аутоаллергенов].
60
При иммунокомплексных реакциях III типа образуются антитела, принадлежащие преимущественно к иммуноглобулинам классов G и М. Повреждающее действие образованного комплекса антиген — антитело реализуется главным образом через активацию комплемента, освобождение лизосомных ферментов. Происходят повреждение базальных мембран, спазм гладких мышц бронхов, расширение сосудов, повышается проницаемость микроциркуляторного русла.
Тип IV (клеточный), при котором повреждающее действие оказывают сенсибилизированные лимфоциты, относится к гиперчувствительности замедленного типа (ГЗТ).
Основными медиаторами аллергической реакции IV типа являются интерлейкины — лимфокины (действуют на макрофаги, эпителиальные клетки) и лизосомные ферменты; возможна роль активации кининовой системы. Под влиянием этих веществ происходят развитие отека, набухание слизистой оболочки, бронхоспазм, гиперпродукция вязкого бронхиального секрета. Выделяющиеся лимфоцитами интерлейкины способствуют также привлечению к месту аллергической реакции других клеток воспаления с развитием персистирующей воспалительной реакции. Все это приводит к длительному нарушению бронхиальной проходимости.
В патогенезе БА определенная роль принадлежит местной «поломке» иммунной защиты: отмечается уменьшение секреторного IgA, нарушается система фагоцитоза, которая в органах дыхания обеспечивается в основном альвеолярными макрофагами. При нарушении их функции (воздействие лимфокинов и др.) резко снижается противовирусная защита организма (вследствие снижения продукции интерферона). Воспаление приобретает персистирующий характер.
Неиммунные механизмы. Известно, что, помимо антиген-зависимой дегрануляции тучных клеток, существует большое количество неспецифических факторов (токсины, ферменты, лекарства, различные макромолекулы и др.), вызывающих дегрануляцию тучных клеток неиммунным путем. Различные физические, механические и химические раздражители (например, дым, двуокись серы, пыль, холодный воздух и др.), инфекционные агенты (без сенсибилизации и аллергизации) провоцируют рефлекторный бронхоспазм путем стимуляции рецепторов в дыхательных путях. Ранее считалось, что такая реакция осуществляется путем повышенной активности парасимпатической нервной системы. Однако в настоящее время этот механизм не считается основным. Обнаружена распространенная сеть нервных волокон неадренергической нехолинергичес-кой регуляции бронхов, содержащих мощные нейропептиды (нейрокин А и В, субстанцию Р, вазоактивный интенстинальный пептид и др.), которые имеют отношение к развитию большинства признаков обострения бронхиальной астмы.
Предполагают участие глюкокортикоидной недостаточности, дизова-риальных расстройств (гиперэстрогенемия и гипопрогестеронемия) и нервно-психических нарушений в формировании «нестабильного метаболизма» тучных клеток.
Недостаточность глюкокортикостероидов способствует развитию гиперреактивности тучных клеток, снижению синтеза катехоламинов, активации простагландинов F2a и др., а также нарушению иммунокомпетент-ной системы (комплексное участие в патогенезе БА и иммунологических и неиммунологических механизмов).
61
Гиперэстрогенемия и гипопрогестеронемия воздействуют главным образом на а - и р-адренорецепторы, повышая активность ос-рецепторов и снижая активность р-рецепторов.
При нарушении бронхиальной проходимости, обусловленной любыми другими механизмами, также отмечается адренергический дисбаланс, выражающийся в преобладании системы гуанилатциклазы над системой аде-нилатциклазы. Кроме того, изменяется содержание внутриклеточного фермента фосфодиэстеразы, усиливается поступление ионов кальция в клетку, нарушается обмен простагландинов.
Преобладание того или иного механизма в патогенезе БА позволяет выделить ее различные патогенетические варианты [, 1982; , 1985].
Классификация. В последние годы в нашей стране с учетом принятого определения БА используется классификация, предложенная Г. Б. Федосеевым (1982). Она не отменяет классификацию, разработанную и (1969), но развивает ее с учетом результатов новых исследований.
Классификация бронхиальной астмы [по , 1982]
• Этапы развития Б А: 1) состояние предастмы, 2) клинически офор
мленная БА.
К предастме относят все состояния, представляющие угрозу возникновения БА (острый и хронический бронхит, а также острая и хроническая пневмония с элементами бронхоспазма, в сочетании с вазомоторным ринитом, крапивницей и другими состояниями, при которых выявляются эозинофилия крови и увеличенное содержание эозинофилов в мокроте). После первого приступа или сразу возникшего астматического статуса БА считается клинически оформленной.
• Формы Б А: 1) иммунологическая, 2) неиммунологическая (в фор
мулировку клинического диагноза на включается).
• Патогенетические механизмы (клинико-патогенетические вариан
ты) БА: 1) атопический, 2) инфекционнозависимый, 3) аутоиммун
ный, 4) дисгормональный, 5) нервно-психический дисбаланс, 6) ад
ренергический дисбаланс, 7) первично измененная реактивность
бронхов.
Разделение БА по патогенетическим механизмам и выделение основного из них представляют трудную и часто неразрешимую задачу, особенно для врачей поликлиник. Однако во всех случаях такая попытка оправдана, так как каждый из патогенетических механизмов предполагает определенный, свойственный только ему характер лекарственной терапии.
У одного больного возможно сочетание нескольких клинико-патогене-тических вариантов. В такой ситуации необходимо на момент обследования выделить основной для данного больного, так как это важно для проведения адекватной терапии. В процессе длительного течения Б А возможна смена патогенетического механизма.
• Тяжесть течения БА: 1) легкое течение, 2) течение средней тяжес
ти, 3) тяжелое течение.
62
При легком течении Б А обострения не длительные, возникают 2 — 3 раза в год. Приступы удушья купируются, как правило, приемом различных бронхолитических препаратов внутрь. В межприступный период признаки бронхоспазма, как правило, не выявляются.
Среднетяжелое течение характеризуется более частыми обострениями 3 — 4 раза в год. Приступы удушья протекают тяжелее и купируются инъекциями лекарственных препаратов.
При тяжелом течении Б А обострения возникают часто (5 раз и более раз в год), отличаются длительностью. Приступы тяжелые, нередко переходят в астматическое состояние.
В ряде случаев разделение Б А по тяжести течения бывает условным. Так, при легком течении Б А больной может погибнуть от внезапно развившегося астматического статуса. В то же время возможна «спонтанная» ремиссия при довольно тяжелом течении болезни.
• Фазы течения Б А: 1) обострение, 2) стихающее обострение, 3) ре
миссия.
Фаза обострения характеризуется наличием выраженных признаков заболевания, прежде всего повторно возникающих приступов Б А или астматического состояния.
В фазе стихающего обострения приступы становятся более редкими и нетяжелыми. Физикальные и функциональные признаки заболевания выражены меньше, чем в фазу обострения.
В фазу ремиссии исчезают типичные проявления БА: приступы удушья не возникают; полностью или частично восстанавливается проходимость бронхов.
• Осложнения: 1) легочные: эмфизема легких, легочная недостаточ
ность, ателектаз, пневмоторакс, астматический статус и пр.; 2) вне-
легочные: легочное сердце (компенсированное и декомпенсирован-
ное с развитием правосердечной недостаточности), дистрофия мио
карда и др.
Примечания к классификации:
1. Первично измененная реактивность бронхов может быть врожденной и при
обретенной, проявляется приступами удушья при физической нагрузке, воздействии
холодного воздуха, медикаментов, инфекции и др.
2. При инфекционнозависимом варианте БА необходимо указывать характер
инфекционной зависимости: стимуляция атопической реакции; инфекционная ал
лергия; формирование первично измененной реактивности бронхов. В тех случаях,
когда инфекция является аллергеном, Б А определяется как инфекционно-аллерги-
ческая.
Предлагаемая классификация, как и все остальные, не лишена недостатков, но более прогрессивна по сравнению с существующей. Настоящая классификация еще не утверждена, но позволяет более эффективно проводить патогенетическую терапию больных Б А.
Экспертами ВОЗ (1993) даны новые критерии тяжести БА, определяемой выраженностью клинических симптомов, объемом форсированного выдоха за первую секунду (ОФВь л/с) и пиковой скоростью выдоха (ПСВ, л/мин) — наиболее значимыми показателями выраженности обструкции дыхательных путей. Оценка по этим степеням тяжести Б А по-
63
зволяет осуществить так называемый ступенчатый подход к лечению больных: объем терапии должен повышаться при увеличении степени тяжести болезни.
Классификация БА, основанная на степени тяжести, наиболее важна, когда нужно принять решение о выборе терапии. Кроме того, предложение экспертов ВОЗ классифицировать БА по степени тяжести базируется на том, что нередко другие рубрики вышеприведенной классификации невозможно с достоверностью определить у всех больных.
Классификация бронхиальной астмы по тяжести течения
• Легкое эпизодическое (интермиттирующее).
Кратковременные симптомы реже 1 раза в неделю.
Короткие обострения (от нескольких часов до нескольких дней).
Ночные симптомы < 2 раз в месяц.
Отсутствие симптомов и нормальная функция внешнего дыхания
между обострениями.
ПСВ и ОФВ1: 2: 80 % от должных.
Разброс показателей < 20 %.
• Легкое персистирующее.
Симптомы от 1 раза в неделю до 1 раза в день.
Обострения могут снижать физическую активность и нарушать
сон.
Ночные симптомы > 2 раз в месяц.
ПСВ и OOBi: £ 80 % от должных.
Разброс показателей 20 — 30 %.
• Среднетяжелое.
Ежедневные симптомы.
Обострения могут приводить к ограничению физической активности и сна.
Ночные симптомы > 1 раза в неделю. ПСВ и ОФВ1 : 60-80 % от должных. Суточный разброс показателей > 30 %.
• Тяжелое.
Постоянное наличие симптомов.
Частые ночные симптомы.
Ограничение физической активности из-за симптомов астмы.
ПСВ и ОФВ1 : <; 60 % от должных.
Суточный разброс показателей > 30 %.
Клиническая картина. Наиболее характерный признак БА — наличие приступов удушья. Однако клинический диагноз БА может быть поставлен с учетом оценки результатов всех трех этапов диагностического поиска, так как удушье встречается как симптом и при других заболеваниях. В связи с этим возникает на каждом из трех этапов необходимость ее дифференциации от заболеваний, составной частью которых является бронхоспастический синдром с развитием приступов удушья.
На I этапе диагностического поиска устанавливают: а) наличие приступов удушья, их особенности и связь с определенными факторами; б) аллергический анамнез (наследственную предрасположенность, непереносимость пищевых и лекарственных веществ); в) наличие предшествую-
64
щих заболеваний легких; г) влияние метеорологических факторов, физических усилий, дизовариальных расстройств и других причин на возникновение приступов удушья; д) эффективность проводимой ранее терапии; е) течение болезни, появление осложнений.
Больные жалуются на приступы удушья (затрудненное дыхание, преимущественно на выдохе), одышку и кашель. Характер кашля может быть разнообразным: чаще кашель сухой, надсадный, приступообразный или с выделением вязкой, трудноотделяемой мокроты. При развитии легочной недостаточности одышка беспокоит и в межприсгупный период. Повышение температуры тела может свидетельствовать об активности бронхоле-гочной инфекции. Затрудненное носовое дыхание, как правило, служит проявлением аллергической риносинусопатии (вазомоторный ринит, полипоз) — частого спутника или предшественника Б А (предастма). При расспросе больного необходимо уточнить частоту возникновения симптомов Б А в неделю, обратив особое внимание на ночные симптомы. Эти данные особенно важны для оценки тяжести течения болезни на момент обследования больного.
Данные анамнеза помогают установить связь развития приступов с воздействием определенных аллергенов и других факторов. Наиболее частой причиной обострения и развития БА является инфекция дыхательных путей; особенно велика ее роль в обострении болезни. Из анамнеза узнают о влиянии физического усилия (быстрая ходьба, смех и пр.), изменений метеорологических факторов (холод, повышенная влажность и др.), дизовариальных расстройств на возникновение приступов удушья. Знакомство с условиями труда помогает обнаружить профессиональную астму.
Изучение аллергологического анамнеза способствует диагностике ато-пического варианта БА. В подобных случаях можно получить сведения о поллинозе: обострения болезни имеют сезонный характер (чаще весной и летом), сопровождаются ринитом, конъюнктивитом. У таких больных бывают крапивница, отек Квинке; выявляется непереносимость пищевых продуктов, ряда лекарственных веществ; отмечается наследственная предрасположенность к аллергическим заболеваниям.
Ориентируясь на данные анамнеза, можно предположительно, а в ряде случаев и с уверенностью высказаться о так называемой аспириновой астме. Эти больные не страдают наследственной формой аллергических заболеваний. Их беспокоит нарушенное носовое дыхание (полипозные разрастания). Наиболее характерный симптом у таких больных — непереносимость нестероидных противовоспалительных препаратов (ацетилсалициловая кислота, индометацин и пр.), вызывающих астматические приступы. На этом этапе уже можно предположить простагландиновый механизм БА.
Указание в анамнезе на прием кортикостероидных препаратов свидетельствует о тяжести болезни, а эффективность приема — об иммунной форме Б А или кортикостероидозависимом ее варианте. Отсутствие эффекта от приема кортикоидных препаратов, особенно у больных с тяжелым течением Б А, делает предположение об аллергическом генезе Б А менее достоверным и практически исключает наличие у больного глюкокортикоид-ной недостаточности. Глюкокортикоиды неэффективны также при астме физического усилия.
Данные о развитии в прошлом астматического статуса свидетельствуют о тяжести течения заболевания и указывают на необходимость проведения терапии кортикостероидами. Наличие предшествующих заболеваний
65
органов дыхания (ХБ, ХП) предопределяет обычно тяжесть течения БА, отсутствие «светлых» промежутков.
Б А может протекать монотонно, с постоянно нарушенным дыханием и потребностью принимать ежедневно противоастматические средства.
Другой тип течения БА характеризуется периодическими обострениями с заметно усиливающимися признаками бронхиальной обструкции и ремиссиями, когда нарушения бронхиальной проходимости резко уменьшаются или исчезают. Такое течение БА наиболее характерно для атопи-ческого варианта заболевания.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 |