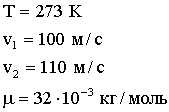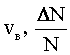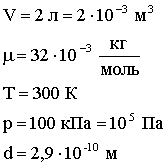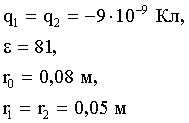где ![]() - парциальные давления.
- парциальные давления.
Из уравнения Менделеева - Клапейрона до соединения сосудов получим:
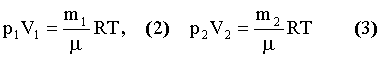
где m1 и m2 - масса газа в первом и во втором сосудах; μ - молярная масса; R - газовая постоянная.
Аналогично для парциальных давлений (после соединения):
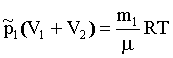 (4)
(4)
и
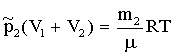 (5)
(5)
Так как T = const и μ = const, то правые части уравнений (2) и (4), а также уравнений (3) и (5) равны. Тогда:
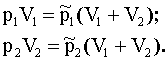
Отсюда:
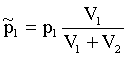 (6)
(6)
и
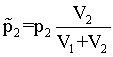 (7)
(7)
Подставляя (6) и (7) в (1), получим:
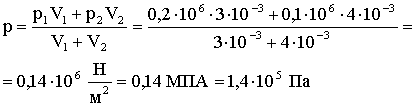
Ответ:
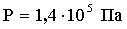
Задача 2. Какая часть молекул кислорода при температуре Т = 273 К обладает скоростями, лежащими в интервале от v1 = 100 м/с до v2 = 110 м/c? Чему равна наиболее вероятная скорость движения молекул?
Дано: |
|
Найти: |
|
Решение: Найдем наиболее вероятную скорость молекул:
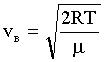
где R - газовая постоянная, μ - молярная масса.
Подставим численные значения:
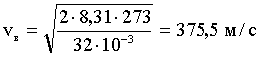
Интервал скоростей:
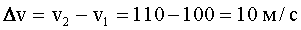
Это много меньше v1 и v2. Поэтому можно использовать приближенную формулу:
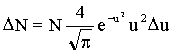 (1)
(1)
где ΔN - число частиц, обладающих скоростями в интервале от v1 до v2 , N - полное число частиц,
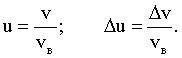
Относительное число частиц или доля молекул, обладающих скоростями в заданном интервале, найдем из формулы (1) при 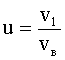 :
:
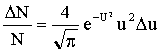 (2)
(2)
Вычислим:
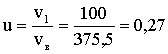 ,
,
подставим в (2) и учтем, что
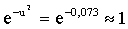
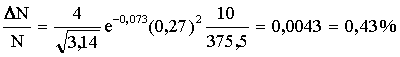
Ответ:
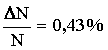 ;
;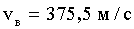
Задача 3. Определить среднюю длину свободного пробега молекул и число соударений за 1 с, происходящих между всеми молекулами кислорода, находящегося в сосуде емкостью 2 л при температуре 27оС и давлении 100 кПа.
Дано: |
|
Найти: | < λ >, z |
Решение: Средняя длина свободного пробега молекул вычисляется по формуле:
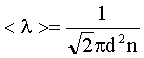 (1)
(1)
где d - эффективный диаметр, n - концентрация, т. е. число молекул в единице объема.
Давление связано с концентрацией:
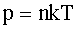
где k - постоянная Больцмана.
Выразим n:
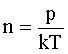 (2)
(2)
Подставим (2) в (1) и получим:
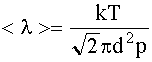 (3)
(3)
Число соударений, происходящих между всеми молекулами за 1 с равно:
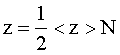 (4)
(4)
где N - число молекул в сосуде объемом V, < z > - среднее число соударений одной молекулы за 1 с.
Число молекул в сосуде равно:
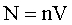 (5)
(5)
Среднее число соударений молекулы за 1 с:
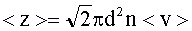 (6)
(6)
где < v > - средняя арифметическая скорость молекулы.
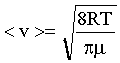 (7)
(7)
Подставим в (4) выражения (5), (6), (7):
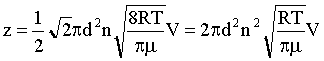
Учтем (2):
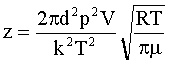
Подставим численные значения:
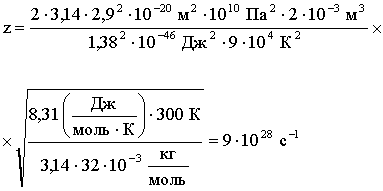
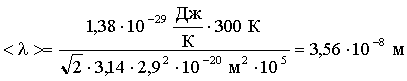
Ответ: z = 9·1028 с-1;< λ > = 3,56·10-8 м.
Задача 4. Горячая вода некоторой массы отдает теплоту холодной воде такой же массы и температуры их становятся одинаковыми. Показать, что энтропия при этом увеличивается.
Решение: Обозначим температуру горячей воды Т1, холодной Т2, а температуру смеси Q. Определим температуру смеси, исходя из уравнения теплового баланса.
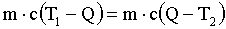
где с - удельная теплоемкость вещества, m - масса.
Тогда:
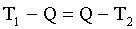
Отсюда температура смеси равна:
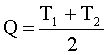 (1)
(1)
Изменение энтропии, происходящее при охлаждении горячей воды:
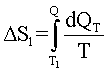
Элементарное количество теплоты равно:
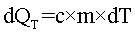
Тогда:
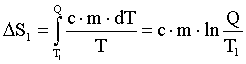
Изменение энтропии, происходящее при нагревании холодной воды:
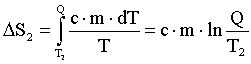
Изменение энтропии системы равно:
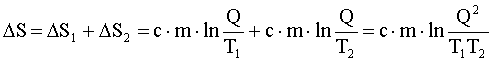
С учетом (1) получим:
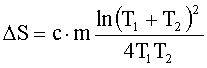
Так как
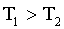 , то
, то
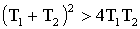 ,
,
следовательно:
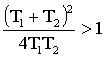
и
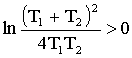 .
.
Тогда ![]() , т. е. энтропия возрастает.
, т. е. энтропия возрастает.
4 Примеры решения задач по электричеству и магнетизму
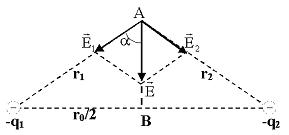
Задача 1. Два равных отрицательных заряда по 9 нКл находятся в воде на расстоянии 8 см друг от друга. Определить напряженность и потенциал поля в точке, расположенной на расстоянии 5 см от зарядов.
Дано: |
|
Рис.3 |
Найти: | Е,φ |
Решение: Напряженность поля в точке А (рис.3) по принципу суперпозиции равна:
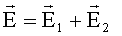
По теореме косинусов:
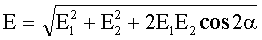
Напряженность поля точечного заряда:
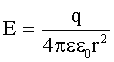
По условию 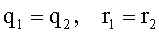 , следовательно,
, следовательно,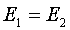 . Тогда:
. Тогда:

Но 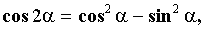 поэтому:
поэтому:
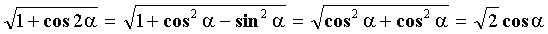
и результирующая напряженность равна:
![]()
Обозначим АВ = h. Тогда 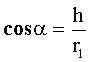
По теореме Пифагора:
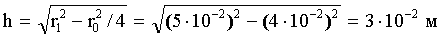
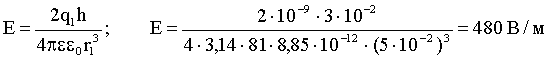

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 |