Глава 3. Хронический гепатит вирусной этиологии
Клиническими проявлениями перехода ОВГ в хроническую форму могут быть стойкая астенизация — недомогание, общая слабость, снижение трудоспособности; диспепсические нарушения—снижение аппетита, тошнота, непереносимость жира, алкоголя и табака, нарушения стула, метеоризм, боль или чувство тяжести в правом подреберье или эпигастральной области, стойкое похудание; часто умеренно увеличенная, слегка болезненная, с гладкой поверхностью печень. Иногда хроническое вирусоносительство или хронический гепатит, обычно ХПГ или ХАГ с умеренной активностью, находят у реконвалесцентов с постгепатитной неконъюгированной гипербилирубинемией. Основную трудность представляет дифференциальный диагноз хронического гепатита с развившимися после ОВГ синдромами постгепатитной астении, диспепсии и дискинезией желчевыво дящих путей, т. е. функциональными постгепатитными расстройствами при интактной печени (так называемый постгепа титный синдром авторов прошлого). Поскольку субъективные жалобы у обоих категорий больных могут быть одинаковыми, решающее значение имеет амбулаторное наблюдение в течение 1 года и выявление объективных клинико-биохимических и серологических признаков хронического гепатита.
Значительно проще диагностировать хронический вирусный гепатит при развитии холестатической или тяжелой некроти зирующей его формы со стойкой или перемежающейся желтухой и другими клинико-биохимическими признаками печеночной недостаточности.
При хроническом гепатите HBsAg находят в среднем у 40% больных [Маскау I. R., 1975]. В нашей клинике из 8000 больных хроническими заболеваниямия печени HBsAg методом встречного иммунофореза и двойной иммунодиффузии был обнаружен в сыворотке крови у 424 (5,3%) больных. При этом более чем у 90% больных с положительным HBsAg был диагностирован ХАГ или постгепатитный цирроз печени. Наиболее часто HBsAg выявлялся у мужчин молодого и среднего возраста. В анамнезе у этих больных нередко отмечались ОВГ, гемотрансфузии и оперативные вмешательства. У большинства этих больных методом непрямой иммунофлюоресценциии было выявлено специфическое свечение цитоплазмы гепатоцитов, свидетельствовавшее о наличии HBsAg в клетках печени. HBeAg обнаружен у 35 из 100 больных ХАГ и циррозом печени [Логинов А. С. и др., 1983]. HBsAg определяется в сыворотке крови у 40% больных ХНГ [Mezey Е., 1982].
По аналогии с ОВГ возможны латентные субклинические и редко тяжелые некротизирующие формы хронического вирусного гепатита. Чаще всего наблюдают латентные и субклинические формы, при которых нередко отсутствует корреляция между клинической картиной и морфологическими изменениями в печени, т. е. при одной и той же клинической картине в пунк тате печени наблюдают изменения, свойственные как благоприятно текущим, редко прогрессирующим формам ХПГ, так и ХАГ различной степени активности и даже начальным стадиям цирроза печени [ и др., 1981]. Компенса торные возможности печени настолько велики, что даже при значительном поражении органа клинические проявления печеночной недостаточности могут отсутствовать. Вместе с тем необходимо подчеркнуть, что у одного и того же больного возможна спонтанная эволюция легких, малоактивных форм хронического вирусного гепатита в формы с выраженной активностью (реактивация) и, наоборот, развитие спонтанной ремиссии, т. е. эволюция активной фазы в малоактивную.
Среди субъективных нарушений при субклинической форме хронического гепатита вирусной этиологии доминируют жалобы на слабость и быструю утомляемость. Возможны также диспепсические нарушения, болевой холецистоподобный синдром, артралгия. Среди больных несколько преобладают мужчины, однако хронический вирусный гепатит у женщин отнюдь не является редкостью. ОВГ-ни А ни В и его последствия наблюдаются у мужчин и у женщин одинаково часто. Заболевание длится от 1 года до 20 лет и более и характеризуется чрезвычайной вариабельностью клинического течения, сменой периодов ремиссии, которые могут продолжаться на протяжении ряда лет и заканчиваться выздоровлением, и периодов реакти вации с исходом в цирроз печени.
Важно отметить, что на стадии ремиссии хронического гепатита возможна сероконверсия и исчезновение из крови маркеров вируса В. К серонегативным формам относятся и хронические вирусные гепатиты типа ни А ни В. Вероятно, этим объясняется отсутствие HBs-антигенемии у многих больных с типичным для хронического вирусного гепатита клиническим течением заболевания. Можно согласиться с J. Dienstag (1978), полагающим, что у некоторых из этих больных с отрицательным HBsAg специфическая противовирусная терапия могла бы оказаться более эффективной, чем противовоспалительное лечение. Ряд авторов проводят резкую грань между ХАГ с положительным HBsAg и ХАГ с отрицательным HBsAg, подразумевая под последним резко отличную по этиологии и патогенезу от вирусных гепатитов форму ХАГ (аутоиммунный гепатит, люпоидный гепатит). Такое разграничение не всегда обосновано, так как нередко хронический гепатит и цирроз печени безусловно вирусной этиологии являются серонегатив ными.
Таким образом, вялое, латентное или субклиническое течение хронических вирусных гепатитов у некоторых больных может быть весьма коварным. В частности, стойкая клиническая ремиссия спустя много лет может перейти в стадию реактива ции, иногда по типу желтушного некротизирующего гепатита с внезапным быстрым ухудшением функций печени, с печеночной энцефалопатией или с быстрым развитием цирроза печени, который у 1/3 больных внезапно проявляется осложненной портальной гипертензией (асцит, желудочно-кишечное кровотечение, гиперспленизм, энцефалопатия). Больные обычно заявляют, что ранее они никогда не переносили «желтухи». У них, по-видимому, имела место безжелтушная, латентная форма ОВГ. Не более Уз больных указывают на давно перенесенный острый гепатит, не оставивший никаких последствий.
У бессимптомных носителей вирусной инфекции острая фаза инфекции (фаза ОВГ) часто начинается с резкой активации аминотрансфераз крови (в 10—20 раз выше нормы) без каких-либо других субъективных или объективных симптомов с последующим снижением активности до субнормальных или нормальных уровней.
Важнейшей причиной реактивации латентно текущей вирусной инфекции является изменение иммунного статуса больного. Тяжелые обострения возможны, например, в различные сроки после длительной иммунодепрессивной терапии или химиотерапии по поводу онкологических заболеваний, после кровотечений, под влиянием дополнительных токсических воздействий (инфекции, медикаменты).
У больной 50 лет через несколько месяцев после завершения массивной рентгенотерапии по поводу рака шейки матки III стадии, приведшей к полному излечению от опухоли, внезапно развилась картина тяжелой холестати чески-цитолитической желтухи с болевыми приступами в правом подреберье, подъемом активности аминотрансфераз крови до 12,5—15 мкмоль/л и полным отсутствием эффекта от высоких доз преднизолона. Больная скончалась вскоре после диагностической лапаротомии. На вскрытии найден подострый некротизирующий гепатит на фоне цирроза печени и выраженного внутрипе ченочного холестаза. Размеры печени были нерезко увеличены, спленомегалия отсутствовала.
Проследить эволюцию ОВГ в хронические формы вирусной инфекции удается не более чем у /з больных. У остальных больных хронический гепатит вирусной этиологии, а нередко и вирусный цирроз печени возникают как бы спонтанно вследствие длительной бессимптомной эволюции оставшегося незамеченным ОВГ. Проявлением такой инаппарантной атаки ОВГ, соотношение которой с симптоматическими формами составляет от 1 : 1 до 10—30 : 1 [Bernstein L., 1980; Wright R., 1980;
Mezey R., 1982], может быть фактически любое преходящее недомогание, гриппоподобное состояние или кишечная диспепсия. Способом диагностики поражения печени при таких со стояниях могло бы быть определение уровня АлАТ крови, активность которой даже при безжелтушных, клинически немых формах ОВГ повышается в десятки раз по сравнению с нормой. Проведение этой несложной пробы на амбулаторном уровне должно, по-видимому, стать правилом у всех больных с синдромами астении, диспепсии, артралгии, холецистопатии или неясной лихорадки.
Первое обращение к врачу [больных хроническим вирусным гепатитом обычно обусловлено астенией, снижением работоспособности и нередко небольшой желтушностью склер и кожи [, , 1973]. Возможен также диспепсический синдром (тошнота, рвота, горечь во рту, метеоризм, периодически понос или запор). При активных, быстро прогрессирующих формах хронического гепатита эти симптомы обычно выражены в большей степени, чем при формах с умеренной активностью, и могут сопровождаться кровотечениями из носа и десен, лихорадкой или субфебрилитетом, зудом кожи, упадком питания, более выраженной желтухой с осветле нием кала и потемнением мочи [, 1974]. Необходимо подчеркнуть, что ни один из перечисленных симптомов не является обязательным для хронического вирусного гепатита. Так; нередко встречаются больные, у которых единственным проявлением гепатита служит выраженная астения или боль в правом подреберье либо упорная тошнота или артрал гия. Часто наблюдается астеновегетативный синдром: боль в области сердца, не связанная с физической нагрузкой, головная боль, потливость, головокружение, психоэмоциональная лабильность. В 20% случаев субъективных жалоб не бывает даже на стадии постгепатитного (вирусного) цирроза печени, а гепатомегалия обнаруживается при врачебном осмотре по поводу другого заболевания (например, язвенной или гипертонической болезни).
Несомненное диагностическое значение может иметь тщательно собранный эпидемиологический анамнез, который, помимо сведений о перенесенном в прошлом ОВГ или о контактах с больными ОВГ, включает данные о факторах риска. К ним относят указания на переливания крови, ее компонентов и препаратов, иммунодепрессивную терапию по поводу системных заболеваний, химио - или лучевую терапию по поводу злокачественных новообразований, обширные операции или трансплантацию органов, инъекционную терапию, например, по поводу сахарного диабета, туберкулеза или венерических заболеваний. В группу риска включены врачи и медицинский персонал, соприкасающиеся с кровью или ее препаратами; лица, выезжавшие в эндемические в отношении ОВГ-В районы; больные со сниженным иммунным статусом (страдающие диффузными заболеваниями соединительной ткани — коллагено зами, гемобластозами, болезнью Дауна, хроническими заболеваниями печени другой этиологии), лица, тесно контактировавшие с носителями вирусной инфекции, имеющие обширную татуировку кожи, получавшие иглорефлексотерапию в домашних условиях, родившиеся от матерей-носителей HBsAg и HBeAg; члены замкнутых коллективов (интернаты, тюрьмы и т. д.); лица с низкими гигиеническими навыками или ведущие беспорядочную половую жизнь. Среди больных сахарным диабетом, получающих инсулин, доля инфицированных лиц составляет 4,19—4,9% [Waden-Knecht, Metzner Ch., 1983].
При объективном исследовании единственным симптомом у больных хроническим вирусным гепатитом часто бывает умеренная гепатомегалия: печень увеличена по правой срединно ключичной линии на 2—5 см, нерезко уплотнена, с гладкой по верхностью, часто умеренно чувствительна при пальпации. Селезенка, по нашим данным, пальпируется у 10% больных, т. е. значительно реже, чем при циррозе печени. Общие клинические анализы крови не обнаруживают каких-либо специфических изменений: у 20—30% больных выявляется умеренно повышенная СОЭ, обычно не более чем до 20—25 мм/ч, нередко, особенно у женщин, отмечается свойственная хроническим заболеваниям любой этиологии умеренная анемия с уровнем гемоглобина крови около 100 г/л. Число лейкоцитов периферической крови обычно незначительно превышает нижнюю границу нормы, составляя 3,5—5 • 10°/л. Часто, особенно при активных формах, наблюдается уменьшение числа Т-лимфоци тов циркулирующей крови в пробе на Е-РОК (норма 1300— 1500 клеток на 1 мл, или 60,5%) и увеличение числа В-лим фоцитов в пробе на М-РОК. (норма 257 клеток на 1 мл, или 13—14% от общего числа лимфоцитов), снижение спонтанной миграционной способности (норма 10—14 ед.) и фагоцитарной способности лейкоцитов крови (в норме фагоцитарное число составляет 60±10%, фагоцитарный индекс 10±2 в 1 клетке). Число тромбоцитов, как правило, нормально, но у некоторых больных наблюдается тромбоцитопения, по-видимому, аутоим мунного генеза.
Из биохимических показателей наиболее характерно умеренное повышение (обычно не более чем в 3—5 раз) активности аминотрансфераз крови (уровень АлАТ, как правило, превосходит активность АсАТ). Это часто сочетается с нерезко выраженной дисглобулинемией: уровень у-глобулина крови при этом редко превышает 20 г/л. У многих больных находят повышение показателя тимоловой пробы. У большинства больных наблюдается после ОВГ нарушение элиминации бром сульфалеина или вофавердина из крови [ и др., 1969]. При этом степень задержки коррелирует со степенью активности патологического процесса.
У 20—40% больных, чаще активными формами хронического вирусного гепатита, бывает незначительное повышение концентрации билирубина крови за счет прямой его фракции. Выраженная прямая гипербилирубинемия в сочетании с высокой активностью щелочной фосфатазы крови характерна для редкой, тяжело протекающей холестатической формы хронического вирусного гепатита. Повышение концентрации непрямого билирубина может быть обусловлено сопутствующим синдромом Жильбера (постгепатитная гипербилирубинемия) или нередким при вирусных инфекциях гемолитическим компонентом. Уровень альбумина крови может быть умеренно снижен. При тяжелых некротических обострениях хронического вирусного гепатита, часто протекающих с симптомами выраженного внутрипеченочного холестаза, наряду с резким повышением активности аминотрансфераз крови отмечается гиперферремия. Оба эти симптома не свойственны механической желтухе, при которой активность АсАТ и АлАТ крови редко повышается более чем в 2—3 раза, а уровень сывороточного железа остается нормальным или снижается.
Таким образом, при первом обращении к врачу у больного хроническим вирусным гепатитом наиболее часто отмечаются астенические или/и диспепсические жалобы в сочетании с ге патомегалией и умеренной гипераминотрансфераземией. У некоторых больных печень не увеличивается, но бывает гипер билирубинемия или только болевой холециститоподобный синдром с нарушением функциональных биохимических проб печени либо, наконец, изолированная гипераминотрансферазе мия. Наиболее постоянным при всех клинических вариантах является биохимический синдром умеренно выраженной воспалительной реакции (гипераминотрансфераземия и дисглобули немия), отражающий сравнительно нетяжелое поражение паренхимы печени при вяло текущем хроническом гепатите. Поэтому начальный биохимический скрининг (определение активности АлАТ и АсАТ крови желательно в сочетании с определением белковых фракций сыворотки или хотя бы показателя тимоловой пробы) является обязательным для всех больных с подозрением на хронический гепатит вирусной этиологии. При наличии у больного признаков нарушения билирубинового обмена или холестаза (желтушность склер, осветление кала, потемнение мочи, зуд кожи) необходимо определение концентрации общего и прямого (конъюгированного) билирубина крови и активности щелочной фосфатазы крови.
Диагноз хронического гепатита любой этиологии на основании клинико-биохимических данных всегда является предварительным, предположительным. Так, например, гепатомега лия с умеренным повышением активности АсАТ и АлАТ возможна при жировой дистрофии печени. Окончательный, достоверный диагноз можно поставить только при комплексном обследовании больного в стационарных условиях, как правило, с применением иммунологических, радионуклидных и морфологических (биоптат печени) методов исследования.
У большинства больных хронический вирусный гепатит протекает клинически мягко, с умеренными биохимическими сдвигами. Возможны периоды полной нормализации активности аминотрансфераз, но со стойкой небольшой диспротеинемией. При этом сравнительно удовлетворительное общее состояние больных с отсутствием клинических стигм тяжелого поражения печени может контрастировать с резко выраженными морфологическими признаками прогрессирующего воспалительного процесса.
Работоспособность больных сохраняется, если работа не связана с тяжелыми физическими нагрузками и отрицательными эмоциями, частыми командировками, контактом с ядами, ночными и сверхурочными работами. Больные с активными формами хронического гепатита нуждаются в дополнительном отдыхе, работе с укороченным рабочим днем или иногда в переводе на более легкую работу, т. е. являются инвалидами III группы. В каждом отдельном случае вопрос о трудоустройстве целесообразно решать индивидуально.
Хроническая инфекция, обусловленная гепатотропными вирусами, может протекать в виде пяти основных клинико-морфологических форм: бессимптомного вирусоносительства, при котором морфологически ткань печени интактна или обнаруживает черты неспецифического реактивного гепатита; хронического персистирующего гепатита; хронического активного гепатита; цирроза печени вирусной этиологии и гепатоцеллю лярного рака печени, который развивается через несколько десятилетий вирусоносительства на поздних этапах инфекции, как правило, на стадии цирроза печени (см. рис. 1).
У вирусоносителей обычно отсутствуют жалобы, но иногда бывают астенизация и небольшие боли в области правого подреберья. В биоптате печени изменений нет или выявляется картина «минимального» гепатита с умеренной лейкоцитарной инфильтрацией в портальных полях и рассеянными по печеночной дольке гепатоцитами с матово-стекловидной цитоплазмой. Отмечается также портальный фиброз различной степени в зависимости от тяжести и продолжительности предшествующей стадии хронического гепатита. и соавт. (1983) выявили интактную печень у 30% из 105 клинически здоровых носителей HBsAg; у 12% выявлялась жировая печень и у 58%—спектр морфологических изменений от «минимального» до острого и хронического активного гепатита.
F. Ishida и соавт. (1975) при морфологическом исследовании печени 20 доноров крови — бессимптомных носителей HBsAg с нормальной активностью аминотрансфераз и нормальным содержанием иммуноглобулинов крови обнаружила у большинства из них незначительные диффузные изменения печени типа неспецифического реактивного гепатита (латентный «минимальный» гепатит) или умеренную жировую дистрофию и плеоморфизм гепатоцитов без воспалительных изменений. Однако при динамическом наблюдении у % больных выявлялись небольшие отклонения печеночных функциональных проб, у 40% носителей отмечались признаки недостаточности системы клеточного иммунитета, снижение РБТЛ или блокирование торможения миграции лейкоцитов очищенным HBsAg.
М. Rizzetto et al. (1976) при обследовании 24 носителей HBsAg без клинических или биохимических признаков заболевания печени у 16 не обнаружили отклонений в пунктате печени, у 2 был найден очаговый неспецифический гепатит, у 1— гистиоцитарная гранулема, у 2 — жировая печень, у 2 — фиброз портальных трактов и у 1 — ХПГ. Поскольку минимальные степени стеатоза и очаговых воспалительных изменений в печени часто выявляются у практически здоровых, неинфицированных лиц, авторы считают, что эти изменения не являются следствием антигенем. ии. Большую частоту морфологической картины неспецифического реактивного гепатита (35%) у доноров крови с положительным HBsAg отмечают также F. Ste igmann и соавт. (1972). Выявление HBsAg всегда требует тщательного стационарного обследования больного для исключения не только хронического заболевания печени, но и многих других системных заболеваний, протекающих с иммунным дефицитом. Так, например, HBsAg выявляют у 75% больных системной красной волчанкой [R. Koff, 1974].
Наиболее частыми, хотя и неспецифичными клинико-мор фологическими формами хронического вирусного гепатита являются хронический персистирующий (ХПГ) и хронический активный гепатит (ХАГ), которые представляют по существу дефектную иммунную воспалительную реакцию на локализованные в клетках печени антигенные детерминанты вируса или на измененные при взаимодействии с возбудителем макромолекулы самой клетки. Обе формы хронического гепатита независимо от этиологии в зарубежной литературе нередко обозначаются как хроническое активное заболевание печени [Sher lock Sh., 1974]. Действительно, термин «неактивный гепатит» (например, применительно к ХПГ) не имеет смысла, так как буквально означает «неактивное воспаление печени» (если есть воспаление, то оно всегда характеризуется той или иной степенью активности).
Помимо вирусной инфекции, которая является наиболее частым причинным фактором, морфологическая картина ХПГ или ХАГ возможна при хронических токсических гепатитах, при аутоимммунном хроническом гепатите, в начальной стадии первичного билиарного цирроза печени, при метаболических наследственных заболеваниях печени (болезнь Вильсона, недостаточность ai-антитрипсина), при системных заболеваниях, например, макроглобулинемии Вальденстрема, коллагенозах [Апросина 3. Г. и др., 1971], хроническом энтероколите с иммунным дефицитом, хроническом язвенном колите, болезни Крона, при хронических инфекциях и при злокачественных новообразованиях, в частности лимфомах [ и др., 1984]. Максимальная частота выявления HBsAg при ХПГ составляет 80%, при ХАГ—61% [Caughan G. et al„ 1982; Thaler Н., 1982], т. е. вирусная инфекция является наиболее частой причиной этих форм хронического гепатита.
Между ХПГ и ХАГ нет резких границ, возможны переходные формы: ХПГ с некоторыми чертами ХАГ и ХАГ с нерезко выраженной активностью, картина которого близка ХПГ. Наконец, обе морфологические формы могут представлять различные этапы эволюции хронического гепатита у одного и того же больного, т. е. возможна эволюция ХАГ в ХПГ или реже ХПГ в ХАГ. Жалобы больных при ХПГ и ХАГ вирусной этиологии могут быть сходны. Так, и соавт. (1984) обнаружили астеновегетативный и болевой синдромы у всех обследованных ими больных ХАГ вирусной этиологии и более чем у ^з больных ХПГ. Согласно нашим данным [, , 1973], на слабость и быструю утомляемость жаловались 72% больных ХПГ и 82% больных ХАГ, на периодические или длительные болевые ощущения в области правого подреберья—соответственно 86 и 65% больных, на боль в подложечной области— 18 и 24%. Одинаково часто в обеих группах отмечались диспепсические нарушения: вздутие живота, тошнота и рвота, горечь и сухость во рту, наклонность к диарее или к запору, снижение аппетита (у V4 больных), похуда ние, боль в суставах, в области сердца, сердцебиение, бессонница, головная боль и головокружение. При ХАГ значительно чаще больные жаловались на периодическую желтушность и зуд кожи (у /з больных), одышку при физической нагрузке. Начальными проявлениями болезни у больных обоими формами хронического гепатита часто были длительный период болей в правом подреберье или в подложечной области, астения, гепатомегалия (чаще при ХПГ) или внезапное развитие умеренной желтухи (чаще при ХАГ). У некоторых больных гепатомегалия выявляется случайно, при врачебном осмотре по другому поводу.
В объективном статусе при ХАГ значительно чаще, чем при ХПГ, выявляют наряду с увеличением печени умеренную спленомегалию, малые печеночные знаки — телеангиэктазии, эритему ладоней, в лабораторных пробах — повышение активности аминотрансфераз, обычно превышающее не более чем в 3—5 раз верхнюю границу нормы (соответственно у 83 и 16% больных), и умеренную гипергаммаглобулинемию (до 20 г/л).
Основным правилом диагностики хронического гепатита является исключение заболевания печени при жалобах на астению, диспепсию и боль в животе. При любых острых или хронических заболеваниях органов брюшной полости — хроническом или остром гастрите, гастроэнтерите, хроническом холецистите, панкреатите, хроническом колите, дискинезии желчных путей и кишечника, хроническом гастродуодените и язвенной болезни, хроническом аппендиците, грыже пищеводного отверстия диафрагмы — необходимо проводить дифференциальный диагноз с хроническим заболеванием печени. В связи с малой специфичностью жалоб больных при хроническом гепатите, частым несоответствием жалоб степени поражения печени и большой частотой сопутствующих хроническим гепатопати ям перечисленных выше заболеваний брюшной полости «ге патологическая настороженность» уместна по отношению ко всем больным гастроэнтерологического профиля. Ярким примером пагубных последствий отсутствия такой настороженности может служить следующая история болезни.
45 лет, наблюдался в течение 10 лет в поликлинике областного центра. Последние 8 лет его беспокоили тошнота, снижение аппетита, периодическая боль в подложечной области, немотивированная общая слабость. Позднее присоединилось упорное вздутие живота. У больного дважды диагностировали острый гастрит, затем хронический гастрит. При гастрофиб роскопии была выявлена язва желудка, по поводу которой его дважды лечили в стационаре. Во время второй госпитализации у больного на фоне постинъекционного абсцесса, сопровождавшегося высокой лихорадкой, развились желтуха, асцит, гиперазотемия, массивное желудочно-кишечное кровотечение из острых язв и эрозий желудка и кишечника, печеночная кома. На вскрытии обнаружен не диагностированный при жизни высокоактивный с множественными некрозами паренхимы цирроз печени, по-видимому, вирусной этиологии. Вероятно, заболевание печени у больного можно было диагностировать еше на стадии хронического активного гепатита при более внимательном анализе его жалоб и своевременном проведении элементарных функциональных пече ночных проб.
Хронический персистирующий гепатит
В пунктатах печени больных хроническим персистирующим гепатитом (ХПГ), который развивается у 3—6% больных, перенесших ОВГ-В, и у 10—12% после ОВГ - ни А ни В, наиболее типичной находкой является портальный гепатит — выраженная инфильтрация лимфоидными клетками портальных и пери-портальных областей, не нарушающая целостности пограничной гепатоцитарной пластинки (слой печеночных клеток, отделяющий портальное соединительнотканное пространство от печеночной дольковой паренхимы) или вызывающая лишь незначительную очаговую ее эрозию. Некоторые мерфологи рекомендуют любое нарушение целостности пограничной пластинки рассматривать как проявление ХАГ. По-видимому, решающее диагностическое значение в таких «пограничных» случаях должна иметь динамика заболевания на протяжении нескольких лет. ХПГ протекает без выраженного внутридолько вого фиброза, с полным сохранением структуры печеночных долек, отсутствием мелкоочаговых («ступенчатых») некрозов паренхимы печени (хотя возможны некрозы единичных печеночных клеток), но нередко с мезенхимально-й внутридолько вой реакцией—узелковой гипертрофией и гиперплазией звездчатых ретикулоэндотелиоцитов и с внутридольковыми круглоклеточными инфильтратами [, 1975; Bi anchi L., 1969; Rossler R. et al., 1970]. Возможно развитие портального фиброза и коротких фиброзных септ, проникающих. на небольшое расстояние в паренхиму из расширенных портальных трастов. Своеобразным морфологическим вариантом ХПГ является хронический лобулярный гепатит (центральный гепатит), при котором изменения в пунктате печени напоминают картину реконвалесцентной фазы ОВГ (рис. 5). При этом нерезко выраженные воспалительные круглоклеточные инфильтраты локализуются преимущественно в центральных и промежуточных отделах печеночной дольки. При лапароскопии у больных ХПГ находят умеренно увеличенную красноватого оттенка печень с гладкой поверхностью, местами с очаговыми поверхностными утолщениями серозной оболочки [Логинов А. С., 1969].
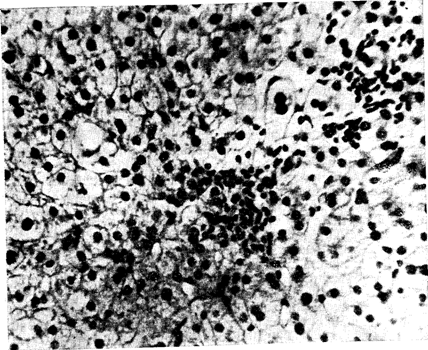
Рис. 5. Лобулярный гепатит. Видны внутридольковые лимфоидно-клеточные инфильтраты. Микрофото. 16Х7. Окраска гематоксилин-эозином.
В клинической картине ХПГ у 70—80% больных преобладают общие симптомы: немотивированная слабость, утомляемость, снижение физической и умственной работоспособности, похудание, нарушения сна, психоэмоциональная лабильность, головная боль. Вторым по частоте субъективным признаком является болевой синдром, наблюдаемый у 60—70% больных: продолжительная или периодическая боль или чувство тяжести в правом подреберье, в подложечной области или в правой половине спины. Этим больным нередко в амбулаторных условиях проводят длительную бесплодную терапию по поводу хронического холецистита или гастрита. Почти столь же частым при ХПГ является диспепсический синдром: плохая переносимость жира, стручковых овощей, капусты и алкогольных напитков, ощущение переполнения, вздутие и распирание живота после еды, плохое отхождение газов, горечь и сухость во рту, тошнота, запор или периодическая диарея. Для ХПГ характерно длительное течение: у большинства больных указанные жалобы отмечаются на протяжении 3—5 лет и более. Вместе с тем до 50% больных ХПГ могут не испытывать субъективных нарушений.
В объективном статусе больных ХПГ наиболее типична умеренная гепатомегалия: край печени, нередко слегка болезненный, пальпируется на 2—4 см ниже реберной дуги по сре динно-ключичной линии; поверхность печени гладкая, консистенция нерезко уплотнена. Селезенка может быть незначительно увеличенной не более чем у 3—9% больных. У больных ХПГ, за редким исключением, отсутствуют внепеченочные органные и системные проявления поражения печени и сопутствующие им иммунные сдвиги: существенных изменений концентрация иммуноглобулинов крови не происходит (возможно умеренное повышение концентрации IgG), отсутствуют циркулирующие аутоантитела к специфическому антигену человеческой печени. Вместе с тем при ХПГ вирусной этиологии часто, не менее чем у /з больных, определяются антигенные маркеры вирусной инфекции: HBsAg (у 40—60% больных) в значительно более высоком, чем при ХАГ, титре [ и др., 1977; Mezey E. 1982] и у 50% носителей HBsAg—также и HBeAg.
Ограниченной и неагрессивной воспалительной реакции печени при ХПГ соответствуют нерезко выраженные изменения печеночных проб; у 15—20% больных они могут быть нормальными. В большинстве случаев наблюдается стойкая умеренная гипераминотрансфераземия с преимущественным повышением активности АлАТ. Гиперферментемия при ХПГ обусловлена не повышенным цитолизом печеночных клеток, а ферментативной индукцией. Она выражена при 3-м морфологическом варианте ХПГ—хроническом септальном гепатите—с очаговой эрозией пограничной пластинки, часто с наличием коротких фиброзных септ вблизи портальных трактов и единичными мелкооча говыми некрозами в области отдельных портальных полей и в печеночных дольках. Эта форма — тип Ic [Volmer L., 1979] в отличие от ХПГ типа 1а (хронический лобулярный гепатит) и типа 1в (классический вариант ХПГ — хронический портальный гепатит) может с частотой до 10% переходить в ХАГ. Поэтому многие авторы рассматривают ХПГ типа Ic как промежуточную между ХПГ и ХАГ форму, при которой точный диагноз возможен только при длительном наблюдении [Schmid М., 1979; Roderick M., 1980], или, что на наш взгляд более целесообразно, относят эту разновидность хронического гепатита к ХАГ с умеренно выраженной активностью [, , 1982].
Остальные биохимические печеночные пробы при ХПГ не изменены или изменены умеренно: возможно нерезкое повышение показателя тимоловой пробы, у 5—38% больных—небольшая гипергаммаглобулинемия, у 18%—повышенная задержка бромсульфалеина. Желтуха гепатоцеллюлярного типа при ХПГ не наблюдается. Развитие такой желтухи указывает на повторное заболевание ОВГ. Вместе с тем у некоторых больных ХПГ, перенесших ОВГ, наблюдается умеренная неконъюгиро ванная гипергбилирубинемия — постгепатитная гипербилиру бинемия (вариант синдрома Жильбера) с перемежающимся желтушным окрашиванием склер и иногда кожи [ С,. , 1977, 1978]. У этих больных ОВГ перешел в хроническую форму и одновременно выявил ранее скрытую генетическую аномалию метаболизма билирубина.
Дифференциальный диагноз ХПГ проводят со многимд заболеваниями вирусной и невирусной этиологии. В отличие от безжелтушной и легкой форм ОВГ—«минимальной», портальной [, 1979; Banchi L., 1969; Klinge 0., 1976] при ХПГ отсутствует лихорадка первой недели, значительно менее повышена активность АлАТ крови. При ремиссии ХАГ любой этиологии, спонтанной или под влиянием терапии, морфологическая картина ХПГ отражает лишь малоактивную стадию ХАГ и не соответствует понятию ХПГ как благоприятно текущего заболевания печени. Умеренный подъем активности ами нотрансфераз крови может наблюдаться при жировом гепа тозе, особенно при алкоголизме. Решающее диагностическое значение в таких случаях имеет анамнез и пункционная биопсия печени. Морфологическую картину ХПГ можно наблюдать у больных алкогольным поражением печени в период абсти ненции после атаки острого алкогольного гепатита, при хроническом лекарственном гепатите, при желчнокаменной болезни, при хронических и системных инфекциях, например, при хроническом пиелонефрите, гнойных инфекциях различной локализации, туберкулезе, злокачественных опухолях.
Наиболее труден дифференциальный диагноз ХПГ с хроническим неспецифическим реактивным гепатитом, морфологические проявления которого могут напоминать ХПГ. Поэтому у всех больных ХПГ необходимо исключить внепеченочную причину хронического гепатита: острые и хронические инфекции, глистные инвазии, коллагенозы и пр. При реактивном гепатите активность аминотрансфераз крови и остальные печеночные пробы обычно нормальны. Исключение составляют редкие случаи синдрома Штеффена, часто протекающего с желтухой (неметастатическое поражение печени при гипернефроме).
Иногда при ХПГ вирусной этиологии с болевым синдромом ошибочно диагностируют хронический холецистит. Важно иметь в виду, что хронический бескаменный холецистит относится к сравнительно редким заболеваниям. Диагноз его обоснован лишь при наличии объективных симптомов органического поражения желчного пузыря — стойкой атонии пузыря, рентгенологических или сонографических признаков перипу зырного спаечного процесса, деформации пузыря или затруднении оттока желчи при шеечном холецистите, наличии симптомов холецистоза с начальным утолщением стенки, неровностью контуров слизистой оболочки и гиперкинезией, и наконец, утратой сократительной способности пузыря.
Болевой синдром в области правого подреберья при исключении весьма распространенного калькулезпого холецистита, редкого бескаменного холецистита, органических заболеваний печени, воспалительных заболеваний правых придатков матки с распространением на подпеченочную брюшину, язвенной болезни, органических поражений правой почки и мочеточника, правой половины толстой кишки, аппендикса при его подпе ченочной локализации наиболее часто наблюдается у соматически здоровых лиц, страдающих неврастенически-ипохондрическими синдромами нередко с элементами канцерофобии и циррозофобии. (1983) отмечает, что «нервные и рефлекторные механизмы могут вести к дискинезии и спазму внепеченочных желчных путей и самого пузыря» и что «уже давно плохое настроение (под влиянием эмоциональных воздействий) и ипохондрию связывают с правым подреберьем...» Мы наблюдали больного врача-ортопеда, который в течение Г/2 года самостоятельно принимал малые дозы предни золона, так как был убежден, что страдает «циррозом печени» (ранее он перенес эпидемический гепатит). Опасения больного рассеялись только после получения результатов исследования пунктата печени, в котором была найдена небольшая очаговая жировая дистрофия, очевидно, индуцированная пред низолоном.
Боли в правом подреберье и другие сенестопатии и алгии наблюдаются при затяжной непсихотической ипохондрии у лиц с остаточными явлениями органического поражения ЦНС инфекционной или инволютивной этиологии и у лиц с патологическим развитием личности [, 1984], а также при эндогенной или экзогенной психической депрессии. Депрессия — одно из самых частых заболеваний в медицине, как правило, сопровождается быстрой физической и психической исто щаемостью, бессонницей, головной болью, запором, разнообразными диспепсическими расстройствами, алгией и часто упадком питания из-за анорексии. При болевом синдроме, не имеющем объективного обоснования, врач должен исключить три вида психических расстройств: истерию, неврастению и депрессию.
Наиболее характерна для таких больных своеобразная пси хопатологичеокая триада: 1) обилие и полиморфизм жалоб или, наоборот, стойкая фиксация на единственном болезненном ощущении (упорная постоянная боль, «жжение» или «прокалывание» в правом подреберье, обычно в одной точке) с аффективно-тревожной окраской жалоб. При внимательном расспросе больного часто удается выявить элементы фобии, т. е. страха перед тяжелым, неизлечимым заболеванием, например, в связи со смертью родственника от рака или от цирроза печени; 2) отсутствие объективных лабораторных и инструментальных данных, которыми можно было бы объяснить жалобы больного; 3) неэффективность любых методов медикаментозной терапии, за исключением психотропных медикаментов. Тревожно-депрессивный фон и стремление соблюдать строгую диету нередко приводят к снижению аппетита, запору, асте низации больного и упадку питания. Такие лица действительно производят впечатление хронически больных, и не удивительно, что у многих из них оказывается сниженным противоин фекционный иммунитет.
Часто создается впечатление, что больных этой категории «не радует» и вызывает негативную реакцию заключение об отсутствии у них серьезного органического недуга. Они упорно настаивают на бредовой концепции «рака» или «цирроза печени», несмотря на все уверения врача и демонстрацию результатов многочисленных исследований. Только настойчивая психотерапия, иногда в сочетании с малыми дозами транк вил. изаторов и антидепрессантов, облегчает состояние. Госпитализация больных с неврастенически-ипохондрическим синдромом в соматический стационар—распространенная и дорогостоящая ошибка. Такие больные, по существу нетерапевтического профиля, с большой неохотой покидают больничную койку, период их госпитализации нередко значительно затягивается в связи с разнообразным обследованием и отсутствием эффекта от проводимой терапии. Последнее обстоятельство по принципу порочного круга еще более укрепляет убеждение больного в наличии у него неизлечимого недуга и некомпетентности лечащих врачей.
У большинства больных ХПГ вирусной этиологии имеет благоприятное течение и хороший прогноз. Полное выздоровление на протяжении 5—15 лет наблюдается у 25% больных, переход в прогредиентные формы хронического гепатита возможен у 8—10% больных. При диспансеризации на протяжении от 2 до 10 лет 97 больных ХПГ мы ни у одного из них не наблюдали перехода в ХАГ или в цирроз печени.
В связи с благоприятным прогнозом больные ХПГ не нуждаются в специальной лекарственной терапии. Необходимо только динамическое диспансерное наблюдение с периодическим (1 раз в 6—12 мес) определением показателей основных биохимических проб печени (активность аминотрансфераз и белковых фракций сыворотки крови, тимоловая проба). Больным ХПГ целесообразно максимально ограничить прием медикаментов, поскольку сами по себе лекарственные средства при длительном их применении являются причиной дистрофических изменений гепатоцитов, диффузных воспалительных и фибро зирующих реакций, жировой инфильтрации печени, т. е. индуцируют клинически латентно протекающие гепатопатии [Zimmerman H., 1979]. Таким больным, в частности, не показано применение желчегонных средств, настоев лекарственных трав, печеночных экстрактов, липотропных препаратов, применение физиотерапевтических процедур на область печени, курсовое введение минеральных вод и инфузионная терапия. При ХПГ вирусной этиологии противопоказаны глюкокортикостероиды, иммунодепрессивные и другие сильнодействующие средства. Больные должны получать четырехразовое питание, полноценную сбалансированную диету с полным исключением алкогольных напитков и ограничением тугоплавких животных жиров, грибов, консервированных, копченых и вяленых продуктов, жареных блюд, изделий из шоколада, крема и сдобного теста.
«Всякая диететика начинается предписанием: Будь спокоен духом!»—справедливо замечает . В связи с частотой у больных ХПГ вегетодистонических симптомов и ипохондрически-депрессивных наслоений большое значение имеет систематическая психотерапия. Необходимо разъяснить больному доброкачественный характер его заболевания и избегать по возможности назначения седативных средств, транквилизаторов и антидепрессантов; допустимо применение настоя корня валерианы и пустырника и не обладающего гепатоток сическим свойством тазепама (оксазепама).
В стационарных и амбулаторных условиях больным ХПГ проводят курсы витаминотерапии (кокарбоксилаза, пиридок син, аскорбиновая кислота, рутин, рибофлавин).
Физическую и трудовую активность больных ХПГ существенно не ограничивают, однако советуют избегать тяжелых физических и психоэмоциональных нагрузок, участия в спортивных соревнованиях, ночных и сверхурочных работах, частых и длительных командировках.
При ХПГ вирусной этиологии не противопоказаны беременность и роды. Состояние больных и показатели функциональных проб печени во время и после беременности обычно не ухудшаются, у больных рождаются здоровые дети, требующие, однако, эпидемиологического наблюдения в связи с возможностью передачи вирусной инфекции через плаценту [Infeld D. et al., 1979].
Хронический активный гепатит
Хронический активный гепатит (ХАГ) вирусной этиологии (морфологические термины: хронический агрессивный гепатит, хронический перипортальный гепатит, прогредиентный гепатит) развивается в 2—3 раза реже, чем ХПГ [Redeker A„ 1975]. До 60% больных являются носителями HBsAg. У 58% больных находят Е-антиген, что указывает на неблагоприятное течение гепатита [Wright R., 1980]. Заболевание наблюдается во всех возрастных группах, несколько чаще у мужчин, чем у женщин, в основном в возрасте 15—50 лет. ХАГ развивается у 3% больных (ХПГ у 7%), перенесших ОВГ-В, особенно легкую или бессимптомную его форму, и у 20—40% больных, перенесших ОВГ - ни А ни В. У 15—20% больных отсутствуют указания на перенесенное ранее острое заболевание печени. У некоторых больных начальные симптомы ХАГ возникают через 1—5 лет или позже после перенесенного ОВГ. Часто заболевание начинается исподволь, постепенно, с появления на фоне полного здоровья явлений астении: общей слабости, быстрой утомляемости, желудочно-кишечного дискомфорта, боли в области правого подреберья, анорексии, похудания и нередко умеренной желтухи. Субъективные жалобы при ХАГ обычно выражены в большей степени, чем при ХПГ. При этом возможна широкая гамма нарушений — от полного субъективного благополучия при ХАГ с умеренной активностью до резко выраженной астенизации с явлениями энцефалопатии при некро тизирующих формах.
При ХАГ вирусной этиологии с выраженными воспалительно-некротическими изменениями и внутрипеченочным хо лестазом наблюдаются геморрагический синдром (кровотечение из носа и десен, подкожные кровоизлияния), субфебрилитет или высокая лихорадка (гриппоподобный дебют ХАГ), боль в суставах, изменения цвета мочи и кала. Иногда начальным симптомом бывает длительное умеренное повышение СОЭ, боль в области правого подреберья. У некоторых больных без гепатомегалии возможно начало заболевания с внепе ченочных проявлений — артралгии, анемии, кровоточивости, стойкой диареи, но наиболее часто больного приводит к врачу длительная немотивированная общая слабость и снижение трудоспособности.
Гепатомегалия наблюдается у большинства больных ХАГ, однако в отдельных случаях она может быть выражена нерезко или даже отсутствовать. У больных ХАГ нередко наблюдается умеренная спленомегалия, обычно без лабораторных признаков гиперспленизма. Выраженная тромбоцитопения или лейкопения часто обусловлена аутоиммунным генезом (образованием в селезенке соответствующих аутоантител). Малые печеночные знаки (эритема ладоней, телеангиэктазии) наблюдаются не менее чем у /з больных ХАГ вирусной этиологии, т, е. значительно чаще, чем при ХПГ и при гепатомегалии, обусловленной жировой дистрофией печени [, Е„ 1973].
На сканограмме при ХАГ обычно выявляется гепатомега лия, иногда с несколько повышенной фиксацией радионуклида в селезенке.
Решающее значение для раннего диагноза ХАГ имеет своевременное проведение основных биохимических печеночных проб, особенно повторное определение активности аминотранс фераз сыворотки крови. При обострении ХАГ активность аминотрансфераз, в большей степени АлАТ, повышена не менее чем в 3 раза. При ХАГ степень активности аминотрансфераз крови соответствует интенсивности воспалительно-некротического процесса в печени и, следовательно, является важнейшим показателем динамики ХАГ. Вместе с тем снижение и даже нормализация активности аминотрансфераз при сохранении и особенно нарастании диспротеинемии могут отражать переход ХАГ в цирроз печени с умеренной или минимальной активностью [, , 1982]. Помимо АлАТ и АсАТ, при ХАГ повышается активность гамма-глутамилтранс пептидазы (у-ГТП) крови, что при умеренной гиперамино трансфераземии может помочь в дифференциальном диагнозе между ХАГ и ХПГ [Adolph L., Lorenz R., 1982]. При ХАГ с резко выраженной активностью, с тяжелыми поражениями ге патоцитов увеличена и активность митохоидриального фермента—глутаматдегидрогеназы (ГДГ) сыворотки. При холеста тическом варианте ХАГ наряду с - у-ГТП повышена активность щелочной фосфатазы (ЩФ) и лейцинаминопептидазы (ЛАП) крови. При особенно тяжелом некротическом поражении печени снижаются активность синтезируемой печенью холинэсте разы, концентрация сывороточного альбумина и факторов свертывающей системы крови — ферментов протромбинового комплекса (менее чем до 50%).
Нередко при ХАГ вирусной этиологии отмечается также умеренная конъюгированная гипербилирубинемия и нерезко выраженная диспротеинемия (гамма-глобулин сыворотки в пределах 18—20 г/л) с увеличением показателя тимоловой пробы. Концентрация общего белка сыворотки при ХАГ вирусной этиологии повышена незначительно в отличие от ХАГ аутоиммунного типа, при котором наблюдается резко выраженная гиперпротеинемия, гиперглобулинемия и гипергамма глобулинемия. Концентрация иммуноглобулинов крови, особенно IgG и IgM, при ХАГ достоверно выше, чем при ХПГ [, 1980].
ХАГ вирусной этиологии протекает длительное время латентно в отличие от идиопатического, аутоиммунного ХАГ. Часто серьезные осложнения, связанные с развитием цирроза печени, возникают через 10—20 лет после начала заболевания. Характерным отличием ХАГ вирусной этиологии от аутоиммунного ХАГ является наклонность к спонтанным, нередко временным, клинико-биохимическим ремиссиям с полной или почти полной нормализацией биохимических печеночных проб; при этом активность аминотраксфераз превышает верхнюю границу нормы не более чем в 2 раза, снижается до нормальных цифр концентрация билирубиьз и гамма-глобулина крови, морфологическая картина ХАГ в пунктате печени сменяется картиной ХПГ или даже неспецифически-реактивного гепатита. При ХАГ аутоиммунного типа, как правило, ремиссии наступают только после иммунодепрессивной терапии. Эта особенность ХАГ вирусной этиологии чрезвычайно затрудняет оценку эффективности лекарственной терапии и иногда дифференциальный диагноз с ХПГ.
Серологической особенностью вирусного ХАГ является сравнительная редкость, в отличие от аутоиммунного ХАГ, обнаружения в сыворотке крови органонеспецифических аутоанти тел к компонентам ядер, микросом, митохондрий и гладкой мускулатуры и более умеренное, чем при аутоиммунном ХАГ, повышение концентрации иммуноглобулинов сыворотки крови (в основном IgG). Серологические маркеры вирусной инфекции встречаются при ХАГ вирусной этиологии реже, чем при ХПГ, поэтому их отсутствие не исключает вирусную природу заболевания печени.
Клинически обоснованное подозрение на ХАГ или на какое-либо другое хроническое активное (прогредиентное) заболевание печени служит важнейшим показанием к пункционной биопсии печени. При этом необходимо иметь в виду, что морфологическая картина хронического агрессивного гепатита, так же как и картина ХПГ, является отражением неспецифической дефектной иммунной реакции печени на многие этиологические факторы и может наблюдаться не только при вирусной инфекции, но и при аутоиммунном гепатите, алкогольной гепатопа тии, хронических лекарственных гепатитах, в начальных стадиях болезни Вильсона — Коновалова и первичного билиарно го цирроза печени, при хроническом прогрессирующем заболевании печени, обусловленном недостаточностью алфа1-антитрип сина, и при некоторых системных и миелопролиферативных заболеваниях. J. Hodges и соавт. (1982), обследовавшие в течение 5 лет в Англии популяцию населениячеловек, выявили 61 больного ХАГ в возрасте в среднем 56 лет. Частота ХАГ составила 3: 100000 населения в год. У 20% больных установлен ХАГ вирусной этиологии, у 26% — алкогольной и у 23% этиологию установить не удалось. У Уз больных при постановке диагноза субъективные симптомы отсутствовали. Тяжелое течение с быстро прогрессировавшими биохимическими и гистологическими сдвигами наблюдалось у незначительного числа больных. Больные ХАГ вирусной, лекарственной и алкогольной этиологии не реагировали на иммунодепрессивную терапию.
Наиболее характерная морфологическая особенность ХАГ— мелкоочаговый (ступенчатый) некроз гепатоцитов в периферических отделах печеночной дольки, т. е. в части паренхимы печени, примыкающей к портальным полям (зона I печеночного ацинуса по Rappoport, см. рис. 6). Очаговые некрозы пери портальной паренхимы всегда сопровождаются массивной инфильтрацией этой области печеночной дольки иммунокомпе тентными клетками — главным образом активированными лимфоцитами и в меньшей степени плазматическими, гистиоци тарными клетками и полиморфно-ядерными лейкоцитами. Плазматические клетки преобладают над лимфоидными при аутоиммунных формах ХАГ, полиморфно-ядерные лейкоциты встречаются при ХАГ алкогольной этиологии. Лимфогистио цитарно-плазматические воспалительные инфильтраты, исходящие из расширенных портальных полей, разрушают пограничную гепатоцитарную пластинку и проникают в перипор тальное пространоство, распространяясь в ряде случаев далеко в глубь дольки по ходу ступенчатых некрозов гепатоцитов. Печеночные клетки в зонах очаговых некрозов увеличены в объеме и нередко образуют розетковидные железистые структуры, отражающие регенераторную активность сохранившихся клеток в неблагоприятных условиях. В дальнейшем по ходу некротических поражений могут образовываться активные, т. е. вновь возникшие и инфильтрированные воспалительными клетками соединительнотканные септы. Прогрессирование или выраженная активность воспалительно-деструктивного процесса при ХАГ может вести к развитию мультилобулярных (сливных) некрозов, т. е. некрозов нескольких прилежащих печеночных долек, или «мостовидных некрозов», простирающихся между двумя соседними портальными трактами или между портальными трактами и центральными венами. Образующиеся на месте таких некрозов соединительнотканные септы расчленяют дольку, вызывают нарушение кровоснабжения, способствуют возникновению беспорядочной узелковой регенераторной реакции в уцелевших между фиброзными тяжами островках паренхимы, формированию «ложных» регенераторных печеночных долек различной величины и макронодуляр ного цирроза печени. Вирусная этиология ХАГ подтверждается выявлением в биоптатах печени гепатоцитов с матово-стекловидной цитоплазмой, т. е. содержащих HBsAg, или с «песочными» ядрами, т. е. содержащих HBcAg.

|
Из за большого объема эта статья размещена на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |



