На правах рукописи
ПЕТРЕНКО
Татьяна Игоревна
ТУБЕРКУЛЁЗ ЛЁГКИХ В СОЧЕТАНИИ С
ХРОНИЧЕСКИМИ ВИРУСНЫМИ ГЕПАТИТАМИ:
ДИАГНОСТИКА, ЛЕЧЕНИЕ, ПРОГНОЗ
14.00.26 – фтизиатрия
14.00.10 – инфекционные болезни
Автореферат
диссертации на соискание ученой степени
доктора медицинских наук
Новосибирск – 2008
Работа выполнена в Новосибирском научно-исследовательском институте туберкулёза Федерального агентства по здравоохранению и социальному развитию
Научные консультанты:
доктор медицинских наук, профессор
доктор медицинских наук, профессор
Официальные оппоненты:
доктор медицинских наук, профессор
доктор медицинских наук, профессор
доктор медицинских наук, профессор
Ведущая организация: Санкт-Петербургский научно-исследовательский институт фтизиопульмонологии Федерального агентства по здравоохранению и социальному развитию
Защита состоится «___»______2008 года в ___часов на заседании Диссертационного совета Д 208.062.01 при Новосибирском государственном медицинском университете Федерального агентства по здравоохранению и социальному развитию г. Новосибирск, Красный проспект, 52.
С диссертацией можно ознакомиться в библиотеке Новосибирского государственного медицинского университета
Автореферат разослан «___»__________2008 года
Ученый секретарь Диссертационного совета,
кандидат медицинских наук, доцент
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Туберкулёз лёгких (ТЛ) – одна из важнейших современных медико-социальных проблем вследствие широкой распространенности, сохраняющейся тенденции роста числа больных, их высокой инвалидизации и смертности, ограниченных возможностей и токсичности противотуберкулёзной терапии ( и соавт., 2003; , 2003; , 2005; , 2007). В последние годы регистрируют возрастание заболеваемости сочетанными инфекциями с участием различных вирусов. Развитие инфекционного заболевания определяется многообразием факторов: воздействие ксенобиотиков при несостоятельности механизмов детоксикации, нарушение внутренней среды организма и системы иммунитета, истощения резервов компенсации у лиц с сочетанной патологией ( и соавт., 2007). Изменения гомеостаза, характера метаболических и иммунных реакций в условиях персистирующих вирусных инфекций обуславливают новые качественные характеристики туберкулёза.
В наступившем столетии туберкулёз, вирусные гепатиты В и С признаны ведущей патологией (ВОЗ, 2002). Вопрос о взаимном влиянии двух инфекций – ТЛ и хронического вирусного гепатита (ХГ) представляет большой интерес из-за высокой частоты их сочетания ( и соавт., 2005) и в связи с ведущей ролью печени в иммунном ответе, в детоксикации и метаболизме противотуберкулёзных препаратов (, 2007).
Угнетение монооксигеназной системы печени (МОС) приводит к увеличению частоты токсических реакций на лекарственные препараты, инактивация которых осуществляется печенью (, , 1997; , , 2004). Один из наиболее информативных показателей активности МОС – антипириновый тест, который рассматривают как отражающий «окислительный метаболизм лекарств печени» (Gurley B. J. et al., 1997), и как «общую метаболическую пробу» (Matzke G. R. et al., 2000). Несмотря на значительное число работ, посвящённых метаболизму антипирина при различных заболеваниях, лишь в единичных оценивается активность МОС у больных ТЛ (Hamide A. et al., 1990), не определена зависимость состояния МОС от способов и кратности приема противотуберкулёзных препаратов.
Традиционная многомесячная ежедневная бактериостатическая терапия туберкулеза часто вызывает у больных побочные (особенно гепатотоксические) реакции, лекарственную болезнь, и может явиться причиной смерти пациента (, 2002; Decocq G. et al., 1996; Ungo J. R. et al., 1998). В связи с ростом лекарственно-устойчивых форм ТЛ эксперты ВОЗ рекомендуют назначать 6–8 противотуберкулёзных препаратов (ПТП) ежедневно без учета сопутствующей патологии и активности МОС. Такое лечение вызывает появление побочных реакций на основные ПТП в 17 % случаев ( и соавт., 2003), а на препараты 2-го ряда – в 73 % ( и соавт., 2004). Развитие побочных реакций ограничивает возможности химиотерапии и снижает эффективность лечения больных ТЛ по таким критериям, как сроки прекращения бактериовыделения и закрытия каверн (, 2007).
В Новосибирском НИИ туберкулеза с 70-х годов разрабатывается и внедряется в практику бактерицидная внутривенная химиотерапия больных ТЛ в интермиттирующем режиме с первых дней лечения ( и соавт., 1979). В эксперименте показано, что внутривенное лечение 2 и 3 раза в неделю по сравнению с ежедневным пероральным или внутривенным введением ПТП существенно уменьшает выраженность структурных и обменных нарушений в печени ( и соавт., 1982). В условиях клиники режим внутривенного лечения 2 или 3 раза в неделю высокоэффективен, значительно сокращает количество побочных реакций (, 1983, , 1998). Однако внедрение данной методики химиотерапии в широкую практику противотуберкулёзных учреждений затруднено в связи с приказом № 000 Министерства Здравоохранения РФ от 01.01.2001, регламентирующим назначение 4-х и более ПТП внутрь ежедневно в течение 2-х и более месяцев. Обоснованием служит общепринятое мнение о том, что прерывистость противотуберкулёзной терапии приводит к развитию вторичной лекарственной устойчивости (ВЛУ) возбудителя. Но это не было доказано в случае назначения ПТП внутривенно 2 или 3 раза в неделю, когда концентрации лекарственных веществ в крови в несколько раз выше их минимальной ингибирующей концентрации, а лечение является контролируемым.
Одна только этиотропная химиотерапия, без воздействия на механизмы патологического процесса, часто не позволяет достичь хороших результатов лечения. Накоплены убедительные факты, свидетельствующие об угнетении иммунитета у больных с деструктивными формами ТЛ (, 2004), хроническими гепатитами В и С (, 2002). Негативные изменения иммунитета и при туберкулёзе, и при гепатите проявляются в снижении количества Т-клеток, изменении их субпопуляционной структуры, в пролиферативном характере ответа Т-лимфоцитов на митогены, в нарушении функциональной активности моноцитов, дисбалансом в цитокиновой системе ( и соавт., 2000; и соавт., 2007; Lai C. K. et al., 1997). Наличие иммунодепрессии и сопряженность степени её выраженности с тяжестью сочетанной инфекционной патологии (туберкулёза легких и вирусного гепатита) диктует необходимость поиска эффективных средств иммунокоррекции как важного компонента терапии. В настоящее время одним из перспективных направлений биологической терапии в клинической медицине является применение цитокинов, таких как интерферон-a. Действие его, как инициатора сбалансированной продукции провоспалительных и противовоспалительных цитокинов, показано ранее при различных видах инфекционной патологии ( и соавт., 1998; , 1999; и соавт., 2003; Zein N. N., 1998). Требуется разработка универсальной терапии, направленной на саморегуляцию организма, имеющую сигнальный характер, что достигается выбором доз препаратов, по возможности максимально сниженных, и способов введения (, 2001; и соавт., 2007). Указанные аргументы послужили планированию цели и задач настоящего исследования, посвященного важным вопросам диагностики, лечения и прогноза при сочетанной инфекционной патологии.
Цель работы. На основании изучения особенностей диагностики, закономерностей течения, сравнения режимов противотуберкулёзного лечения и определения факторов, влияющих на прогноз, разработать терапевтическую тактику ведения пациентов с сочетанной инфекционной патологией – туберкулёзом лёгких и хроническим гепатитом В и/или С.
Задачи исследования:
1. Определить частоту выявления и спектр диагностических маркеров HBV - и HCV-инфекции у пациентов противотуберкулезных стационаров с разными сроками течения туберкулёза лёгких.
2. Выявить медико-социальные факторы, ассоциированные с неблагоприятным течением туберкулеза легких (у пациентов с хроническими вирусными гепатитами в сравнении с больными без гепатитов).

3. Определить связь морфологической активности патологических процессов в печени с иммунологическими характеристиками и ответом на противотуберкулёзную терапию у пациентов с сочетанной инфекционной патологией.
4. Дать оценку состояния монооксигеназной системы печени больных с впервые выявленным туберкулёзом лёгких в процессе внутривенной интермиттирующей в сравнении с ежедневной традиционной противотуберкулёзной терапией.
5. Изучить частоту, сроки развития и спектр вторичной лекарственной устойчивости микобактерий туберкулёза у впервые выявленных больных туберкулёзом лёгких, получавших внутривенную интермиттирующую химиотерапию.
6. Проанализировать результаты лечения туберкулёза лёгких у больных моно - и микст-инфекцией с учетом разных режимов терапии (внутривенной интермиттирующей и ежедневной традиционной).
7. Разработать эффективную терапевтическую тактику стационарного ведения больных туберкулёзом лёгких в сочетании с хроническими вирусными гепатитами с включением реаферона в противотуберкулёзную терапию.
8. Оценить влияние интерферонотерапии на особенности тканевых реакций у больных туберкулезом легких с сопутствующими хроническими гепатитами В и С.
Научная новизна. Впервые были исследованы закономерности ответа пациента на одновременное поражение нескольких систем макроорганизма различными инфекционными агентами, изучено влияние патологических процессов разной этиологии друг на друга и на успешность лечения каждого из них.
Впервые определен маркерный профиль хронических гемоконтактных гепатитов у пациентов туберкулёзных стационаров с разными сроками течения ТЛ. Показано, что впервые выявленный туберкулёз лёгких ассоциирован с повышенным относительным риском HBV-инфицирования, а длительно текущий, в том числе хронический ТЛ – HCV - и HCV + HBV-инфицирования.
Установлены факторы, ассоциированные с выявлением хронического вирусного гепатита у больных ТЛ. Выявлены клинические особенности течения микст-инфекции, а также иммунологические, морфологические, биохимические параметры, неблагоприятно влияющие на прогноз туберкулёза лёгких. Показано, что наличие сочетанной инфекционной патологии негативно сказывается на результатах лечения пациентов с впервые выявленным туберкулёзом лёгких.
Установлено, что для прогнозирования и мониторинга токсических осложнений химиотерапии, для определения скорости метаболических процессов в печени больного туберкулёзом лёгких оптимальным методом исследования является легкая в интерпретации, простая в исполнении, атравматичная для пациента антипириновая проба (Патент на изобретение «Способ определения антипирина в слюне» № /15 от 01.01.2001).
Впервые показано, что активность монооксигеназной системы печени у пациентов с туберкулёзом легких на протяжении ежедневного лечения противотуберкулёзными препаратами снижается в сравнении с больными, получавшими внутривенную интермиттирующую химиотерапию, что свидетельствует о более агрессивном характере ежедневной химиотерапии ТЛ в отношении метаболической функции печени.
Установлено, что для пациентов туберкулёзом лёгких с сопутствующими хроническими гепатитами В и С предпочтителен высокоэффективный метод лечения, предупреждающий возникновение токсических реакций, - внутривенная интермиттирующая химиотерапия 2 раза в неделю.
Впервые была изучена частота возникновения вторичной лекарственной устойчивости у пациентов, получавших внутривенную интермиттирующую химиотерапию, в сравнении с группой ежедневного перорального лечения. Выявлено, что частота развития вторичной ЛУ в группах больных была одинакова, а множественная ЛУ при интермиттирующем лечении развивалась реже. В процессе внутривенной интермиттирующей химиотерапии вторичная ЛУ появлялась медленнее, чем при ежедневном приеме химиопрепаратов, в среднем через 3 месяца от начала химиотерапии.
Разработан и применен показатель «плотности доз» противотуберкулезных препаратов с целью объективного разделения пациентов на группы ежедневного и интермиттирующего лечения и беспристрастной оценки результатов лечения ТЛ у них. Этот показатель позволил выявить промежуточную группу «проблемных» больных, регулярность режима приема препаратов у которых по различным причинам нарушена, и проанализировать у них неблагоприятные прогностические факторы течения туберкулёза лёгких.
Впервые для лечения больных туберкулезом легких с сопутствующими хроническими гепатитами В и С применен реаферон (интерферон-a), назначаемый в дозе 3 млн. МЕ ректально капельно в дни проведения внутривенной интермиттирующей противотуберкулёзной терапии (Патент на изобретение № /14 от 01.01.2001). Показано, что в группе пациентов, получавших реаферон, было больше больных, достигших прекращения бактериовыделения и закрытия полости(тей) распада на терапевтическом этапе, причем в более ранние сроки, чем в группе сравнения. Установлено, что комбинированное лечение реафероном в сочетании с внутривенной интермиттирующей химиотерапией 2 раза в неделю приводило к уменьшению сроков восстановления показателей гемограммы, к увеличению количества лимфоцитов крови и их субклассов, к снижению проявлений цитолиза и холестаза.
Впервые получены морфологические признаки противовоспалительного действия реаферона (при включении его в терапию больных с ТЛ) как непосредственно в зоне специфического воспаления, так и в окружающих тканях легкого.
Теоретическая и практическая значимость. Результаты исследования позволяют расширить существующие представления о взаимодействии микст-инфекции (ТЛ + ХГ) в организме больного, о влиянии гепатотропных вирусов на течение, лечение и прогноз туберкулёза лёгких.
Разработана система обследования больных туберкулёзом лёгких, позволяющая выявлять у них хронические вирусные гепатиты в зависимости от их этиологии, биохимической и морфологической активности, и, с учетом этого, планировать лечебные мероприятия.
Выявленные особенности клинического течения сочетанной инфекции, характеризующиеся слабой выраженностью симптомов каждого из заболеваний в отдельности, свидетельствующие о недостаточной активности метаболических и иммунных реакций макроорганизма, определяют поиск дополнительных диагностических и лечебных мероприятий, направленных на полное клиническое излечение пациента от туберкулёза лёгких в условиях персистенции вирусов.
Для прогнозирования течения и исходов туберкулёза лёгких и хронических гепатитов В и С, а также побочных реакций у больных ТЛ предложен весьма простой, неинвазивный, легкий для интерпретации антипириновый тест, проводимый в динамике на протяжении противотуберкулёзной терапии.
С целью объективного разделения пациентов на группы по режиму лечения и оценки эффективности химиотерапии предложен показатель «плотности доз» противотуберкулезных препаратов.
Применение антипиринового теста и показателя «плотности доз» наряду с традиционными клинико-лабораторными методами исследования позволило продемонстрировать, что внутривенная интермиттирующая химиотерапия предпочтительна у пациентов ТЛ с сопутствующими ХГ, как эффективный и предотвращающий токсические реакции способ лечения в условиях скомпрометированной вирусом печени.
Полученные клинико-биохимические, иммунологические и морфологические данные свидетельствуют о высокой терапевтической эффективности реаферона у больных ТЛ с сопутствующими ХГ и позволяют рекомендовать его к практическому применению.
Разработанная тактика ведения больных микст-инфекцией позволяет улучшить верификацию диагноза хронического вирусного гепатита во фтизиатрической практике на 89 %, повысить эффективность лечения туберкулёза лёгких: уменьшить сроки прекращения бактериовыделения на 1,8 месяца, закрытия каверн – на 1,4 месяца.
Положения, выносимые на защиту:
1. Комплексное иммуно-биохимическое обследование пациентов фтизиатрических стационаров Новосибирска позволяет выявлять диагностические маркеры HBV - и HCV-инфекции в 32 – 48 % случаев. У пациентов с длительно протекающим туберкулёзом легких повышены относительные риски HCV - и HCV + HBV-инфицирования, а с впервые выявленным туберкулёзом – HBV-инфицирования.
2. У социально дезадаптированных пациентов туберкулёзом лёгких повышен относительный риск выявления хронических вирусных гепатитов. Сочетание туберкулёза легких и хронических гепатитов В и С характеризуется: преимущественно слабовыраженными симптомами туберкулёзной интоксикации с отсутствием температурной реакции; малосимптомным течением гепатитов с повышенными уровнями АЛТ, АСТ и ГГТП; снижением вероятности раннего (до 3-х месяцев) прекращения бактериовыделения в 2 раза с относительным риском развития лекарственной устойчивости к этамбутолу и канамицину; снижением в 2,3 раза вероятности благоприятной рентгенологической картины при выписке из стационара. В условиях отсутствия явных клинических признаков сочетанной патологии (ТЛ + ХГ) возрастает роль дополнительных методов обследования (лабораторных, морфологических), которые важно учитывать в совокупности для разработки оптимальных подходов к лечению и прогнозу.
3. Факторами неблагоприятного течения туберкулёза лёгких у пациентов с сочетанной патологией являются: а) наличие ХГС или ХГВС в сравнении с ХГВ; б) слабовыраженный фиброз печени в сравнении с умеренным или выраженным; в) низкая степень морфологической активности гепатита в сравнении с умеренной или высокой; г) нормальные уровни АЛТ и АСТ в сравнении с повышенными; д) выраженный нейтрофилез в синусоидах и липофусциноз гепатоцитов в сравнении с отсутствием или слабой выраженностью этих параметров; е) уровень всех лимфоцитов менее 1000 в мкл и уровень CD4+ менее 400 клеток в мкл в сравнении с бóльшим их уровнем.
4. Внутривенная интермиттирующая химиотерапия имеет ряд преимуществ перед ежедневной: а) более частое закрытие полостей распада, б) отсутствие подавления монооксигеназной системы печени и редкое развитие токсических осложнений, в) отсутствие нарастания частоты вторичной ЛУ, а в случаях её появления – развитие в более поздние сроки.
5. Результатами иммуномодулирующего действия реаферона в комплексе с внутривенной интермиттирующей (2 раза в неделю) химиотерапией у больных туберкулезом с сопутствующими хроническими вирусными гепатитами являются: а) укорочение сроков прекращения бактериовыделения и закрытия полостей распада, б) снижение признаков цитолиза и холестаза, в) уменьшение морфологических проявлений специфического и неспецифического воспаления в лёгочной ткани.
Апробация работы. Материалы диссертации доложены и обсуждены на: 7 Российском съезде фтизиатров «Туберкулёз сегодня» (Москва, 2003), на международном конгрессе Европейского Респираторного Общества (Глазго, 2004), на международной конференции «Развитие международного сотрудничества в области изучения инфекционных заболеваний» (Новосибирск, 2004), на внутренней научно-практической конференции ННИИТ (Новосибирск, 2005), на заседании Ученого Совета ННИИТ (24 июня 2005), на международном конгрессе Европейского Респираторного Общества (Копенгаген, 2005), на областном обществе фтизиатров (г. Новосибирск, 31 мая 2006 г.), на международном конгрессе Европейского Респираторного Общества (Мюнхен, 2006), на II Российско-Германской конференции «Туберкулёз, СПИД, вирусные гепатиты» (Томск, 2007), на юбилейной межрегиональной научно-практической конференции «Современное здравоохранение: проблемы и перспективы» (Новосибирск, 2007).
Внедрение результатов исследования. Материалы диссертации, её выводы и рекомендации используются в учебном процессе кафедры туберкулёза факультета повышения квалификации и кафедры патологической анатомии Новосибирского государственного медицинского университета. Разработанная тактика ведения больных микст-инфекцией внедрена в клиническую практику работы клиник Новосибирского НИИ туберкулёза, Санкт-Петербургского НИИ фтизиопульмонологии, Екатеринбургского НИИ фтизиопульмонологии, специализированой туберкулезной больницы № 3 (г. Новосибирск).
Публикации. По теме диссертации опубликовано 45 печатных работ, в том числе 1 монография, 3 патента на изобретение, 11 статей в ведущих рецензируемых журналах.
Объем и структура диссертации. Работа состоит из введения, 4-х глав, включающих аналитический обзор литературы, описание методов исследования и характеристику больных, результаты собственных исследований и обсуждение полученных результатов, выводов, практических рекомендаций. Диссертация изложена на 232 страницах машинописного текста, включает в себя 58 таблиц и 32 рисунка. Указатель использованной литературы содержит 120 отечественных и 157 иностранных источников.
Личное участие автора. Работа выполнена на базе клиники Новосибирского НИИ туберкулёза (директор – профессор ), на кафедре патологической анатомии НГМУ (зав. кафедрой - акад. РАМН, профессор ), в Институте клинической иммунологии СО РАМН (директор – акад. РАМН, профессор ), ДИКБ № 3 г. Новосибирска (гл. врач – к. м.н. ), туберкулёзной больнице № 3 г. Новосибирска (гл. врач – ).
Автор самостоятельно собрал, статистически обработал и проанализировал все полученные данные. Проведенное клиническое исследование одобрено локальным этическим комитетом Новосибирского научно-исследовательского института туберкулёза Росмедтехнологий.
Автор выражает искреннюю благодарность коллегам по совместным исследованиям: доценту кафедры патологической анатомии НГМУ, д. м.н. , зав. лабораторией клинической иммунологии ИКИ СО РАМН, д. м.н., проф. , научному сотруднику лаборатории иммунологии ННИИТ, к. м.н. , врачам клинико-биохимической лаборатории ННИИТ, к. м.н. и , зав. отд. ДИКБ № 3 к. м.н. , сотрудникам ННИИТ и туберкулёзной больницы № 3 г. Новосибирска. Особую благодарность автор выражает своим учителям – проф. , проф. и научным консультантам – д. м.н., проф. , д. м.н., профессору .
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Характеристика пациентов, включенных в исследование, понятие показателя «плотности доз». Всего обследовано 566 больных, находившихся с различными формами туберкулёза лёгких в клинике ННИИТ и в туберкулёзной больнице № 3 г. Новосибирска в 2000 – 2007 гг.
На рисунке 1 схематично представлены этапы исследования.
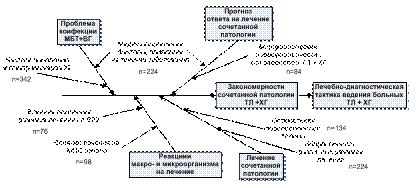 Рисунок 1. Схема исследования
Рисунок 1. Схема исследования
Структура исследования. На 1-м этапе исследования – решение проблемы коинфекции, вызванной возбудителями туберкулёза и вирусного гепатитаВ и/или С. Определяли частоту выявления и спектр диагностических маркеров HBV- и HCV-инфекции у 188-ми пациентов, последовательно поступавших в ННИИТ в 2002 – 2003 гг. и у 154-х больных, госпитализированных в туберкулёзную больницу № 3 г. Новосибирска в 2003 – 2004 гг. с разными сроками течения туберкулёза легких. К длительно болеющим ТЛ относили пациентов, срок диспансерного наблюдения которых во фтизиатрической службе составлял от 1 года и более.
Изучали медико-социальные факторы, обуславливающие неблагоприятное течение туберкулёза лёгких (у пациентов с хроническими вирусными гепатитами в сравнении с больными без гепатитов). Обследовали и проспективно наблюдали в клинике ННИИТ 224 больных, из них у 95-ти пациентов гепатитов не было (группа 1), у 129-ти выявлены хронические гепатиты В и С (группа 2): В (ХГВ) – у 58-ми больных, С (ХГС) – у 29-ти, В + С (ХГВС) – у 42-х. Больные с ХГВ были старше (36,3 ± 12,2 лет), чем с ХГС (26,6 ± 5,6 лет, р = 0,0003) и ХГВС (29,7 ± 8,7 лет, р = 0,005). Средний возраст пациентов, не имевших гепатита, составил 30,9 ± 11,2 лет. Пациентов в 1 группу отбирали методом случайных чисел. Критерии исключения: очаговый и фиброзно-кавернозный туберкулёз, казеозная пневмония, первичные формы туберкулёза, генерализованный туберкулёз, возраст пациентов менее 17 и более 70 лет.
На 2-м этапе исследования – оценка у больных с сочетанной инфекционной патологией связи морфологической активности патологических процессов в печени с иммунологическими характеристиками и ответом на противотуберкулёзную терапию. В течение первых 2-х недель нахождения в стационаре 84-м пациентам туберкулёзом легких с сопутствующими хроническими гепатитами В и С была выполнена пункционная биопсия печени. У этих пациентов определяли связи между клинико-биохимическими, морфологическими и иммунологическими показателями. Кроме того, сравнили результаты иммунологического обследования и стационарного лечения этих пациентов и 49-ти больных ТЛ, не имевших гепатитов. Группы не различались по полу, возрасту, формам туберкулёзного процесса.
На 3-м этапе исследования – изучение реакции макро - и микроорганизма на различные режимы противотуберкулёзной терапии. Проводили оценку состояния монооксигеназной системы печени больных с впервые выявленным ТЛ в процессе внутривенной интермиттирующей терапии в сравнении с ежедневным традиционным приемом противотуберкулёзных препаратов. Исследовали антипириновый тест в течение первых 2-х недель пребывания в клинике НИИ туберкулёза и спустя 6 месяцев у 47-ми пациентов группы интермиттирующего лечения (на фоне внутривенной терапии 2 раза в неделю) и у 52-х впервые выявленных больных группы ежедневного лечения.
Определяли частоту и сроки развития, спектр вторичной лекарственной устойчивости (ВЛУ) микобактерий туберкулёза (МБТ) у впервые выявленных больных ТЛ (в том числе с сопутствующими ХГ), получающих внутривенную интермиттирующую химиотерапию. Проанализировали данные теста лекарственной чувствительности микобактерий у 76-ти пациентов – бактериовыделителей с впервые выявленным ТЛ, поступавших на лечение в клинику Новосибирского НИИ туберкулёза в 2004 – 2005 гг. Противотуберкулёзную терапию до поступления в стационар все эти больные не получали. Отбор больных в группы ежедневного и интермиттирующего лечения проводили рандомизированно. Сроки наблюдения больных составили 5–14 месяцев. Внутривенную интермиттирующую химиотерапию с первых дней лечения назначали 38-ми пациентам (основная группа); ежедневный прием ПТП – 38-ми больным, которые составили группу сравнения. Больных с сопутствующими туберкулёзу ХГВ и/или ХГС в основной группе было 11, в группе сравнения – 8. ВЛУ микобактерий туберкулёза определяли исходно и через каждые 2 месяца от начала лечения. Сроки наблюдения больных составили от 5 до 14 месяцев (в течение всего времени пребывания в стационаре).
На 4-м этапе исследования – анализ результатов лечения туберкулёза лёгких у больных моно - и микст-инфекцией с учетом разных режимов химиотерапии (внутривенной интермиттирующей и ежедневной традиционной) и разработка оптимальной терапевтической тактики. Сведения о клиническом, биохимическом, рентгенологическом, бактериологическом, серологическом, биохимическом, иммунологическом, морфологическом динамическом обследовании 224-х пациентов в динамике на протяжении курса стационарного лечения заносили в статистическую таблицу SPSS. При последующем анализе применённых схем лечения оказалось, что не всем пациентам удалось закончить режим противотуберкулёзной терапии в том виде, в котором он был назначен. Так, у некоторых пациентов наблюдали развитие необратимых или тяжелых побочных реакций на лечение, заставлявших на какое-то время отменять ПТП с последующим постепенным подбором лекарств и доз. У ряда других больных в процессе лечения была выявлена лекарственная устойчивость МБТ, сопровождавшаяся клинико-рентгенологическими признаками прогрессирования болезни, заставлявшая пересматривать схемы и режимы лечения. Мы разделили количество дней лечения ПТП (количество доз) каждого пациента на количество койко-дней, проведенных им в клинике, и получили показатель, который назвали «плотность доз». Это позволило выделить из 224-х пациентов группу больных (Х), которых нельзя отнести ни к группе интермиттирующего (2 раза в неделю), ни к группе ежедневного лечения.
Пациенты с «плотностью доз» от 0,22 до 0,3 были отнесены к группе А: 128 человек (за весь период нахождения в стационаре они соблюдали схему лечения 2 раза в неделю); менее 0,22 и от 0,31 до 0,6 – к группе Х: 45 больных (схему лечения изменяли по причинам, перечисленным выше); от 0,61 и более – к группе Б: 51 пациент (прием препаратов 5 – 7 раз в неделю). Пациенты, не закончившие курс стационарного лечения (выписанные досрочно за нарушение режима; их койко-день был от 8 дней до 3 месяцев), исключены из анализа результатов противотуберкулёзной терапии.
Для разработки эффективной терапевтической тактики стационарного ведения больных туберкулёзом лёгких с сопутствующими хроническими гепатитами В и С оценили результаты лечения реафероном-ЕС в составе комплексной внутривенной интермиттирующей химиотерапии у 134-х больных ТЛ, у 92-х (68,7 %) из них – в сочетании с ХГ В и/или С. Отбор больных в группы сравнения проводили согласно критериям проспективного когортного исследования: 67 человек получали реаферон и составили I группу, а 67 пациентов II группы реаферон не получали. Курс лечения реафероном был 6 месяцев и более.
Для выявления признаков влияния интерферонотерапии на особенности тканевых реакций при туберкулезе легких были отобраны 34 пациента с инфильтративным ТЛ в фазе распада, у которых ранее был проведен предварительный 5–6-месячный курс терапии ПТП в сочетании с реафероном, после чего выполнено хирургическое резекционное лечение. На момент проведения операции у 25-ти пациентов данной группы легочный процесс был представлен туберкуломами, у 9-ти – фиброзно-кавернозным туберкулезом. Группу сравнения составили 35 прооперированных пациентов с подобными изменениями в лёгких (туберкуломы – у 25-ти человек, фиброзные каверны – у 10-ти человек), которые лечились в тех же условиях, но без реаферона. При подборе пациентов в группу сравнения стремились к соответствию всех параметров: пола, возраста, характера туберкулёзного процесса на момент оперативного вмешательства, этиологии хронического вирусного гепатита.
Объектом исследования служил операционный материал легких. Микроскопическому исследованию подвергали кусочки ткани из стенок каверн, капсул очагов и туберкулом, макроскопически неизмененных участков, исследовали бронх у места его пересечения по краю резекции. Использовали окраску гематоксилином и эозином, пикрофуксином по ван Гизону в комбинации с фукселином, окраску по Цилю–Нельсену на МБТ.
Для объективизации морфологической характеристики легочной ткани у пациентов сравниваемых групп гистологические препараты изучали, не имея на этот момент никакой информации о пациенте. Основные структурные компартменты легких оценивали с помощью разработанной нами совместно с д. м.н. схемы полуколичественной морфометрии:
1. Инкапсулированные зоны казеозного некроза (очаги и туберкуломы)
a. Зрелость капсулы: зрелая – 0 (преобладают фиброциты, плотное расположение пучков коллагена без лимфоцитарной инфильтрации, лимфоциты только вокруг капсулы в виде редких небольших скоплений), незрелая – 1 (преобладают фибробласты, пучки коллагена рыхлые, отечные, капсула диффузно инфильтрирована мононуклеарами)
b. Признаки специфического поражения капсулы: нет – 0, есть – 1 (участки казеоза структур капсулы)
c. Воспалительная инфильтрация ткани вокруг капсулы: минимальная продуктивная – 0, выраженная продуктивная – 1, экссудативная – 2
2. Ткань легкого на отдалении от очагов специфического воспаления
a. Признаки хронического бронхита: нет – 0, ремиссия – 1 (очаговая мононуклеарная инфильтрация перибронхиальной ткани без признаков эпителиотропизма), обострение – 2 (диффузный, часто муфтообразный характер перибронхиальной инфильтрации, значительная примесь плазмоцитов и нейтрофильных гранулоцитов среди клеток инфильтрата, признаки повреждения бронхиального эпителия, отек стромы)
b. Обструктивный характер бронхита: нет – 0, есть – 1 (наличие в просвете бронхов слизистого и/или гнойного экссудата, десквамированных эпителиоцитов)
c. Очаговая пневмония: нет – 0, есть – 1 (безвоздушные участки, экссудат в просвете альвеол, нейтрофильная инфильтрация межальвеолярных перегородок)
d. Интерстициально-десквамативная пневмония (очаговое или диффузное утолщение межальвеолярных перегородок за счет инфильтрации мононуклеарами, гиперплазия и десквамация в просвет альвеол альвеолярных макрофагов и альвеолоцитов 2 типа): нет – 0, минимальная – 1, умеренная/выраженная – 2
3. Туберкулез бронха: нет – 0, есть – 1 (любые признаки казеификации стенки бронха с повреждением его эпителия)
4. Пневмофиброз (избыточное отложение масс коллагена, пролиферация фибробластов разной степени зрелости)
a. Периваскулярный и перибронхиальный: нет или минимальный – 0, умеренный – 1, выраженный – 2
b. Интерстициальный (вне видимой связи с сосудами и бронхами): нет – 0, минимальный – 1, умеренный/выраженный – 2.
Объем обследования больных туберкулёзом лёгких. Сведения о всех пациентах, включенных в исследование, заносили в специальную таблицу. Они охватывали паспортные данные, анамнез, жалобы и объективные признаки заболевания, сопутствующие болезни, осложнения туберкулёзного процесса, результаты лабораторного и других методов исследования, характер лечения и его результаты. Динамику клинических симптомов болезни оценивали на основании данных анамнеза и результатов ежедневных клинических осмотров обследуемых пациентов.
Рентгенологическое исследование включало обзорную рентгенографию органов грудной клетки в двух проекциях, прицельную томографию зоны воспалительной реакции лёгочной ткани, по показаниям выполняли цифровую томографию и компьютерную томографию органов грудной клетки. Рентгенологический контроль динамики туберкулёзного процесса осуществляли ежемесячно. «Распространённым» считали туберкулёзный процесс, охватывающий 3 и более сегментов лёгких.
Бактериологическое исследование включало посевы мокроты на МБТ и люминесцентную микроскопию, которые выполняли трёхкратно при поступлении и двукратно ежемесячно в процессе проведения противотуберкулёзной терапии. Пациентам с бактериовыделением определяли тест лекарственной чувствительности МБТ ко всем противотуберкулёзным препаратам (1-го и 2-го ряда) и это исследование повторяли каждые 2 месяца в случае сохранения бактериовыделения на фоне проводимой химиотерапии.
Такой тщательный контроль позволил выявить первичную лекарственную устойчивость и констатировать появление вторичной лекарственной устойчивости МБТ, установить момент прекращения бактериовыделения, стойкость негативации мокроты, судить о времени закрытия полостей распада и рентгенологической динамике в сравниваемых группах.
Объем обследования для диагностики вирусного гепатита. Гепатиты у больных выявляли в процессе специального обследования, включавшего анамнез, жалобы, объективный осмотр, исследование биохимического анализа крови, ультразвуковое исследование органов брюшной полости, метод иммуноферментного анализа, позволявший выявлять маркёры гепатита В (HBsAg, aHBs, aHBcIgG, aHBcIgM, HBeAg, aHBeIgG), гепатита С (aHCV сумм., aHCVIgM, aHCVcoreIgG, aHCVNS3IgG, aHCVNS4, aHCVNS5), гепатита D (aHDV сумм), полимеразную цепную реакцию крови и ткани печени, забираемой при пункционной биопсии, морфологическое исследование биоптатов печени.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |




