По частоте обострений в год пациентов разделили на 2 группы, сходные по поло-возрастному составу и длительности анамнеза. Первую группу составили пациенты с количеством рецидивов от 6 до 11 раз в год (n = 21), вторую — больные с непрерывно рецидивирующим течением заболевания (12 и более обострений в год; n = 28). У пациентов сравниваемых групп изменения параметров НСТ-теста были однонаправленными (повышение НСТб по сравнению с контролем; р = 0,02 и р = 0,005 соответственно) (рисунок 2). Однако степень изменения значений НСТб у больных с количеством рецидивов от 6 до 11 в год была значимо выше, чем у лиц с большей частотой рецидивов (170 и 100 % соответственно, р = 0,02).
При сопоставлении значений НСТб в группах больных, разделенных по длительности анамнеза (1–10 лет и более 10 лет), а также по наличию или отсутствию дисбиоза кишечника, различий между сравниваемыми группами не обнаруживалось.
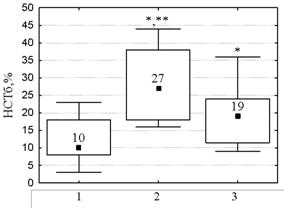
Рисунок 2 — Показатели базальной кислородпродуцирующей активности нейтрофилов
у больных ХРГИ с различной частотой рецидивов в год
Примечание: данные представлены в виде Ме: 25%; 75%; Min-Max.
1 — контрольная группа, 2 — 6–11 обострений в год, 3 — более 12 обострений в год
* различие значимо в сравнении с аналогичным показателем контрольной группы;
** различие статистически значимо между показателями в группах больных ХРГИ
Корреляционный анализ по Спирмену подтвердил полученные результаты. Мы обнаружили наличие обратной взаимосвязи умеренной силы между значениями НСТб и частотой обострений герпетической инфекции (rs = –0,34; р = 0,03). В то же время корреляций НСТб с длительностью анамнеза и наличием дисбиоза у больных ХРГИ не выявлено.
Известно, что наиболее значимым в клинической практике является не сравнение групповых показателей, а характеристика отклонений параметров конкретных пациентов относительно нормы. Индивидуальный анализ значений НСТб у обследованных нами пациентов позволил обнаружить значительную разнонаправленность изменений показателей кислородпродуцирующей активности нейтрофилов. Так, среди больных, обследованных в обострении ХРГИ, у 9 пациентов НСТб был в пределах нормативных величин, а у 15 больных превышал контрольные значения (на 99 %, р = 0,006). В ремиссии заболевания у 23 пациентов НСТб не выходил за диапазон нормы, но у 26 человек был значительно выше значений здоровых лиц (на 170 %, р = 0,001).
Мы провели сравнительный анализ параметров липопероксидации в группах больных с нормальными и повышенными значениями НСТб. При этом у пациентов с обострением ХРГИ на фоне повышения НСТб отмечался более низкий уровень конечных продуктов окисления нейтральных липидов эритроцитов (ОШэ/г, р = 0,034), чем у лиц с нормальными значениями НСТб. У пациентов в ремиссии заболевания повышение НСТб сопровождалось более низкими значениями КД п/и относительно пациентов, у которых НСТб не изменялся (р = 0,04). По содержанию других продуктов липопероксидации в крови больные с наличием или отсутствием реакции со стороны НСТб не различались.
Результаты проведенных исследований показали, что повышение базальной активности нейтрофилов у больных ХРГИ сопровождается снижением показателей ПОЛ крови. Данный факт подтвержден путем анализа взаимосвязей между параметрами НСТ-теста и показателями липопероксидации по методу Спирмена (рисунок 3).

Рисунок 3 — Характер взаимосвязей показателей функциональной активности нейтрофилов
и параметров липопероксидации у больных ХРГИ и здоровых лиц
Как видно на рисунке 3, в контрольной группе обнаруживалась прямая положительная корреляция между НСТб↔ДКп/г, а также отрицательная взаимосвязь НСТст↔ОШ э/и. У больных ХРГИ взаимосвязи между параметрами НСТ-теста и ПОЛ носили только отрицательный характер, причем различались в зависимости от стадии заболевания. У пациентов в ремиссии заболевания обнаружены взаимосвязи НСТб с показателями ДКп/и и ОШ п/и, а у пациентов в обострении ХРГИ – корреляция между НСТст и ОШэ/г.
Таким образом, результаты проведенной работы показали, что повышение базальной кислородпродуцирующей активности нейтрофилов, характерное для больных ХРГИ тяжелого течения, обратно коррелирует с интенсивностью ПОЛ. Дальнейшие исследования в этом направлении позволят решить вопрос о механизмах такой активации, а также представляют интерес в плане возможностей использования параметров НСТ-теста и ПОЛ для мониторинга заболевания.
Выводы
1. У больных с тяжелой формой хронической рецидивирующей герпетической инфекции кожи (ХРГИ) как в обострении, так и в ремиссии заболевания наблюдается активация перекисного окисления липидов, что проявляется повышением первичных, промежуточных и конечных продуктов липопероксидации. Степень увеличения содержания конечных продуктов окисления фосфолипидов эритроцитов у больных в ремиссии заболевания значимо выше, чем в обострении.
2. У больных тяжелой формой хронической рецидивирующей герпетической инфекции наблюдается дисбаланс между интенсивностью липопероксидации в плазме и эритроцитах. При этом накопление конечных продуктов окисления фосфолипидов превалирует в эритроцитах, тогда как нейтральных липидов — в плазме.
3. У больных ХРГИ независимо от стадии заболевания (ремиссия-обострение) наблюдается повышение базальной кислородпродуцирующей активности нейтрофилов по результатам НСТ-теста. Степень изменения данного параметра снижается по мере увеличения частоты рецидивирования.
4. Обнаружены отрицательные взаимосвязи (rs = –0,50–0,67) между показателями кислородпродуцирующей активности нейтрофилов и перекисного окисления липидов у лиц с герпесвирусной инфекцией.
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
1. Каримова, И. Н. Герпесвирусная инфекция. Диагностика, клиника, лечение / . — М.: Медицинское информационное агентство, 2004. — С. 44–72.
2. Малышева, О. А. Состояние вегетативной нервной и иммунной систем у инфицированных вирусом простого герпеса / , // Эпидемиология и инфекционные болезни. — 2001. — № 3. — С. 37–40.
3. Дидковский, Н. А. Герпетическая инфекция тяжелого течения / , // Терапевтический архив. — 2007. — № 11. — С. 52–57.
4. Кудин, А. П. Роль Herpes simplex в патологии человека. Ч. I. Этиология, патогенез, состояние иммунитета / , // Медицинские новости. — 2004. — № 5. — С. 11–14.
5. Шанин, Ю. И. // Антиоксидантная терапия в клинической практике / , , . — СПб., 2003. — 128 с.
6. Волчегорский, И. А. Сопоставление различных подходов к определению продуктов перекисного окисления липидов в гептан-изопропанольных экстрактах крови / , // Вопр. мед. химии. — 1989. — Т. 35, № 1. — С. 127–130.
7. Новикова, И. А. Взаимосвязь степени окисленности плазмы и мембран эритроцитов в условиях активации свободнорадикального окисления / , // Вес. Нац. акад. навук Беларусi. Сер. Мед. навук. — 2010. — № 3. — С. 70–74.
8. Региональные показатели субпопуляционного состава лимфоцитов здоровых жителей Гомельской области / и [др.] // Медико-биологические проблемы жизнедеятельности. — 2010. — № 3. — С. 67–74.
9. Дидковский, Н. А. Актуальные вопросы тяжелой герпетической инфекции у взрослых / , // Лечащий врач. — 2006. — № 2. — С. 4–11.
10. Комплексная лабораторная оценка иммунного статуса: учеб.-метод. пособие для практ. занятий с врачами клин. лаб. диагностики / [и др.]. — Витебск, 2003. — 39 с.
11. Biron, С. A., Brossay, L. NK cells and NKT cells in innate defense against viral infections // Curr. Opin. Immunol. — 2001. — Vol. 13. — P. 458–464.
12. A proinflammatory peptide from herpes simplex virus type 2 glycoprotein G affects neutrophil, monocyte, and NK cell functions / L. Bellner [et al.] // J. Immunol. — 2005. — Vol. 174(4). — P. 2235–2241.
13. Gordon, S. Alternative activation of macrophages // Nat. Rev. Immunol. — 2003. — Vol. 3. — P. 23–35.
Поступила 10.12.2010
УДК 616.345+616.351-006.5
ТАКТИКА ВЕДЕНИЯ ПАЦИЕНТОВ С КОЛОРЕКТАЛЬНЫМИ ПОЛИПАМИ
,
Республиканский научно-практический центр
радиационной медицины и экологии человека, г. Гомель
Гомельский государственный медицинский университет
Анализ публикаций последних лет свидетельствует о тенденции к неуклонному росту заболеваемости колоректальным раком во всем мире. По данным ВОЗ, в мире ежегодно регистрируется более 500 тыс. случаев этой болезни. В структуре онкологической заболеваемости колоректальный рак прочно занимает второе-третье место как у мужчин, так и у женщин и второе место среди причин смерти от онкопатологии в большинстве экономически развитых стран.
Известно, что большинство колоректальных опухолей развивается из аденоматозных полипов. Последовательность «аденома – рак» подтверждена многочисленными исследованиями, и хотя не каждая аденома трансформируется в рак, такая вероятность существует у значительного числа данных новообразований. В связи с этим своевременная эндоскопическая диагностика и удаление аденоматозных полипов прямой и толстой кишки являются эффективным методом профилактики колоректального рака.
Ключевые слова: полип, аденома, колоноскопическая полипэктомия, малигнизированный полип.
TACTICS OF CARE AFTER PATIENTS WITH RECTAL POLYPI
А. D. Borsuk, Е. G. Malaeva
Republican Research Center for Radiation Medicine and Human Ecology, Gomel
Gomel State Medical University
The analysis of the late publications is evidence of the tendency to the rising rectal cancer incidence in the whole world. According to the data of World Health Organization every year more than 500 thousand cases of this disease are registered in the world. In the structure of oncologic incidence rate rectal cancer takes the second-third place in both men and women and goes second among the oncopathology death reasons in the majority of economically developed countries.
The adenomatous polypi are known to develop the majority of rectal neoplasms. The chain «adenoma – cancer» has been proved by numerous researches and though not every adenoma tranforms into cancer, this is possible in a considerable number of the present neoplasms. In connection with this, the endoscopic diagnosis and ablation of adenomatous polypi of rectum and large intestine are effective methods of rectal cancer prophylaxis.
Key words: polypus, adenoma, colonoscopic polypectomy, malignant polypus.
Введение
Полипом называется любое видимое возвышение над поверхностью слизистой оболочки, связанное с ней ножкой или широким основанием. Гистологически колоректальные полипы классифицируют на опухолевые и неопухолевые (таблица 1).
Таблица 1 — Классификация колоректальных полипов
Опухолевые полипы | Неопухолевые полипы | |
эпителиальные | неэпителиальные | |
Аденома — тубулярная — тубуловорсинчатая — ворсинчатая | Лейомиома Липома Гемангиома | Гиперпластический Воспалительный Слизистый Гамартома: — синдром Пейтца-Егерса — ювенильный полипоз |
Тактика при обнаружении колоректальных полипов должна быть основана на совокупности данных, включающих клинические проявления, локализацию и гистологическое строение.
Диагностика и наблюдение
Колоректальные полипы часто диагностируются у бессимптомных лиц при проведении скрининговых осмотров или когда исследование проводится по другим причинам (например, желудочно-кишечное кровотечение). Полипы могут быть обнаружены во время эндоскопического исследования (ректороманоскопия или колоноскопия) или рентгенологически (ирригоскопия).
Из всей большой группы колоректальных полипов клинически значимыми являются аденомы, так как возможна их малигнизация. Классически предполагается, что злокачественный потенциал аденом коррелирует с их типом, размером и степенью дисплазии. Увеличение процента ворсинчатого компонента в ткани полипа, размеры больше 1 см и более высокие степени дисплазии повышают риск злокачественной трансформации. В настоящее время общепринято считать, что солитарные аденомы являются факультативным, а диффузный аденоматоз — облигатным предраковым заболеванием [1]. Многочисленные исследования доказывают, что колоноскопическое удаление аденоматозных полипов значительно снижает риск развития колоректального рака [2]. В отличие от аденом гиперпластические, воспалительные, гамартомные полипы не имеют риска малигнизации.
При обнаружении небольших полипов (меньше 1 см) при ректороманоскопии выполняется биопсия с последующим морфологическим исследованием. Если размер полипа превышает 1 см, биопсия обычно не требуется, так как пациенту необходима колоноскопическая полипэктомия. Если гистологическое строение полипа, обнаруженного при ректороманоскопии, соответствует аденоме, пациенту необходимо проведение колоноскопии.
При колоноскопии аденома, обнаруженная во время ректороманоскопии, удаляется и проводится осмотр проксимальных отделов толстой кишки на предмет обнаружения синхронных аденом или других опухолевых поражений. Несколько исследований доказали повышенный риск развития проксимальных синхронных образований у пациентов с дистальными аденомами. В проспективном исследовании бессимптомных лиц с повышенным риском развития колоректального рака выявлено, что у 31 % наряду с доброкачественной дистальной аденомой, выявленной при ректороманоскопии, были обнаружены проксимальные синхронные неоплазии, в том числе у 8 % — прогрессирующие аденомы (размер больше 1 см, ворсинчатые, с умеренной или выраженной степенью дисплазии) и инвазивные карциномы [3]. Другое исследование бессимптомных лиц с повышенным риском развития колоректального рака выявило, что у 42 % из них с диагностированными ранее во время ректороманоскопии дистальными аденомами при тотальной колоноскопии обнаружены проксимальные синхронные аденомы [4].
Некоторые исследователи, однако, ставят под сомнение необходимость проведения колоноскопии лицам, у которых были выявлены небольшие (меньше 1 см) аденомы во время ректороманоскопии. При исследовании пациентов, которым проводилась колоноскопия после выявления одной или нескольких тубулярных аденом небольших размеров (1 см и меньше) во время ректороманоскопии, проксимальные синхронные аденомы с прогрессирующим течением составили менее 1 % [5]. Другое исследование показало, что у пациентов с бессимптомным течением заболевания и размером единичной тубулярной аденомы меньше 1 см, отсутствием родственников первой линии родства с колоректальным раком в анамнезе риск развития проксимальной синхронной аденомы или инвазивного рака составляет около 3 %, что соответствует риску развития данного заболевания в общей популяции [6]. Длительное наблюдение пациентов, которым проводилась ректороманоскопия без колоноскопии и были удалены тубулярные аденомы (одна или несколько) небольших размеров (меньше 1 см) со слабой или умеренной степенью дисплазии, выявило, что пациенты имели риск развития колоректального рака, сопоставимый с общей популяцией [7].
Таким образом, утверждение, что пациенты с выявленными во время ректороманоскопии дистальными тубулярными аденомами небольших размеров нуждаются в проведении колоноскопии и последующем наблюдении, является спорным. В настоящее время рекомендуется проведение колоноскопии и последующее наблюдение данной категории пациентов с более длительными интервалами (например, один раз в 5 лет).
Считается, что для динамического наблюдения за колоректальными полипами колоноскопия предпочтительнее ирригоскопии. И хотя ирригоскопия легче переносится пациентами и имеет меньше осложнений, колоноскопия является более информативным исследованием, позволяет выполнить биопсию для морфологической верификации и удалить полипы.
Колоноскопическая полипэктомия
При колоноскопии все полипы должны быть полностью удалены. Впрочем, есть обстоятельства, например, тяжелая сопутствующая патология, ожидаемая небольшая продолжительность жизни пациента, которые исключают необходимость удаления случайно обнаруженных полипов во время диагностической колоноскопии.
При обнаружении полипов и выполнении полипэктомии весь материал должен извлекаться и направляться на морфологическое исследование.
Наиболее часто используемые методы колоноскопической полипэктомии — петлевая электроэксцизия, коагуляция с помощью щипцов для «горячей» биопсии, биопсия без коагуляции.
Петлевая полипэктомия применяется при удалении полипов как на ножке, так и на широком основании и включает накидывание петли на полип с последующей электрокоагуляцией и срезанием. Небольшие полипы на широких основаниях в дистальных отделах толстой кишки, как правило, удаляются с помощью щипцов для «горячей» биопсии. При этом методе полип осторожно оттягивается от стенки кишки, чтобы не вызвать перфорацию и коагулируется. Ткань полипа в чашечках щипцов изолирована от теплового воздействия и поэтому может быть направлена на гистологическое исследование. Небольшие полипы на широком основании могут быть удалены методом биопсии без коагуляции. Такой метод особенно предпочтителен при небольших полипах в проксимальных отделах толстой кишки, когда биопсия с коагуляцией может осложняться постполипэктомическими кровотечениями.
Крупные полипы на широком основании представляют собой более сложную задачу для специалиста. В определенных условиях такие полипы могут удаляться в несколько этапов с помощью петлевой электроэксцизии. Существует методика с использованием физиологического раствора для облегчения полипэктомии при крупных полипах на широком основании. При такой методике перед тем как провести петлевую полипэктомию, производится инъекция раствора под основание полипа, чтобы приподнять его и отделить от стенки кишки. Инъекция физиологического раствора создает защитный слой, что уменьшает риск перфорации. Крупные полипы на широком основании, при эндоскопическом удалении которых высок риск осложнений, удаляются с помощью хирургической резекции.
Колоноскопические полипэктомии являются безопасным методом с достаточно низким числом осложнений. Перфорации или массивные кровотечения наблюдаются примерно в 0,1–0,2 % случаев.
Постполипэктомическое наблюдение
После удаления одного или нескольких аденоматозных полипов обычно рекомендуется эндоскопический мониторинг, чтобы снизить риск развития колоректального рака. Исследования показали, что после удаления всех аденом на всем протяжении толстой кишки следующую колоноскопию можно смело отложить на три года [8]. В этих исследованиях участвовали 1418 случайно отобранных пациентов после колоноскопического удаления всех аденом с последующими контрольными колоноскопиями от одного до трех лет или только через три года. Не было никакой разницы (3,3 % в обеих группах) в обнаружении аденом с прогрессирующим течением.
После колоноскопического удаления всех аденом с тяжелой дисплазией (рак in situ или внутрислизистый рак) рекомендуется трехлетний интервал наблюдения. Гистологические исследования аденоматозных полипов показали, что лимфатические сосуды не проникают выше уровня мышечной пластинки слизистой оболочки [9]. В связи с этим полипы с тяжелой дисплазией эпителия в пределах слизистой оболочки не имеют риска метастазирования в регионарные лимфатические узлы. Последующее наблюдение за пациентами, которым производилось колоноскопическое удаление таких полипов, не выявило неблагоприятных исходов [10].
В отдельных случаях, когда были удалены не все аденомы или удалялись очень большие полипы на широких основаниях, или был некачественный осмотр из-за плохой подготовки кишки, проведение контрольных колоноскопий рекомендуется в более ранние сроки.
Малигнизированные полипы
Малигнизированным колоректальным полипом считается аденома, которая содержит инвазивный рак, представленный злокачественными клетками, проникающими через мышечную пластинку слизистой оболочки в подслизистый слой [11]. Более ранние исследования показали, что примерно 5 % эндоскопически удаленных аденом являются малигнизированными [12], однако данные последующих исследований говорят, что эта цифра не превышает 2 % [8].
Малигнизированные полипы могут быть на ножке или широком основании. Хотя их внешний вид может не отличаться от доброкачественных полипов, имеются признаки, позволяющие предположить малигнизацию: неровная поверхность полипа, изъязвления, плотность при инструментальной «пальпации», широкая или деформированная ножка, повышенная ранимость и кровоточивость слизистой оболочки.
В отличие от аденомы с высокой степенью дисплазии раковые клетки малигнизированного полипа уже не ограничиваются слизистой оболочкой, поэтому есть вероятность метастазирования. По этой причине после колоноскопического удаления малигнизированного полипа решается вопрос о необходимости хирургического вмешательства. Это решение основывается на определении риска в связи с вероятностью оставления ткани опухоли в месте удаленного полипа и метастазов в лимфатические узлы по сравнению с хирургическим риском лапаротомии и резекции кишки.
При решении вопроса о необходимости хирургической операции после колоноскопического удаления малигнизированного полипа надо руководствоваться несколькими прогностическими критериями. Благоприятными прогностическими критериями являются высоко - или умереннодифференцированная аденокарцинома, отсутствие инвазии в лимфатические или кровеносные сосуды, отсутствие злокачественных клеток в краях резекции (включая края ножки у полипов на ножке) и эндоскопические признаки полного удаления. Неблагоприятные прогностические критерии включают в себя низкодифференцированную аденокарциному, инвазию в лимфатические и (или) кровеносные сосуды, наличие злокачественных клеток вблизи краев резекции и эндоскопические признаки неполного удаления. Наиболее распространенным неблагоприятным критерием является наличие злокачественных клеток на уровне или вблизи краев резекции [13].
Исследования показали, что риск резидуального рака или риск метастазирования в лимфатические узлы в полипах с благоприятными прогностическими критериями составил 0,3 % в полипах на ножке и 1,5 % в полипах на широком основании [13]. Смертность при выборе хирургического лечения составила примерно 1–2 %, однако операционный риск может быть ниже у молодых пациентов и выше — у пожилых с тяжелой сопутствующей патологией.
Учитывая, что после колоноскопического удаления малигнизированных полипов на ножке с благоприятными прогностическими критериями риск оперативного вмешательства выше, чем риск развития резидуального рака или риск метастазирования в лимфатические узлы, хирургическая операция, как правило, не показана. Однако вопрос о проведении операции может рассматриваться в случаях, когда пациент молодого возраста и риск хирургического вмешательства невысок и когда нельзя исключить даже минимальную вероятность метастазирования или развития резидуального рака. В противоположность этому после колоноскопического удаления малигнизированного полипа на ножке с неблагоприятными прогностическими критериями пациенту необходимо хирургическое вмешательство.
Нет единого мнения о выборе тактики ведения пациентов с малигнизированными полипами на широком основании. Одни специалисты рекомендуют хирургическое вмешательство при всех малигнизированных полипах на широком основании, даже если для них характерны благоприятные прогностические критерии, так как считают, что широкое основание само по себе увеличивает риск развития резидуального рака [14, 15]. Другие считают, что нет доказательств того, что во всех случаях широкое основание является абсолютным показанием к хирургическому вмешательству. Исследования показали, что малигнизированные полипы с благоприятными прогностическими критериями, будь они на ножке или на широком основании, не отличаются по степени риска метастазирования в лимфатические узлы или развития резидуального рака [16]. Это позволяет сделать вывод, что небольшие полипы на широком основании с благоприятными прогностическими критериями имеют низкую вероятность злокачественной инвазии и поэтому не требуют этапного колоноскопического удаления или хирургического вмешательства.
Считается, что при малигнизированных полипах на широком основании с благоприятными прогностическими критериями колоноскопическая полипэктомия является адекватным лечением для большинства пациентов, однако решение должно приниматься индивидуально для каждого из них. При малигнизированных полипах на широком основании с неблагоприятными прогностическими критериями тактика такая же, как и при малигнизированных полипах на ножке. При колоноскопии, когда обнаружен полип и есть подозрение на его малигнизацию, врач-эндоскопист в первую очередь оценивает, является ли он резектабельным эндоскопически или нет. Полипы на ножке или небольшие полипы на широком основании могут быть полностью удалены, однако большой полип на широком основании должен быть подвергнут биопсии. После удаления полипа вся ткань должна направляться на патоморфологическое исследование. Локализация полипа должна быть точно отражена в медицинской документации, так как в случае, если он окажется малигнизированным и будут определены неблагоприятные прогностические критерии, может быть необходима хирургическая резекция. При колоноскопической полипэктомии в местах удаленных полипов можно вводить тушь в стенку кишки с целью создания постоянных меток для определения уровня резекции в случае хирургического вмешательства.
Одной из центральных фигур, определяющих тактику лечения пациентов с малигнизированными колоректальными полипами, является врач-морфолог, который должен иметь четкие представления о последствиях постановки того или иного диагноза. Для повышения точности патоморфологического диагноза рациональным является получение заключения от двух и более независимых специалистов или заключение их консилиума.
После колоноскопического удаления малигнизированных полипов с благоприятными прогностическими критериями следующая колоноскопия проводится, как правило, через 3–6 месяцев, чтобы оценить радикальность удаления, особенно если полип был на широком основании. При обнаружении резидуального рака пациента направляют на резекцию, если нет противопоказаний к операции. Если резидуального рака нет, следующая колоноскопия выполняется через один год и при отрицательном результате может быть повторена через три года.
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
1. Федоров, В. Д. Диффузный полипоз толстой кишки / В. Д. Федоров, . — М.: Медицина, 1991. — 120 с.
2. Winawer, S. J. Prevention of colorectal cancer by colonoscopic polypectomy / S. J. Winawer, A. G. Zauber, M. N. Ho // N Engl J Med. — 1993. — Vol. 329. — P. 1977–1981.
3. Read, T. E. Importance of adenomas 5 mm or less in diameter that are detected by sigmoidoscopy / T. E. Read, J. D. Read, L. F. Butterly // N Engl J Med. — 1997. — Vol. 336. — P. 8–12.
4. Lieberman, D. A. Screening for colon malignancy with colonoscopy / D. A. Lieberman, F. W. Smith // Am J Gastroenterol. — 1991. — Vol. 86. — P. 946–951.
5. Zarchy, T. M. Do characteristics of adenomas on flexible sigmoidoscopy predict advanced lesions on baseline colonoscopy? / T. M. Zarchy, D. Ershoff // Gastroenterology. — 1994. — Vol. 106 — P. 1501–1504.
6. Grossman, S. Colonoscopic screening of persons with suspected risk factors for colon cancer. II: Past history of colorectal neoplasms / S. Grossman, M. L. Milos, I. S. Tekawa // Gastroenterology. — 1989. — Vol. 96. — P. 299–306.
7. Atkin, W. S. Long-term risk of colorectal cancer after excision of rectosigmoid adenomas / W. S. Atkin, B. C. Morson, J. Cuzick // N Engl J Med. — 1992. — Vol. 326. — P. 658–662.
8. Winawer, S. J. Randomized comparison of surveillance intervals after colonoscopic removal of newly diagnosed adenomatous polyps / S. J. Winawer, A. G. Zauber, M. J. O’Brien // N Engl J Med. — 1993. — Vol. 328. — P. 901–906.
9. Fenoglio, C. M. Distribution of human colonic lymphatics in normal, hyperplastic, and adenomatous tissue: Its relationship to metastasis from small carcinomas in pedunculated adenomas, with two case reports / C. M. Fenoglio, G. I. Kaye, N. Lane // Gastroenterology. — 1973. — Vol. 64. — P. 51–66.
10. Haggitt, R. C. Prognostic factors in colorectal carcinomas arising in adenomas: Implications for lesions removed by endoscopic polypectomy / R. C. Haggitt, R. E. Glotzbach, E. E. Soffer // Gastroenterology. — 1985. — Vol. 89 — P. 328–336.
11. Белоус, Т. А. Патоморфология предраковых состояний толстой кишки / // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2002. — № 4. — С. 50–55.
12. Wolff, W. I. Definitive treatment of «malignant» polyps of the colon / W. I. Wolff, H. Shinya // Ann Surg. — 1975. — Vol. 182 — P. 516–525.
13. Cranley, J. P. When is endoscopic polypectomy adequate therapy for colonic polyps containing invasive carcinoma? / J. P. Cranley, R. E. Petras, W. D. Carey // Gastroenterology. — 1986. — Vol. 91 — P. 419–427.
14. Williams, C. B. Practical aspects of endoscopic management of malignant polyps / C. B. Williams, J. E. Whiteway, J. R. Jass // Endoscopy. — 1987. — Vol. 19. — P. 31–37.
15. Wilcox, G. M. Early invasive cancer in adenomatous colonic polyps («malignant polyps»): Evaluation of the therapeutic options by decision analysis / G. M. Wilcox, J. R. Beck // Gastroenterology. — 1987. — Vol. 92. — P. 1159–1168.
16. Ehrinpreis, M. N. Management of the malignant polyp / M. N. Ehrinpreis, J. L. Kinzie, R. Jaszewski // Gastroenterol Clin North Am. — 1988. — Vol. 17. — P. 837–850.
Поступила 06.12.2010
УДК 616.1-003.96-053.2-07:796.071
ЗНАЧЕНИЕ ГАРВАРДСКОГО СТЕП-ТЕСТА В ОЦЕНКЕ АДАПТАЦИОНЫХ
ВОЗМОЖНОСТЕЙ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ У ДЕТЕЙ-СПОРТСМЕНОВ
,

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 |




