В том случае, когда более эффективный метод являлся более дорогим, выявить доминантный метод лечения не удавалось, проводился инкрементальный анализ, который позволял определить прибавленную стоимость (incremental cost), т. е. стоимость дополнительных преимуществ более дорогого метода.
Расчет в данном случае проводился по формуле:
CEAΔ = (DC1 - DC2) / (Ef1 - Ef2), где:
CEAΔ – соотношение дополнительных затрат и эффективности;
DC1 – прямые затраты первого метода лечения;
DC2 - прямые затраты второго метода лечения;
Ef1 – эффективность первого метода лечения;
Ef2 - эффективность второго метода лечения.
Последующее сравнение полученных результатов позволяло определить наиболее экономически предпочтительный метод.
Прямые медицинские затраты: подсчет затрат на повторные госпитализации больного осуществлялся по формуле: (стоимость койко-дня х число дней госпитализации) + тариф на дополнительные методы исследования и тарифицированные методы лечения; затраты на амбулаторный визит к врачу.
Учет прямых медицинских затрат, отражающих расходы на приобретение необходимого количества препаратов в аптечной сети, выражался в произведении средней стоимости 1 таблетки, среднесуточной дозы препарата длительности назначения.
Прямые немедицинские затраты: расходы пациента в связи с пребыванием в стационаре, транспортные расходы; транспортные расходы при амбулаторных визитах. Размеры затрат оценивались по опросам пациентов с ИБС, подвергшихся реваскуляризации миокарда, обратившихся за стационарной и амбулаторной помощью в 2009 году.
Непрямые затраты: оплата дней нетрудоспособности пациенту и производственные потери, связанные с временным отсутствием на работе
Стоимостное выражение для подсчета прямых и непрямых затрат калькулировалось исходя из данных МЭС РФ, ТФОМС и по данным Госкомстата РФ на 31.12.09. Информация обо всех категориях затрат служила основой для построения базы данных (в формате документа Excel) и дальнейшего статистического анализа результатов исследования.
Статистический анализ производился с помощью программ «STATISTICA 6.0» (StatSoft, USA) и «Microsoft Office Excel 2007». Обработка результатов исследования проводилась методами параметрической и непараметрической статистики (, 2002). Характер распределения данных оценивался критериями Колмогорова-Смирнова и Шапиро-Уилкса. В случае если распределение признака принималось приближенно нормальным, результаты представлялись в виде (M±m), где М – среднее арифметическое значение, m – стандартная ошибка среднего значения, для анализа использовался параметрический критерий (Т-критерий Стьюдента). При характере распределения результатов отличном от нормального, анализ проводился с помощью методов непараметрической статистики. С целью проверки гипотезы о различии средних для трех и более изучаемых групп использовался непараметрический метод Фридмана ANOVA или критерий Вилкоксона. Качественные переменные описывались абсолютными и относительными (%) частотами. За уровень статистической значимости различий показателей принималась величина p < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ.
Результаты проспективного открытого рандомизированного сравнительного клинико-экономического исследования.
Реваскуляризация миокарда – широкое понятие, включающее как операцию КШ, так и различные виды ТЛБАП с КС на коронарных артериях. Цель реваскуляризации - улучшение прогноза (профилактика ИМ и внезапной смерти, уменьшение или полная ликвидация симптомов).
Нам удалось проследить судьбу 1074 пациентов, подвергшихся КШ и ТЛБАП с КС в период с 2000 по 2007 гг. Срок наблюдения составил 36 месяцев, который учитывал промежуток времени от начала и до конца испытания или до момента наступления неблагоприятного события для каждого конкретного больного в течение периода наблюдения. Мы оценили в качестве неблагоприятного события все случаи сердечно-сосудистой летальности, нефатальные инфаркты миокарда, инсульты, эпизоды нестабильной стенокардии, повторные оперативные вмешательства на коронарных артериях. Анализ наших данных указывает на лучший прогноз у пациентов с КШ, по сравнению с ТЛБАП с КС. Вероятность благоприятного исхода при КШ составила 91,9%, при ТЛБАП с КС только 77,4%, отличие в 14,5% оказались высоко достоверными (p<0,002) с учётом критерия Уилкоксона. Относительный риск (ОР) в группе ТЛБАП с КС составил 2,79 при 95% доверительном интервале (ДИ) 2,04 - 3,84 (p<0,05), по сравнению с результатами КШ.
14,5% (p<0,002) ОР 2,798 при 95% ДИ 2,04-3,84 ТЛБАП 22,62% КШ 8,1%
![]()
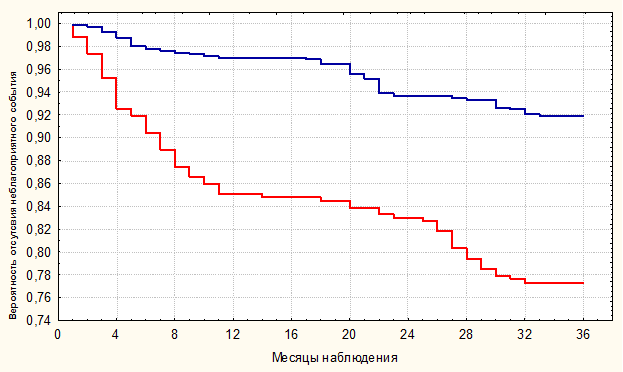
Рисунок 1. Вероятность развития неблагоприятных исходов в группах наблюдения
Проведя сравнительный анализ затратной эффективности в исследуемых группах (в качестве положительных результатов рассматривалось отсутствие летальных исходов, ОКС, повторных оперативных вмешательств, возобновление стенокардии), мы установили, что в периоперационном периоде у пациентов группы КШ отмечалось увеличение положительных результатов на 2,7% при снижении общих затрат на 7.789 руб. В периоперационном периоде для получения единицы результата необходимо затратить 3.939,4 руб., в группе ТЛБАП с КС – 4.198,7 руб.
Через 3 года наблюдения в группе КШ отмечалось увеличение количества положительных результатов на 35,3% случаев на фоне снижения общих затрат на 113.877 руб. За весь период наблюдения для получения единицы результата необходимо затратить 5.230,2 руб., в группе ТЛБАП с КС – 14.038 руб.
После проведенного оперативного вмешательства 33,6% пациентов после КШ и 43% после ТЛБАП со стентированием вернулись к трудовой деятельности, 6% больных после КШ и 9% после ТЛБАП со стентированием были первично освидетельствованы во МСЭК и признаны инвалидами II группы. Наиболее сильное влияние на показатель долгосрочной занятости оказал такой фактор, как возраст пациента к моменту начала исследования. Медицинские факторы оказывали меньшее влияние на показатели занятости в долгосрочном плане, чем демографические факторы и характеристики самой работы.
Прогресс, который был достигнут в хирургическом лечении ИБС, диктует необходимость оценки результатов лечебных методик не только по оценке осложнений и смертности, но также и по эффективности результатов при долгосрочном наблюдении.
Коронарное шунтирование, с учетом объема реваскуляризации (полная и неполная)
При проведении КШ полная реваскуляризация (ПР) выполнена у 136 больных, неполная реваскуляризация (НР) – у 92 пациентов.
Операционная летальность при выполнении ПР составила 1 (0,7%), при НР - 3 (3,3%) (р<0,05). Периоперационный инфаркт миокарда (ИМ) имел место в группе ПР у 2,9%, в группе НР – у 3 (3,3%) Возобновление стенокардии III-IV ФК у 3 (3,4%) больных в группе НР (в группе ПР – не отмечено).
В отдаленном периоде после операции отмечено 1 (0,7%) летальный исход в группе ПР. Различия по рецидивам тяжелой стенокардии (III и IV ФК) чаще отмечалось в группе НР (за весь период наблюдения – у 9% пациентов (в группе ПР – 1,5%)). Необходимость в проведении повторных вмешательств (в группе с ПР - 1 (0,7%), с НР - 5 (5,6%) случаев).
В группе ПР в течение 3 лет отмечалось 69 случаев госпитализации (из них –,4%) с ОКС). В группе НР - 63 случая госпитализаций (7 (7,9%) - с ОКС). Средние затраты за весь период наблюдения за больными ИБС, включенными в исследование представлены на рис.2.
В периоперационном периоде в группе ПР отмечалось увеличение положительных результатов (отсутствие летальных исходов, ОКС, повторных реваскуляризаций, рецидива стенокардии III-IV ФК) в сравнении с группой НР на 19,6% при снижении общих затрат на 11.172,7 руб. Через 3 года в группе ПР - увеличение положительных результатов на 12,6% при снижении общих затрат на 0.345,4 руб.
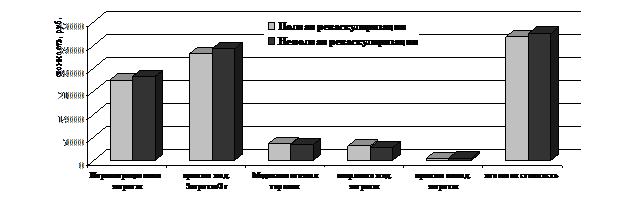
Рисунок 2. Средние затраты у больных ИБС, подвергшихся коронарному шунтированию с полной и неполной реваскуляризацией за период наблюдения
Анализ полученных данных подтверждает высокую эффективность ПР у больных с ИБС. Уже на госпитальном этапе реабилитации большинство пациентов были адаптированы к нагрузкам на уровне I – II ФК. Таким образом, увеличение объема операции не ухудшает непосредственные результаты, а отдаленные результаты свидетельствуют о преимуществах шунтирования мелких коронарных артерий.
ТЛБАП со стентированием с учетом объема реваскуляризации (полная и неполная)
При проведении ТЛБАП со стентированием ПР выполнена у 58 пациентах, НР – у 58. В среднем в группе ПР реваскуляризировано 78 сегментов (количество стентов – 1,3±0,05), стенты Сурhег (США) использовался у 6 (10,3%) больных (в группе НР реваскуляризировано 79 сегментов (в среднем – 1,4±0,04) стенты Сайфер – у 4 (6,9%) больных). Частота ангиографического успеха — 96,8%, клинического успеха – 69% (40 пациентов) (в группе НР – 94,8% и 50% (29 пациентов) соответственно).
Периоперационный ИМ отмечен у 1 (1,7%), рецидив стенокардии III-IV ФК у 6 (10,3%) больных в группе ПР и у 2 (3,4%) и 8 (13,8%) соответственно в группе НР.
За период наблюдения стенокардия напряжения III-IV ФК имела место в группе ПР – у 9 (15,5%), в группе НР - у,9%) (p < 0,05). Большее количество пациентов группы НР за период наблюдения перенесли повторный ИМ – 5 (8,6%) (в группе ПР - 1 (1,7%)) и повторные реваскуляризации –,7%) в группе с ПР – 7 (12,1%).
В группе ПР в течение 3 лет отмечалось 55 случаев госпитализаций (в группе НР – 66), в том числе с ОКС – в 3 (5,2%) и%) случаях соответственно. Стоимость лечения на амбулаторном этапе наблюдения у пациентов в группе ПР в течение 3 лет составила – 87.662,04±2515,2 руб. (в группе НР – 95.856,4±2725,3 руб.).
В периоперационном периоде у пациентов группы ПР отмечалось увеличение положительных результатов в сравнении с группой НР на 8,6% (через 3 года на 36,2%) при увеличении общих затрат на 1.985,3 руб. (через 3 года – на 31.486,4 руб.).
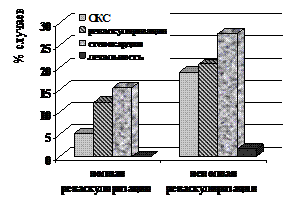
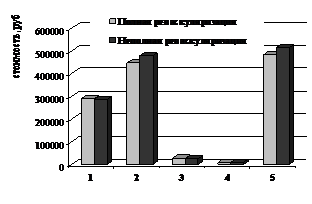
Осложнения в отдаленном периоде Средние затраты, руб.
Рисунок 3. Осложнения в отдаленном послеоперационном периоде и средние затраты у больных ИБС, подвергшихся ТЛБАП со стентированием с полной и неполной реваскуляризацией.
1-периоперационные затраты, руб.; 2 – прямые медицинские затраты за 3 года, руб.; 3 – непрямые медицинские затраты за 3 года, руб.; 4 – прямые немедицинские затраты за 3 года; 5 – итоговые затраты за 3 года, руб.
После проведения ТЛБАП со стентированием к концу периода наблюдения процент больных с возобновлением стенокардии был больше в группе НР. В этой связи, можно предположить, что при проведении ТЛАП со стентированием у больных с многососудистым поражением на прогноз заболевания влияет не степень реваскуляризации миокарда, а правильный выбор стеноза, ответственного за ишемию миокарда.
Коронарное шунтирование на работающем сердце и с использованием аппарата искусственного кровообращения
КШ без ИК выполнено у 47 больных, КШ с ИК – у 44 пациентов. Операции без ИК выполнялись с применением системы стабилизации миокарда (использовались Tissue Stabilizer OCTOPUS 4 (Medtronic)). Операция КШ в условиях ИК выполнялась по стандартной методике с применением венозных и артериальных графтов. В среднем у пациентов в группе КШ без ИК наложено 1,7±0,1 (в т. ч. артериальных – 0,9±0,03) шунтов, в группе КШ с ИК – 2,9±0,2 (в т. ч. артериальных – 0,86±0,03) .
Операционная кровопотеря при применении ИК в среднем в 1,6 раза превышала таковую при КШ без ИК, а необходимость хирургической ревизии раны по поводу кровотечения в группе после КШ с ИК чаще в 2,7 раза (2 (4,2%) в группе КШ без ИК и 5 (11,4%) - в группе КШ с ИК). Госпитальная летальность составила в группе КШ без ИК – 2,1%, в группе КШ с ИК – 11,4%, частота периоперационных ИМ – 2,1% и 6,8% соответственно, гемодинамически значимых НРС – 25,5% и 13,4%, преходящее нарушение мозгового кровообращения ,4%) наблюдении в группе КШ с ИК. Риск развития гнойных осложнений также сведен к минимуму: в группе КШ с ИК – 3 (7,7%) случаев наблюдали развитие серозно-гнойного медиастинита; синдром острого повреждения легких (СОПЛ) развился в 1 (2,1%) случае в группе КШ без ИК и у 8 (18,2%) – в группе КШ с ИК. Рецидив стенокардии III-IV ФК в раннем периоде отмечен у 2 (4,3%) пациентов после КШ на работающем сердце (в группе после КШ с ИК – не отмечено).
За период наблюдения стенокардия напряжения III-IV ФК имела место у пациентов в группе после КШ без ИК – у 3 (6,5%), в группе после КШ с ИК у 1 (2,6%) пациента.
В группе после КШ без ИК за время наблюдения отмечалось 23 случая госпитализации, из них – 4 (8,9%) случаев по поводу ОКС; в 1 (2,2%) случае выполнена повторная реваскуляризация. В группе после КШ с ИК - 15 случаев госпитализаций, из них 3 (7,9%) с ОКС, в 1 (2,6%) случае потребовалась ТЛБАП со стентированием.
Средняя сумма прямых медицинских затрат в периоперационном периоде у пациентов группы после КШ без ИК составила 252.518±3209,3 руб., в группе после КШ с ИК – 254.162,6±4697,7 руб. (p<0,05).
В периоперационном периоде в группе после КШ без ИК отмечалось увеличение положительных результатов в сравнении с группой после КШ с ИК на 20,2% при снижении общих затрат на 1.634,6 руб. Через 3 года наблюдения у пациентов группы после КШ без ИК отмечалось уменьшение положительных результатов на 1,5% при снижении общих затрат на 8.245,5 руб.
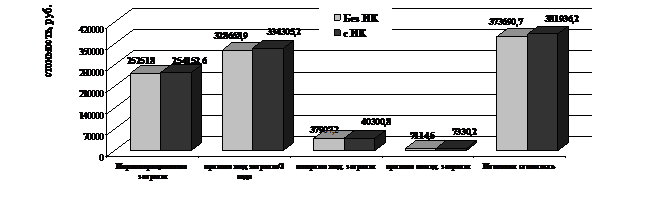
Рисунок 4. Средние затраты у больных ИБС, подвергшихся КШ на работающем сердце и в условиях ИК за весь период наблюдения
Основными преимуществами КШ без ИК являются: снижение количества летальных исходов, частоты периоперационных ИМ, послеоперационной кровопотери и необходимости гемотрансфузий, более короткий срок послеоперационного пребывания в отделении реанимации (2,9±0,07 и 4±0,3 сут. соответственно) и в клинике (15,1±0,3 сут, и 20,1±0,8 сут. соответственно); потенциальная экономия финансов.
По отдаленным результатам исследования в группе после КШ без ИК частота рецидива стенокардии III-IV ФК, отдаленной смертности и повторных реваскуляризаций отмечена в большем проценте случаев по сравнению с группой после КШ с ИК.
Коронарное шунтирование с геометрической реконструкцией ЛЖ
КШ с ГРЛЖ выполнено 130 пациентов, у 70 из которых исходно по данным ЭхоКГ (с учетом движения рубцово-измененного участка миокарда), были диагностированы акинетичные аневризмы ЛЖ и у 60 больных – дискинетичные.
В группе с акинетичными аневризмами в 8 (11,4%) случаях дополнительно выполнялась пластика митрального клапана (МК) на опорном кольце и в 1 (1,4%) случае – протезирование МК механическим протезом. В,1%) случаях резекция аневризмы была дополнена реваскуляризацией миокарда в необходимом объеме (в среднем - 2,9±0,03 шунтов).
В группе с дискинетичными аневризмами резекция аневризмы ЛЖ в 3 (5%) случае дополнительно выполнена пластика МК. В%) случаях резекция аневризмы была дополнена реваскуляризацией миокарда (в среднем – 2,8±0,2 шунтов).
В периоперационном периоде в группе с дискинетичными аневризмами отмечено меньшее количество пациентов с ишемией миокарда – (5% против 8,6%), СМСВ (0% против 7,1%), необходимостью применение ВАБК (0 против 4,3%), СОПЛ (5% против 11,4%). Возобновление стенокардии III-IV ФК в группах не отмечено.
По данным ЭхоКГ в раннем послеоперационном периоде хирургическая редукция аневризмы ЛЖ в группе с акинетичными аневризмами привела к более значимому снижению КДР ЛЖ - к концу первого месяца на 6,2%, к концу 1 года наблюдения на 4,7% от исходного значения, к концу 3 года – на 1,6% от исходного (в группе с дискинетичными аневризмами - 3,6%, 3,6% и на 5,4% соответственно). Также отмечалось уменьшение КДО за период наблюдения – на 17,1%, 14,5%, 8,7% соответственно (в группе с дискинетичными аневризмами - на 11,6%; 13,1% и 8,5%).
В группе с акинетичными аневризмами отмечается уменьшение ММ ЛЖ к концу первого месяца на 12,9%, к концу 1 года наблюдения на 9,5%, к концу 3 года – на 1,6% от исходного (в группе с дискинетичными аневризмами – на 4,6%; 7,7%; и 5% соответственно).
Отмечается уменьшение МС у пациентов к концу первого месяца на 5,6%, к концу 1 года наблюдения – на 3,7%, к концу 3 года – увеличение на 3,5% от исходного (в группе с дискинетичными аневризмами – уменьшение на 6%; 9,1%; и 5,4% соответственно).
Независимо от вида аневризмы, ГРЛЖ приводила к уменьшению ФК стенокардии, максимально выраженную в раннем послеоперационном периоде. За трехлетний период наблюдения рецидив стенокардии III-IV ФК отмечен у 4 (6,1%) больных в группе с акинетичными аневризмами и у 1 (1,7%) в группе с дискинетичными аневризмами. Значительно реже (у 16,6%) снижаются клинические проявления сердечной недостаточности. У 48,6% больных в группе с акинетичными аневризмами и 50% в группе с дискинетичными аневризмами ХСН IIА стадии сохранялась или прогрессировала в течение года наблюдения. При межгрупповом сравнении также отмечено, что ФК ХСН с акинетичными аневризмами превышал таковые значения в группе с дискинетичными аневризмами.
В периоперационном периоде в группе с акинетичными аневризмами отмечалось уменьшение положительных результатов в сравнении с группой с дискинетичными аневризмами на 12,9% (через 3 года на 6,4%) при увеличении общих затрат на 5.864,4 руб. (через 3 года - при увеличении общих затрат на 13.003,7 руб.).
Средние затраты за весь период наблюдения за больными ИБС, включенными в исследование представлены на рис.5.

Рисунок 5. Средние затраты у пациентов ИБС с акинетичными и дискинетичными аневризмами левого желудочка, подвергшихся КШ с ГРЛЖ за период наблюдения
Акинетичные постинфарктные аневризмы ЛЖ по сравнению с дискинетичными определяют более неблагоприятное течение послеоперационного периода и менее эффективные результаты операции. Наличие дискинетичной аневризмы связано с более значимым послеоперационным повышением ФВ и меньшей операционной летальностью (в группе акинетичных аневризм – 5 (7,1%) летальных исходов, в группе с дискинетичными аневризмами - 2 (3,3%)).
Реваскуляризация миокарда у больных ИБС с острым коронарным синдромом на момент оперативного вмешательства
133 пациента с ИБС, находившиеся на стационарном лечении с диагнозом ОКС, которым была выполнена реваскуляризация миокарда, были рандомизированы в 2 группы в зависимости от тактики реваскуляризации - 57 пациентам выполнено КШ и 76 пациентам ТЛБАП со стентированием. Группы были однородны по демографическим показателям и наличию сопутствующей патологии.
Большая часть больных обеих групп ,9%) в группе КШ и,9%) в группе ТЛБАП со стентированием (р>0.05)) страдали прогрессирующей стенокардией. Впервые возникшую стенокардию чаще диагностировали среди пациентов группы ТЛБАП со стентированием (2 (2,6%)), ранняя постинфарктная стенокардия имела место у,1%) пациентов в группе КШ и,5%) в группе ТЛБАП со стентированием.
Основным видом оперативного вмешательства у пациентов группы КШ было КШ в условиях ИК (у 87,7%). В среднем наложено 3,7±0,16 (в т. ч. артериальных – 1±0,01) шунтов. Основным видом эндоваскулярного вмешательства - была ТЛБАП со стентированием. 76 пациентам были имплантированы 107 стентов (1,3±0,01) для устранения 200 стенозов.
Отсроченное КШ выполнено,7%) больным, экстренное КШ - 3 (5,3%) пациентам в группе. Экстренную ТЛБАП со стентированием выполнили,5%), отсроченную -,5%) пациентам.
Непосредственный клинический эффект КШ и ТЛБАП со стентированием при ОКС составляет, соответственно, 93,8% и 94,7%. Периоперационная летальность (операция + первые сутки после операции) в группе КШ – 1,7% против 5,3% в группе ТЛБАП со стентированием. Достоверные различия отмечены по частоте развития периоперационного ИМ (1,7% в группе КШ против 10,5% в группе ТЛБАП со стентированием). Острая сердечно-сосудистая недостаточность, не связанная с интраоперационным ИМ, достоверно чаще возникает у оперированных пациентов ,1%) против 4 (5,3%) (p < 0.05)). Рецидив стенокардии III-IV ФК на момент выписки в группе КШ - 2 (3,6%), в группе ТЛБАП со стентированием -,3%).
За 3 года наблюдения в группе КШ у 5 (8,9%) пациентов наблюдалась клиника ОКС, в 1 (1,8%) случае выполнена повторная реваскуляризация (ТЛБАП со стентированием аутовенозного шунта), летальных исходов не было. В группе ТЛБАП со стентированием - в,1%) случаях отмечено развитие ОКС, у,5%) пациентов выполнены повторные реваскуляризации ,6%) - ТЛБАП со стентированием и 5 (6,9%) – КШ), из них у 3 (4,2%) в течение первого года после вмешательства, летальных исходов – 1 (1,4%). Рецидив стенокардии III-IV ФК за период наблюдения отмечен у 2 (3,6%) пациентов, в группе ТЛБАП со стентированием – у%).
Основные затраты при лечении больных с ОКС при проведении реваскуляризации миокарда приходятся на стоимость оперативного вмешательства (в группе КШ – 250.023,1±1812,6 руб., в группе ТЛБАП со стентированием – 292.834,2±12034 руб.). Стоимость лечения на амбулаторном этапе наблюдения у пациентов в группе КШ в течение 3 лет составила – 51.966,8±2560,3 руб. (в группе ТЛБАП со стентированием – 106.400,9±4333 руб.) (p < 0,05).
В периоперационном периоде в группе КШ отмечалось увеличение положительных результатов в сравнении с группой ТЛБАП со стентированием на 36% при снижении общих затрат на 42.811,1 руб. Через 3 года наблюдения у пациентов в группе КШ - увеличение положительных результатов на 50% при снижении общих затрат на 176.338,6 руб.
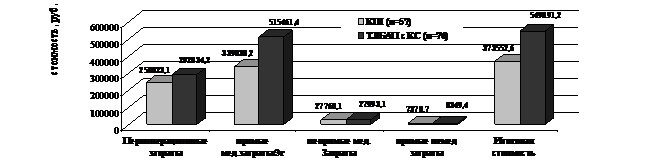 Рисунок 6. Средние затраты у пациентов ИБС с острым коронарным синдромом, подвергшихся реваскуляризации миокарда за период наблюдения
Рисунок 6. Средние затраты у пациентов ИБС с острым коронарным синдромом, подвергшихся реваскуляризации миокарда за период наблюдения
Активное использование эндоваскулярных и хирургических методов лечения больных с ОКС позволяет снизить частоту развития ОИМ и летальных исходов на стационарном этапе и в отдаленные сроки. Однако нужно отметить значительно большую необходимость повторных вмешательств у пациентов, перенесших ТЛБАП со стентированием.
Реваскуляризация миокарда у больных ИБС с низкой ФВ левого желудочка
Реваскуляризация миокарда больным с ИБС с низкой ФВ была выполнена 104 пациентам: 64 пациента перенесли КШ и 40 пациентов – ТЛБАП со стентированием.
По данным ЭХО КГ в группе КШ - величина ФВ колебалась от 19% до 40% (в среднем – 32,9±0,6%). В группе ТЛБАП со стентированием - от 19% до 40% (в среднем – 32,6±0,9%). У пациентов в обеих группах отмечалась псевдонормализация диастолической дисфункции.
Основной вид оперативного вмешательства у пациентов группы КШ - КШ в условиях ИК. Количество шунтов в среднем - 3,4±0,2. Интраоперационное решунтирование выполнено у 3 (4,7%) больных. Частота периоперационного ИМ – 12,5%, летальных исходов - 5 (7,8%) случаев.
Основным видом эндоваскулярного вмешательства была ТЛБАП со стентированием. Всего имплантировано 55 стентов (в среднем -1,4±0,01), из них 3 (7,5%) с лекарственным покрытием. Частота периоперационного ИМ – 1 (2,5%), летальных исходов - 1 (2,5%) случаев.
За период наблюдения в группе КШ установлено достоверное увеличение общей ФВ от 32,9±0,06% до 43,8±1,3% (р<0,001). В группе ТЛБАП со стентированием - с 32,6±0,9 до 41,6%±1,9 (р<0,001).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |



