Глубокий неинвазивный мониторинг гемодинамики как маркер оценки инверсии дыхания во время анестезии
,
До сих пор мало сведений о механизмах влияния респираторной поддержки на гемодинамику. Многие из них противоречивы. Появление респираторов последних поколений принято считать важным для лечения поражённого лёгкого ("жёсткого", наводнённого и пр.). Общеизвестно также, что традиционная ИВЛ во время анестезии способна привести к жёсткому лёгкому и нарушению гемодинамики. Одним из главных направлений улучшающей ИВЛ является метод респираторной поддержки в виде инверсии вдоха к выдоху, а также ПДКВ для создания лучших условий для поддержания альвеол открытыми, препятствуя процессам формирования "жёсткого" лёгкого. Однако влияние этих методов остаётся малоизученным с точки зрения влияния на гемодинамику.
В то же время, в последнее время всё большее внимание уделяется вариативности пульсации аорты, ударного объёма сердца в процессе вентиляции пациентов. Вариабельность сердечного ритма стала популярным методом оценки регуляторных процессов, зависимых от вегетативных сдвигов при различной патологии. Исходя из этих соображений целью исследования послужила сравнительная оценка вариабельности 12 параметров гемодинамики на фоне различных режимов вентиляции с премедикацией НПВП и без неё, а также оценка параметров механики дыхания до операции и в конце неё.
Материал и методы
После получения информированного согласия проведено обследование 86 пациентов без сопутствующей кардиореспираторной патологии ASA I-II, которым выполнена плановая гистерэктомия. Протокол включал рандомизацию и распределение больных на 4 группы в зависимости от режима ИВЛ и премедикации.
Нами применены два вида соотношения вдоха и выдоха - 1:2 и 2:1. Использовали для уточнения влияния растяжения альвеол РЕЕР и воздействия на метаболизм - нестероидный противовоспалительный аналгетик ортофен.
В 1-й группе (N=28) во время наркоза проводилась ИВЛ аппаратом "KION" Siemens с традиционным соотношением продолжительности вдоха к выдоху 1:2 и минимальным РЕЕР - 2 см. вод. ст. Во второй группе (N=22) ИВЛ с I:E 2:1, общая продолжительность которой составляла 50 ± минут. В третьей группе (N=20) применялась та же методика, что и во второй, но на фоне премедикации НПВП (ортофен 75 мг). В четвёртой группе (N=16) ИВЛ проводилась при физиологическом соотношении вдоха к выдоху I:E 1:2 в сочетании с РЕЕР. 5-6 см. вод. ст., которое устанавливалось таким образом, чтобы уровень среднего давления в дыхательных путях Pmean соответствовал среднему уровню (М Pmean) среднего давления, регистрируемого во второй группе.
Всем пациентам ИВЛ применялась со стандартными параметрами VТ - 7 мл/кг, MVе - 70мл/кг, FiO2 0.28, прямоугольной формой инспираторного потока (постоянный поток). Методика анестезии была сопоставима на всех её этапах и проводилась по вышеуказанной общепринятой схеме. Вводная анестезия: фентанил 2-3 мкг/кг, тиопентал Na 300-350 мг, миоплегия дитилином из расчёта 2 мг/кг. Поддержание анестезии: фторотан 0,8 - 1,0 об.%, фентанил 0,15 - 0,2 мг, миоплегия - ардуан 0,04 - 0,05 мг/кг.
Измерение контрольных показателей респираторной механики производилось с использованием монитора Servo Screen 390 в условиях полной мышечной релаксации с контролем нейромышечной проводимости аппаратом TOF-GUARD. Протокол исследования включал регистрацию следующих показателей: Рpeak, Рpause, Рmean (давление: пиковое, во время инспираторной паузы, среднее), Dyn. Char. (динамический комплайнс), Re (сопротивление дыхательных путей на выдохе), на 2 этапах операции: 1-й исходный - непосредственно после интубации, в условиях полной мышечной релаксации, до операции (базовые показатели механики дыхания); 2-й контроль через 50 ± мин (после удаления матки и ранорасширителя из брюшной полости, также в условиях полной мышечной релаксации). Регистрация Dyn. Char. выполнялась на основании расчёта среднего показателя за 10 циклов с момента наименьшего колебания отображаемого на дисплее значения.
При изучении легочной механики статистическая значимость изменений получена только для двух показателей: Ppeak, Dyn. char.(динамический комплайнс) в группах, где не использовалась премедикация с НПВП. В третьей группе больных (вентиляция 2:1+ ортофен) была отмечена аналогичная направленность изменений регистрируемых показателей, но статистической значимости не наблюдалось. Несмотря на то, что исходные показатели Ppeak, Pmean в первой и третьей группах оказались фактически одинаковыми, результирующие изменения динамических характеристик у больных после премедикации были менее выраженными, несмотря на инверсию I:E. Существенных различий в содержании углекислоты в выдыхаемом газе не отмечено (колебания et CO2 в пределах 1-2 мм. рт. ст.). Иными словами, можно отметить, что грубых нарушений механики дыхания не происходило.
При этом наиболее статистически значимые сдвиги обнаружены при измерении вариабельности параметров гемодинамики. Эти сдвиги характеризовались как числом, так и особенностью распределения.
Гемодинамика регистрировалась неинвазивным способом по компьютерной технологии проф. . Автоматически параметры регистрировались за 500 ударов сердца и проводился расчёт спектров по Фурье. В результате получения каждой выборки из 500 ударов рассчитывались не только абсолютные значения (что уже само по себе давало возможность получить среднее арифметическое значение и медиану более корректно, чем за меньшее число ударов сердца). Проводился расчёт вариабельности (отклонения от среднего значения за эти пятьсот ударов) в виде дисперсии (S) или её квадрата, что позволяло получить спектральную плотность мощности спектра, обозначаемую как общую мощность (P - power). Она говорила о выраженности колебательного процесса вообще. Выделение таких значений в четырёх диапазонах спектра позволяла анализировать разные виды регуляторной активности, ведя расчёт мощности (Р) на четырёх общепризнанных частотах: парасимпатическую (связанную с дыханием) - Р4 (0.15-0.5Гц); симпатическую-Р3 (0.07-0.15 Гц); гуморальную - Р2 (0.03-0.07 Гц) и метаболическую (0-0.03Гц).
Анализ проводился со следующими допущениями: что колебания АД отражают роль барорегуляции, колебания УО связаны с регуляцией объёма. Доказательства этому в литературе имеются. С барорегуляцией связывают преимущественно диапазон Р3, с объёмной регуляцией - диапазон спектра Р4. Для удобства понимания мы так эти процессы и называли. Нами отслеживались не только абсолютные значения Р1, Р2, Р3 и Р4, но и их процентное отношение к общей величине мощности колебаний (Р). Кроме этого рассчитывалась середина спектра (Fm - frequency median) каждого параметра в герцах. Он отражал состояние свообразного "качания" процесса колебания по шкале частот. Если это происходило вправо - больше высокочастотных значений, влево - наоборот.
Наконец, мы использовали известный приём, обозначая сдвиги каждого из мощностей диапазона в виде активности самостоятельного регулятора. То есть мощность спектра в каждом из четырёх диапазонов (Р1,Р2,Р3 и Р4) рассматривалась нами как состояние определённого регулятора. Это отвечает общей тенденции анализа регуляции с позиции вариабельности: "вариабельность как мера регуляции".
Результаты и обсуждение
Для конечного результата барорегуляции в виде АД наиболее неблагоприятным оказалось применение вдоха и выдоха (I:E) 1:2 и применение РЕЕР, поскольку произошла активация медленноволновых процессов (прирост Р1 и Р2) на фоне повышения мощности всего спектра АД. Поскольку при применении препарата метаболического действия ортофена этих сдвигов не происходило, можно считать объективным вывод о соответсвующем повышении метаболической регуляции (Р1 и Р2). В свою очередь прирост Р3 при применении инверсии I:E - 2:1 даёт основание говорить о лучшей барорегуляции во время этого вида респираторной поддержки.
Применение дыхания 1: 2 также оказало неблагоприятное перераспределение мощности колебаний ритма сердца (РС) в сторону самых медленных волн (Р1 и Р2) при отсутствии изменений абсолютных значений. Логично середина всего спектра (Fm) сдвинулась в сторону медленных колебаний Интересно, что инверсия дыхания 2:1 вызвала изменения регуляторной активности ритма сердца, совпадающее по многим параметрам с теми, которые имели место при описаннии влияния дыхания 1:2 на АД. То есть произошла активация медленноволновых регуляторов. Применение РЕЕР изменило ситуацию в противоположную сторону, например Fm переместилась в направлении более высоких частот и приросте барорегуляторного осциллятора Р3 при явном снижении медленных волн. То есть РЕЕР оказал благоприятное действие на регуляцию ритма сердца при дыхании 1:2, чем одно только дыхание 1:2. Видимо, растяжение рецепторов альвеолярной зоны благоприятно сказалось на регуляции ритма сердца. Ортофен при дыхании 2:1 способствовал урежению ритма сердца (аналгетические свойства), не препятствовал приросту активности метаболического регулятора Р1% и способствовал снижению Р3%. И здесь сказалась разница воздействия ортофена на регуляцию АД и РС.
Более предпочтительным с точки зрения распределения спектральной активности УО по сравнению с остальными оказался режим с РЕЕР на фоне дыхания 1:2. Он не снизил абсолютной величины и благоприятно способствовал снижению медленных волн (Р1, Р1%, Р2%), приросту активности симпатической и парасимпатической систем регуляции (Р3, Р4, Р3%). Середина спектра сместилась вправо (в сторону высоких частот). Одно только соотношение 1:2 вызвало снижение УО, общей мощности спектра Р. Интересно, что при этом снизились осцилляторы С3 и С4 , но вырос Р1% - самый медленноволновой спектр. В целом реакция оказалось неблагоприятной. Режим 2:1 почти не изменил ситуацию (снизился Р2 и прирос Р2%). Применение ортофена, наоборот, способствовало выраженному росту Р1%, Р2% и снижению Р4. Это обстоятельство говорит о том, что имеется связь регуляторов медленных волн УО с изменённым метаболизмом.
Особый интерес представляет изменение вариабельности пульсации кровенаполнения пальца ноги. Дыхание в режиме 1:2 вызвал только снижение амплитуды пульсации. Оно никак не повлияло на спектральные характеристики. Зато дыхание с соотношением вдох-выдох 2:1 вызвало резкое увеличение общей мощности спектра, прирост дисперсии за счёт прироста мощности колебаний Р1, Р2 и Р3. При этом были меньше Р2% и больше Р3%. Важно, что применение ортофена практически устранило эту картину, сохранив только достоверный (небольшого уровня) прирост дисперсии и Р2. Здесь налицо влияние на гуморально-метаболические и барорегуляторные (здесь симпатические) влияния на микрососуды периферии длительного вдоха, возможно, за счёт большего раздражения рецепторов растяжения альвеол. Можно говорить об активном эфферентном звене регуляции обратном метаболорефлексу.
Таблица 1
Статистически достоверные сдвиги данных спектрального анализа
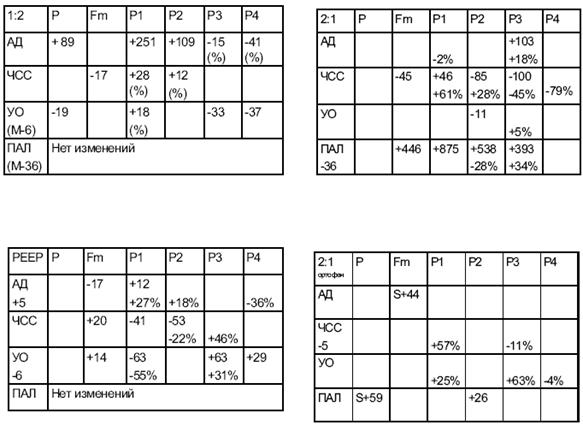
ЗАКЛЮЧЕНИЕ
В данной работе мы использовали анализ вариабельности четырёх главных параметров гемодинамики, которые широко используются анестезиологами и реаниматологами у критических больных.
При применении трёх видов ИВЛ мы не обнаружили выраженных сдвигов механики дыхания. Не было выраженных сдвигов абсолютных значений гемодинамики. Однако вариабельность параметров изменилась весьма существенно и с особым значением. Это говорит о важной роли вариабельности как мере регуляции. Известно, что регуляция изменяется раньше существенных сдвигов. Она может быть маркером начальных признаков напряжённости адаптационной системы.
Следует выделить важные аспекты влияния стандартного и инверсированного искусственного дыхания во время анестезии при здоровом лёгком.
Режим отношения вдоха к выдоху является значительной нагрузкой на регуляторную систему центрального кровообращения, в результате которой активизируется гуморально - метаболические регуляторы. Как известно, их преобладание делает регуляцию более медленной и более уязвимой для экстремальных ситуаций.
Режим 2:1 является более оптимальным, особенно если он сочетается с применением средств блокады метаболизма.
Режим положительного давления на выдохе менее однозначно влияет на регуляторные параметры основных показателей гемодинамики. Хуже всего то, что он влияет на замедленность регуляции артериального давления. Однако регуляция ударного объёма становится лучше. Вероятно, это служит компенсацией.
Интерес представляет тот факт, что разные режимы вентиляции так или иначе влияют на самые медленноволновые процессы изменения параметра ударного объёма. Мы предполагаем, что это связано с изменениями тех процессов перемещения объёмов (в частности венозного возврата), которые связаны с метаболическими функциями тканей и органов.
В целом можно говорить о важности измерения вариабельности параметров гемодинамики как маркеров эффективности применения ИВЛ во время анестезии.




