63. Аферезные гранулоциты перед переливанием облучаются в дозе от 25 до 50 Грей.
64. Аферезные гранулоциты переливаются сразу после их получения.
65. Основными медицинскими показаниями к назначению переливания гранулоцитов являются:
а) снижение абсолютного количества гранулоцитов у реципиента менее ![]() при наличии неконтролируемой антибактериальной терапией инфекции;
при наличии неконтролируемой антибактериальной терапией инфекции;
б) сепсис новорожденных, неконтролируемый антибактериальной терапией.
Гранулоциты должны быть совместимы по антигенам систем АВО и резус-принадлежности.
66. Критериями оценки эффективности трансфузии (переливания) гранулоцитов является положительная динамика клинической картины заболевания: снижение температуры тела, уменьшение интоксикации, стабилизация ранее нарушенных функций органов.
XII. Правила трансфузии (переливания) донорской крови и (или) ее компонентов детям
67. При поступлении в организацию ребенка, нуждающегося в трансфузии (переливании) донорской крови и (или) ее компонентов, первичное исследование групповой и резус-принадлежности крови ребенка проводится медицинским работником в соответствии с требованиями пункта 7 настоящих Правил.
68. В обязательном порядке у ребенка, нуждающегося в трансфузии (переливании) компонентов донорской крови и (или) ее компонентов (после первичного определения групповой и резус-принадлежности), в клинико-диагностической лаборатории проводятся: подтверждающее определение группы крови АВО и резус-принадлежности, фенотипирование по другим антигенам эритроцитов С, с, Е, е, ![]() , К и k, а также выявление антиэритроцитарных антител.
, К и k, а также выявление антиэритроцитарных антител.
Указанные исследования проводятся в соответствии со следующими требованиями:
а) определение группы крови по системе АВО проводится с использованием реагентов, содержащих антитела анти-А и анти-В. У детей старше 4 месяцев группа крови определяется, в том числе перекрестным методом, с использованием реагентов анти-А, анти-В и стандартных эритроцитов O(I), А(II) и В(III);
б) определение резус-принадлежности (антиген D) проводится с использованием реагентов, содержащих анти-D-антитела;
в) определение антигенов эритроцитов С, с, Е, е, ![]() , К и k проводится с использованием реагентов, содержащих соответствующие антитела;
, К и k проводится с использованием реагентов, содержащих соответствующие антитела;
г) скрининг антиэритроцитарных антител проводится непрямым антиглобулиновым тестом, при котором выявляются клинически значимые антитела, с использованием панели стандартных эритроцитов, состоящей не менее чем из 3 образцов клеток, содержащих в совокупности клинически значимые антигены в соответствии с подпунктом "г" пункта 22 настоящих Правил. Не допускается применение смеси (пула) образцов эритроцитов для скрининга антиэритроцитарных аллоантител.
69. При выявлении у ребенка антиэритроцитарных антител осуществляется индивидуальный подбор доноров эритроцитсодержащих компонентов с проведением непрямого антиглобулинового теста или его модификации с аналогичной чувствительностью.
70. При необходимости экстренной трансфузии (переливания) донорской крови и (или) ее компонентов в стационарных условиях организации при отсутствии круглосуточного иммуносерологического обеспечения, ответственным за определение группы крови по системе АВО и резус-принадлежности ребенка является врач, проводящий трансфузию (переливание) донорской крови и (или) ее компонентов.
71. Выполнение исследований, указанных в пункте 68 настоящих Правил, проводят иммуносерологическими методами: ручным способом (нанесение реагентов и образцов крови на плоскую поверхность или в пробирку) и с применением лабораторного оборудования (внесение реагентов и образцов крови в микропланшеты, колонки с гелем или стеклянными микросферами и другими, разрешенными к применению для данных целей на территории Российской Федерации методами исследования).
72. Для проведения трансфузии (переливания) донорской крови эритроцитсодержащих компонентов аллоиммунизированным реципиентам детского возраста применяются следующие правила:
а) при выявлении у реципиента детского возраста экстраагглютининов 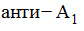 ему переливаются эритроцитсодержащие компоненты, не содержащие антигена
ему переливаются эритроцитсодержащие компоненты, не содержащие антигена ![]() , свежезамороженную плазму - одногруппную. Реципиенту детского возраста с
, свежезамороженную плазму - одногруппную. Реципиенту детского возраста с 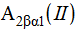 переливаются отмытые эритроциты O(I) и свежезамороженная плазма А(II), реципиенту детского возраста с
переливаются отмытые эритроциты O(I) и свежезамороженная плазма А(II), реципиенту детского возраста с ![]() переливаются отмытые эритроциты O(I) или В(III) и свежезамороженная плазма AB(IV);
переливаются отмытые эритроциты O(I) или В(III) и свежезамороженная плазма AB(IV);
б) при наличии у реципиента детского возраста неспецифически реагирующих антиэритроцитарных антител (панагглютининов) ему переливаются эритроцитсодержащие компоненты O(I) резус-отрицательные, не реагирующие в серологических реакциях с сывороткой реципиента;
в) для аллоиммунизированных реципиентов детского возраста индивидуальный подбор донорской крови и эритроцитсодержащих компонентов проводится в клинико-диагностической лаборатории;
г) для HLA-иммунизированных реципиентов детского возраста проводится подбор доноров тромбоцитов по системе HLA.
73. У новорожденных в день трансфузии (переливания) донорской крови и (или) ее компонентов (не ранее чем за 24 часа до трансфузии (переливания) из вены производится забор крови не более 1,5 мл; у детей грудного возраста и старше из вены производится забор крови 1,5 - 3,0 мл в пробирку без антикоагулянта для проведения обязательных контрольных исследований и проб на совместимость. Пробирка должна быть маркирована с указанием фамилии и инициалов реципиента детского возраста (в случае новорожденных первых часов жизни указывается фамилия и инициалы матери), номера медицинской документации, отражающей состояние здоровья реципиента детского возраста, наименования отделения, групповой и резус-принадлежности, даты взятия образца крови.
74. При плановом переливании эритроцитсодержащих компонентов врач, проводящий трансфузию (переливание) донорской крови и (или) ее компонентов, обязан:
а) по данным медицинской документации, отражающей состояние здоровья реципиента детского возраста, и данным на этикетке контейнера, сравнить фенотип донора и реципиента по антигенам эритроцитов с целью установления их совместимости. Запрещается введение пациенту антигена эритроцитов, отсутствующего в его фенотипе;
б) перепроверить группу крови реципиента детского возраста по системе АВО;
в) определить группу крови донора по системе АВО (резус-принадлежность донора устанавливается по обозначению на контейнере);
г) провести пробу на индивидуальную совместимость крови реципиента детского возраста и донора методами: на плоскости при комнатной температуре, одной из трех проб (непрямая реакция Кумбса или ее аналоги, реакция конглютинации с 10% желатином или реакция конглютинации с 33% полиглюкином). Если донорская кровь или эритроцитсодержащий компонент индивидуально подобран в клинико-диагностической лаборатории, данная проба не проводится;
д) провести биологическую пробу.
75. При экстренной трансфузии (переливании) эритроцитсодержащих компонентов реципиенту детского возраста врач, проводящий трансфузию (переливание) донорской крови и (или) ее компонентов, обязан:
а) определить группу крови реципиента детского возраста по системе АВО и его резус-принадлежность;
б) определить группу крови донора по системе АВО (резус-принадлежность донора устанавливают по обозначению на контейнере);
в) провести пробу на индивидуальную совместимость крови донора и реципиента детского возраста методами: на плоскости при комнатной температуре, одной из трех проб (непрямая реакция Кумбса или ее аналоги, реакция конглютинации с 10% желатином или реакция конглютинации с 33% полиглюкином);
г) провести биологическую пробу.
В случае невозможности определения фенотипа реципиента детского возраста по антигенам эритроцитов С, с, Е, е, ![]() , К и k допускается не учитывать при переливании эритроцитсодержащих компонентов указанные антигены.
, К и k допускается не учитывать при переливании эритроцитсодержащих компонентов указанные антигены.
76. Биологическая проба при проведении трансфузии (переливании) донорской крови и (или) ее компонентов реципиенту детского возраста проводится в обязательном порядке.
Порядок проведения биологической пробы:
а) биологическая проба состоит в трехкратном введении донорской крови и (или) ее компонентов с последующим наблюдением за состоянием реципиента детского возраста в течение 3 - 5 минут при пережатой системе для переливания крови;
б) объем вводимой донорской крови и (или) ее компонентов для детей до 1 года составляет 1 - 2 мл, от 1 года до 10 лет мл, после 10 лет мл;
в) при отсутствии реакций и осложнений трансфузия (переливание) донорской крови и (или) ее компонентов продолжается при постоянном наблюдении врача, проводящего трансфузию (переливание) донорской крови и (или) ее компонентов.
Экстренная трансфузия (переливание) донорской крови и (или) ее компонентов реципиенту детского возраста также проводится с применением биологической пробы.
Биологическая проба, как и проба на индивидуальную совместимость, проводится в обязательном порядке в тех случаях, когда реципиенту детского возраста переливается индивидуально подобранная в лаборатории или фенотипированная донорская кровь или эритроцитсодержащие компоненты.
77. Критерием оценки трансфузии (переливания) донорской крови и эритроцитсодержащих компонентов у детей является комплексная оценка клинического состояния ребенка и данных лабораторного исследования.
Для детей до 1 года в критическом состоянии трансфузия (переливание) донорской крови и (или) эритроцитсодержащих компонентов проводится при уровне гемоглобина менее 85 г/л. Для детей старшего возраста трансфузия (переливание) донорской крови и (или) эритроцитсодержащих компонентов - при уровне гемоглобина менее 70 г/л.
78. При трансфузии (переливании) донорской крови и (или) эритроцитсодержащих компонентов новорожденным:
а) переливаются эритроцитсодержащие компоненты, обедненные лейкоцитами (эритроцитная взвесь, эритроцитная масса, отмытые эритроциты, размороженные и отмытые эритроциты);
б) трансфузия (переливание) новорожденным проводятся под контролем объема перелитых компонентов донорской крови и объема взятой на исследования крови;
в) объем трансфузии (переливания) определяется из расчетамл на 1 кг массы тела;
г) для трансфузии (переливания) используют эритроцитсодержащие компоненты со сроком хранения не более 10 дней с момента заготовки;
д) скорость трансфузии (переливания) донорской крови и (или) эритроцитсодержащих компонентов составляет 5 мл на 1 кг массы тела в час под обязательным контролем показателей гемодинамики, дыхания и функции почек;
е) компоненты донорской крови предварительно согревают до температуры°С;
ж) при подборе компонентов донорской крови для трансфузии (переливания) учитывается, что мать является нежелательным донором свежезамороженной плазмы для новорожденного, поскольку плазма матери может содержать аллоиммунные антитела против эритроцитов новорожденного, а отец является нежелательным донором эритроцитсодержащих компонентов, поскольку против антигенов отца в крови новорожденного могут быть антитела, проникшие из кровотока матери через плаценту;
з) наиболее предпочтительным является переливание детям негативного по цитомегаловирусу эритроцитосодержащего компонента.
79. Подбор донорской крови и (или) ее компонентов при трансфузии (переливании) детям до четырех месяцев жизни при гемолитической болезни новорожденных по системе АВО или подозрении на гемолитическую болезнь новорожденных осуществляется в соответствии с таблицей, приведенной в приложении N 3 к настоящим Правилам.
В случае трансфузии (переливания) эритроцитсодержащих компонентов, отличающихся по системе АВО от группы крови ребенка, используются отмытые или размороженные эритроциты, не содержащие плазмы с агглютининами ![]() и
и ![]() , с учетом фенотипа реципиента.
, с учетом фенотипа реципиента.
80. Для внутриутробной трансфузии (переливания) донорской крови и (или) ее компонентов используются эритроцитсодержащие компоненты O(I) группы резус-D-отрицательные со сроком хранения не более 5 дней с момента заготовки компонента.
81. Заменные переливания крови осуществляются для коррекции анемии и гипербилирубинемии при тяжелой форме гемолитической болезни новорожденных или при гипербилирубинемии любой этиологии: ДВС-синдроме, сепсисе и других угрожающих жизни ребенка заболеваниях.
82. Для заменного переливания крови используются эритроцитсодержащие компоненты со сроком хранения не более 5 дней с момента заготовки компонента.
83. Донорская кровь и (или) ее компоненты переливаются из расчета мл/кг массы тела для доношенного ребенка и мл/кг для недоношенного.
84. Подбор компонентов донорской крови в зависимости от специфичности аллоантител осуществляется следующим образом:
а) при гемолитической болезни новорожденных, вызванной аллоиммунизацией к антигену D системы резус, используются одногруппные резус-отрицательные эритроцитсодержащие компоненты и одногруппная резус-отрицательная свежезамороженная плазма;
б) при несовместимости по антигенам системы АВО переливаются отмытые эритроциты или эритроцитная взвесь и свежезамороженная плазма в соответствии с таблицей, приведенной в приложении N 3 к настоящим Правилам, соответствующие резус-принадлежности и фенотипу ребенка;
в) при одновременной несовместимости по антигенам систем АВО и резус переливают отмытые эритроциты или эритроцитную взвесь O(I) группы резус-отрицательные и свежезамороженную плазму AB(IV) резус-отрицательную;
г) при гемолитической болезни новорожденных, вызванной аллоиммунизацией к другим редким антигенам эритроцитов, осуществляется индивидуальный подбор донорской крови.
85. Свежезамороженная плазма переливается реципиенту детского возраста в целях устранения дефицита плазменных факторов свертывания, при коагулопатиях, при острой массивной кровопотере (более 20% объема циркулирующей крови) и при выполнении терапевтического плазмафереза.
Не допускается переливание свежезамороженной плазмы вирус (патоген) инактивированной реципиентам детского возраста, находящимся на фототерапии.
XIII. Аутодонорство компонентов крови и аутогемотрансфузия
86. При проведении аутодонорства используются следующие методы:
а) предоперационная заготовка аутокомпонентов крови (аутоплазмы и аутоэритроцитов) из дозы консервированной аутокрови или методом афереза;
б) предоперационная нормоволемическая или гиперволемическая гемодилюция, предполагающая заготовку 1 - 2 доз крови (мл) непосредственно до операции или начала анестезии с обязательным восполнением временной кровопотери солевыми и коллоидными растворами с поддержанием нормоволемии или гиперволемии;
в) интраоперационная аппаратная реинфузия крови, предполагающая сбор во время операции из операционной раны и полостей излившейся крови с выделением из нее эритроцитов с последующим отмыванием, концентрированием и последующим возвратом в русло крови реципиента аутоэритроцитов;
г) трансфузия (переливание) дренажной крови, полученной в стерильных условиях при послеоперационном дренировании полостей тела, с использованием специализированного оборудования и (или) материалов.
Каждый из указанных методов может применяться отдельно или в различных сочетаниях. Допускается одновременное или последовательное проведение трансфузии (переливания) аутологичных компонентов крови с аллогенными.
87. При проведении аутотрансфузии крови и ее компонентов:
а) пациент дает информированное согласие на заготовку аутокрови или ее компонентов, которое фиксируется в медицинской документации, отражающей состояние здоровья реципиента;
б) предоперационная заготовка аутокрови или ее компонентов осуществляется при уровне гемоглобина не ниже 110 г/л, гематокрита - не ниже 33%;
в) частота аутологичных донаций крови и (или) ее компонентов перед операцией определяется лечащим врачом совместно с врачом-трансфузиологом. Последняя аутодонация осуществляется не менее чем за 3 суток до начала оперативного вмешательства;
г) при нормоволемической гемодилюции постгемодилюционный уровень гемоглобина не должен быть ниже 90-100 г/л, а уровень гематокрита не должен быть менее 28%; при гиперволемической гемодилюции поддерживается уровень гематокрита в пределах%
д) интервал между эксфузией и реинфузией при проведении гемодилюции не должен быть более 6 часов. В противном случае контейнеры с кровью помещаются в холодильное оборудование ппи температуре 4 - 6°С;
е) интраоперационная реинфузия крови, собранной во время операции из операционной раны и полостей излившейся крови, и реинфузия дренажной крови не проводится при ее бактериальном загрязнении;
ж) перед трансфузией (переливанием) аутологичной крови и ее компонентов врачом, проводящим трансфузию (переливание) аутологичной крови и (или) ее компонентов, выполняется проба на их совместимость с реципиентом и биологическая проба, как и в случае применения компонентов аллогенной крови.
XIV. Посттрансфузионные реакции и осложнения
88. Выявление и учет реакций и осложнений, возникших у реципиентов в связи с трансфузией (переливанием) донорской крови и (или) ее компонентов, ведутся как в текущий период времени после проведения трансфузии (переливания) донорской крови и (или) ее компонентов, так и спустя неопределенный период времени - несколько месяцев, а при повторной трансфузии - лет после ее проведения.
Основные виды реакций и осложнений, возникающих у реципиентов в связи с трансфузией (переливанием) донорской крови и (или) ее компонентов, указаны в таблице, приведенной в приложении N 4 к настоящим Правилам.
89. При выявлении реакций и осложнений, возникших у реципиентов в связи с трансфузией (переливанием) донорской крови и (или) ее компонентов, заведующий трансфузиологическим отделением или трансфузиологическим кабинетом организации, либо врач-трансфузиолог, назначенный приказом руководителя организации:
а) организует и обеспечивает оказание реципиенту экстренной медицинской помощи;
б) незамедлительно направляет руководителю организации, которая заготовила и поставила донорскую кровь и (или) ее компоненты, уведомление о реакциях и осложнениях, возникших у реципиентов в связи с трансфузией (переливанием) донорской крови и (или) ее компонентами, по рекомендуемому образцу, приведенному в приложении N 5 к настоящим Правилам;
в) передает оставшуюся часть перелитой донорской крови и (или) ее компонентов, а также образцы крови реципиента, взятые до и после трансфузии (переливании) донорской крови и (или) ее компонентов, в организацию, которая заготовила и поставила донорскую кровь и (или) ее и резус-принадлежности донорской крови и (или) ее компонентов, а также для исследования на наличие антиэритроцитарных антител и маркеров гемотрансмиссивных инфекций;
г) осуществляет анализ действий медицинских работников организации, в которой осуществлялась трансфузия (переливание) донорской крови и (или) ее компонентов, в результате которой возникла реакция или осложнение.
XV. Формирование запаса донорской крови и (или) ее компонентов
90. Формирование запаса донорской крови и (или) ее компонентов осуществляется в соответствии с порядком, устанавливаемым в соответствии с частью 6 статьи 16 Федерального закона от 20 июля 2012 г. N 125-ФЗ "О донорстве крови и ее компонентов".
Приложение N 1
к Правилам клинического использования
донорской крови и (или) ее компонентов,
утвержденным приказом Министерства
здравоохранения РФ
от 2 апреля 2013 г. N 183н
Рекомендуемый образец
Протокол трансфузии (переливания) донорской крови
и (или) ее компонентов
1. Ф. И.О. реципиента: __________________ N медицинской карты: ___________
2. Дата трансфузии (переливания) донорской крови и (или) ее компонентов:
"___"__________________ 20__ г.
3. Время начала трансфузии (переливания) донорской крови и (или) ее
компонентов реципиенту: _________________________________________________
4. Время окончания трансфузии (переливания) донорской крови и (или) ее
компонентов реципиенту:__________________________________________________
5. Группа крови реципиента: _____________________________________________
6. Резус-принадлежность: ________________________________________________
7. Фенотип: _____________________________________________________________
8. Определение резус-принадлежности реципиента проводилось:
в лаборатории / экспресс методом: _______________________________________
9. Исследование антител выявлены / не выявлены: _________________________
10. Медицинские показания к проведению трансфузии (переливания) донорской
крови и (или) ее компонентов: ___________________________________________
___________________________________________________Hb_______ Ht _________
11. Трансфузионный анамнез: трансфузии были / не были: __________________
_________________________________________________________________________
12. Трансфузии по индивидуальному подбору в прошлом: были / не были _____
_________________________________________________________________________
13. Реакции и (или) осложнения, возникшие у реципиента в связи с
трансфузией (переливанием) донорской крови и (или) ее компонентов: ______
_________________________________________________________________________
14. Акушерский анамнез (количество беременностей): ______________________
15. Особенности течения (самопроизвольные аборты, гемолитическая болезнь
новорожденного и другое): _______________________________________________
_________________________________________________________________________
16. Макроскопическая оценка крови и (или) ее компонента: пригодна к
переливанию / не пригодна к переливанию: ________________________________
_________________________________________________________________________
17. Данные с этикетки контейнера с кровью и (или) ее компонентом: _______
18. Наименование компонента крови: ______________________________________
19. Наименование организации, заготовившей донорскую кровь и (или) ее
компоненты: _____________________________________________________________
_________________________________________________________________________
20. Дата заготовки донорской крови и (или) ее компонентов: ______________
21. Срок годности донорской крови и (или) ее компонентов: _______________
22. N контейнера донорской крови и (или) ее компонентов: ________________
23. Объем донорской крови и (или) ее компонентов (мл): __________________
24. Код донора крови и (или) ее компонентов (ФИО донора): _______________
25. Группа крови донора крови и (или) ее компонентов: ___________________
26. Резус-принадлежность донора крови и (или) ее компонентов: ___________
┌─────────────────────────────────────────────┐
│ │
│ │
│ │
│ │
│ │
│ │
│ Место для этикетки │
│ │
│ │
│ │
│ │
│ │
└─────────────────────────────────────────────┘
27. Перед трансфузией (переливанием) донорской крови и (или) ее
компонентов проведены контрольные проверки показателей:
Группа крови реципиента ______ Резус-принадлежность реципиента __________
Группа крови донора*__________ Резус-принадлежность донора* _____________
28. При определении показателей использовались реактивы _________________
_________________________________________________________________________
(наименование с указанием серии и срока годности)
29. Проведены пробы на индивидуальную совместимость*:
_________________________________________________________________________
_________________________________________________________________________
указать метод, используемые реактивы (наименование, серию, срок
годности), результат проведения каждой пробы
30. Биологическая проба: ________________________________________________
указать метод, результат проведения пробы
31. Способ трансфузии (переливания) донорской крови и (или) ее
компонентов:_____________________________________________________________
32. Осложнения во время трансфузии (переливания) донорской крови и (или)
ее компонентов: _________________________________________________________
33. Наблюдение за состоянием реципиента:
Артериальное давление, мм рт. ст. | Частота пульса, уд/мин. | Температура, °С | Диурез, цвет мочи | |
Перед переливанием | ||||
Через 1 час после переливания | ||||
Через 2 часа после переливания | ||||
** Через 3 часа после переливания |
34. Врач, проводивший трансфузию (переливание) донорской крови и (или) ее
компонентов: _________________________
______________________________________ ______________________
(ФИО) (подпись)
______________________________
* Указывается при проведении трансфузии (переливания) эритроцитсодержащих
сред
** Указывается при проведении трансфузии (переливания) донорской крови
и (или) ее компонентов в амбулаторных условиях
Приложение N 2
к Правилам клинического использования
донорской крови и (или) ее компонентов,
утвержденным приказом Министерства
здравоохранения РФ
от 2 апреля 2013 г. N 183н
Таблица
подбора доноров крови и (или) ее компонентов, совместимых с реципиентом по Rh-Hr и Кк, при трансфузии (переливании) эритроцитсодержащих компонентов
N п/п | Реципиент | Донор крови и (или) ее компонентов | |
Совместимый | При экстренных показаниях к трансфузии (переливанию) допустим | ||
фенотип | фенотип | фенотип | |
1 | CcDee | CcDee CCDee ccddee ccDee Ccddee | - |
2 | CCDee | CCDee CCddee | - |
3 | CcDEe | Любой фенотип, кроме | |
4 | ccddee | ccddee | Ccddee |
5 | ccDEe | ccDEe ccddee ccDee ccDEE ccddEe | CcDee CcDEe Ccddee CcddEe |
6 |
|
| CCDee |
7 | ccDEE | ccDEE ccddEE | ccDEe CcDEE |
8 |
|
| CcDee CCDee
|
9 | ccDee | ccDee ccddee | CcDee Ccddee |
10 | Ccddee | Ccddee ccddee CCddee | ccddEe |
11 |
|
ccDEe ccddee | CcDee CcDEe |
12 |
|
ccddee | Ccddee |
13 | CcddEe | ccddee Ccddee CcddEe ccddEe CCddee | - |
14 | CCDEe | CCDEe CCDee CCddee | - |
15 | ccddEe | ccddEe ccddEE ccddee | Ccddee CcddEe |
16 | CcDEE | CcDEE ccDEE ccddEE | CcDEe CcddEe ccddEe |
17 |
|
ccddee | Ccddee |
18 | CCddee | CCddee | Ccddee ccddee |
19 | CCDEE | CCDEE | CCDEe CCDee |
20 | CCddEe | CCddEe CCddee | Ccddee ccddee |
21 | CcddEE | CcddEE ccddEE | CcddEe ccddEe ccddee |
22 | ccddEE | ccddEE | ccddEe |
23 |
|
CCddee | CCDee |
24 |
|
| Ccddee ccddee |
25 |
| ccddee ccddEe
| Ccddee CcddEe |
26 |
|
ccddEe ccddEE | CcddEe ccddee |
27 |
| ccddee ccddEe
| Ccddee CcddEe |
28 |
|
ccDEE ccddEE | CcDEe |
29 | kk | kk | - |
30 | Kk | Kk kk KK | - |
31 | KK | KK | Kk kk |
Приложение N 3

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |




