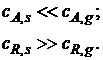 (8.2)
(8.2)
Перепады концентраций ∆сА = сА,g – сА,s и ∆cR = cR,s – cR,g возникают в пограничном диффузионном слое, толщина которого δ зависит от ряда факторов, например в ламинарном потоке, δ = aRe–0,5, где а – линейный размер; Re – число Рейнольдса.
Скорость процесса, протекающего во внешнедиффузионной области, может быть выражена скоростью диффузионного (конвективного) переноса к внешней поверхности с учетом неравенства (8.2)
![]() (8.3)
(8.3)
где S – внешняя поверхность катализатора; βА – коэффициент массоотдачи, зависящий от коэффициента диффузии компонента А и толщины пограничного диффузионного слоя.
При диффузии разных газообразных веществ уравнение (8.3) относится к наиболее медленно диффундирующему компоненту. Как видно из уравнения (8.3), независимо от механизма каталитической реакции и истинных кинетических закономерностей скорость процесса, протекающего во внешнедиффузионной области, формально описывается уравнением первого порядка (прямо пропорциональна концентрации газообразного реагента).
Энергия активации гетерогенно-каталитического процесса в этой области формально определяется температурной зависимостью коэффициентов диффузии. Так как зависимость эта слабая, энергия активации оказывается очень небольшой и даже иногда равной нулю. Поэтому при повышении температуры скорость реакции возрастает быстрее, чем скорость диффузии, и, как следствие, в области высоких температур скорость диффузии начинает лимитировать процесс.
Реализация каталитического процесса во внешнедиффузионной области может сопровождаться некоторыми нежелательными явлениями. Вследствие подобия явлений массо - и теплопередачи при затрудненной диффузии коэффициенты теплопередачи от поверхности катализатора в газовый объем невелики. Для экзотермических реакций это может привести к сильному разогреву катализатора, нежелательному для обратимых процессов, так как это приводит к смещению равновесия в обратную сторону. При протекании последовательных реакций торможение транспорта промежуточного продукта способствует более длительному пребыванию его у поверхности и благоприятствует побочным превращениям, что приводит к снижению селективности.
Скорость процесса при переходе во внешнедиффузионную область очень существенно снижается по сравнению с протеканием реакции в кинетической области; например, скорость окисления аммиака может уменьшиться на 99 %, окисление диоксида серы на 2,5–47 % по сравнению со скоростью в кинетической области.
Переходу процесса из внешнедиффузионной области в кинетическую область способствуют снижение температуры процесса, увеличение линейной скорости газа или интенсивности перемешивания, снижение давления, уменьшение размеров гранул катализатора.
Влияние массопередачи в порах. Каталитическая реакция протекает в основном на поверхности пор катализатора, так как внутренняя поверхность катализатора на несколько порядков больше внешней. Условия транспорта реагентов в поры катализатора поэтому могут оказать существенное влияние на протекание химической реакции.
Если диффузия в порах катализатора протекает быстро по сравнению с химической реакцией, очевидно, вся доступная поверхность катализатора принимает участие в реакции, так как реагенты достигают внутренней поверхности пор, прежде чем прореагируют. В таком случае, хотя между наружной и внутренней частями зерна катализатора перепад концентраций и невелик, наблюдается установившийся диффузионный поток, перемещающий реагирующие молекулы внутрь частиц и выводящий из них образовавшиеся молекулы. Для медленных химических реакций полезной оказывается вся внутренняя поверхность катализатора.
Такие медленные реакции можно противопоставить быстрой реакции на очень активном катализаторе, при которой реагирующие вещества превращаются в конечные продукты еще до того, как проникают в глубь пор. Около внешней поверхности зерна возникает резкий градиент концентраций, и молекулы реагентов быстро диффундируют наружу. В результате реакция почти целиком протекает на внешней поверхности катализатора, а внутренняя часть пористой структуры не используется.
Таким образом, в зависимости от соотношения интенсивности двух параллельных протекающих процессов – диффузии в поры и химической реакции – внутренняя поверхность катализатора используется с большей или меньшей степенью эффективности.
Стадия адсорбции. Определяющую роль в ходе гетерогенно-каталитического процесса играет стадия адсорбции реагентов на поверхности катализатора. Характер адсорбции в значительной степени влияет на вид кинетических уравнений, необходимых для расчета каталитических реакторов. Рассмотрим поэтому некоторые особенности стадии адсорбции.
При физической адсорбции, как правило, очень быстро устанавливается равновесие между адсорбированными частицами, находящимися в газовой фазе, т. е. равенство скоростей адсорбции и обратного ей процесса десорбции. Считают, что физическая адсорбция вызывается теми же неспецифическими силами межмолекулярного взаимодействия, что и конденсация паров.
Теплота физической адсорбции невелика; она близка к теплоте конденсации и составляет обычно 10–40 кДж/моль. Как правило, физическая адсорбция играет существенную роль при понижении температуры газа ниже критической, т. е. когда газ находится в виде пара.
Хемосорбция может протекать при температуре и выше, и ниже критической температуры адсорбента. От физической адсорбции ее отличает, прежде всего, значительно большая специфичность, т. е. зависимость от химической природы адсорбента и адсорбата. Значения теплоты хемосорбции близки к значениям теплоты химических реакций. Хемосорбированные вещества удалить с поверхности адсорбента значительно труднее, чем при физической адсорбции, причем десорбция может сопровождаться химическими реакциями. Например, при термической десорбции кислорода с угля (кислород хемосорбируется на угле очень прочно) вместо кислорода выделяется смесь СО и СО2.
Хемосорбция нередко протекает сравнительно медленно, со скоростью, определяемой наличием активационного барьера (отсюда название «активированная адсорбция»). Процесс хемосорбции может состоять из двух стадий: сначала происходит быстрая физическая адсорбция газа, а затем он вступает в медленную химическую реакцию с поверхностью твердого тела.
При низких температурах скорость хемосорбции так мала, что практически наблюдается только физическая адсорбция. Наоборот, при высоких температурах физическая адсорбция почти незаметна и происходит лишь хемосорбция.
Скорость гетерогенно-каталитических реакций пропорциональна поверхностным концентрациям адсорбированных молекул. Так как на практике часто можно считать, что на поверхности катализатора имеет место адсорбционно-десорбционное равновесие, о поверхностных концентрациях реагентов можно судить по равновесному распределению молекул адсорбата между поверхностью твердого тела и газовой фазой. Это распределение зависит от давления, температуры, природы адсорбента и адсорбата, от площади адсорбента. Принято оценивать равновесное распределение по изотермам адсорбции, показывающим, как количество адсорбированного вещества зависит от равновесного парциального давления данного газа при постоянной температуре.
Существует несколько видов изотерм адсорбции. Рассмотрим вывод изотермы адсорбции Ленгмюра. В основе этого вывода лежит несколько допущений, учет которых приводит к более сложным уравнениям. Допущения эти таковы:
– адсорбированные частицы связаны с определенными локализованными центрами на поверхности адсорбента;
– каждый центр может присоединять только одну адсорбирующуюся частицу;
– энергия адсорбированных частиц на всех центрах поверхности одинакова и не зависит от присутствия или отсутствия других адсорбирующихся частиц на соседних центрах.
Влияние характера адсорбции на кинетику гетерогенного катализа. Для расчета каталитического реактора необходимо иметь конкретный вид кинетического уравнения, т. е. зависимость скорости процесса от концентрации участников, температуры и т. д. По аналогии с гомогенными системами скорость каталитической реакции зависит от поверхностных концентраций адсорбированных частиц. На практике известны не поверхностные, а объемные концентрации компонентов в газовой фазе или их парциальные давления. Поэтому обычно кинетические уравнения гетерогенно-каталитических реакций представляют в виде зависимости скорости от концентрации реагентов в газовой фазе (парциальных давлений).
Вывод кинетических уравнений достаточно сложен. Строгий учет всех химических и физических явлений не всегда возможен и поэтому при разработке теории часто прибегают к значительным упрощениям. Наиболее распространенной является кинетическая модель Ленгмюра – Хиншельвуда. В рамках этой модели предполагается, что поверхностные концентрации реагирующих веществ являются равновесными по отношению к их объемным концентрациям, а молекулы в адсорбированном слое довольно подвижны и, прежде чем десорбироваться, подвергаются многочисленным столкновениям.
При этих допущениях адсорбционное равновесие описывается изотермой Ленгмюра, а скорость реакции определяется законом действующих поверхностей (аналогом закона действующих масс для химических процессов, протекающих на поверхности твердого тела).
Вопросы и упражнения
для повторения и самостоятельной работы
1. Какие вещества называются катализаторами?
2. В чем заключается природа действия катализаторов?
3. Может ли катализатор сместить равновесие химической реакции?
4. Перечислите основные технологические характеристики твердых катализаторов и дайте их определения.
5. Какая кинетическая модель гетерогенных процессов подходит для описания каталитической реакции на твердом пористом катализаторе?
6. Какие отрицательные последствия может вызвать протекание каталитической реакции на твердом катализаторе во внешне диффузионной области?
7. Что такое коэффициент эффективности использования поверхности катализатора?
СПИСОК ЛИТЕРАТУРЫ
1. , Каргин азотной кислоты. – М.: Химия, 1970.
2. Бесков B. C., Сафронов B. C. Общая химическая технология и основы промышленной экологии. – М.: Химия, 1999.
3. Биомасса как источник энергии / под ред. С. Соуфера, О. Заборски. – М.: Мир, 1985.
4. Биотехнология / под ред. . – М.: Наука, 1984.
5. , Отвагина серной кислоты. – М.: Химия, 1985.
6. Газожидкостные реакции. – М.: Химия, 1972.
7. Введение в моделирование химико-технологических процессов. – М.: Химия, 1982.
8. , Производство метанола. – М.: Химия, 1973.
9. Химическая термодинамика. – М.: Химия. 1975.
10. Катализ в промышленности: в 2 т. / Б. Лич, Ю. Сандерс, Э. Шлюссмахер и др.; под ред. Б. Лича. – М.: Мир, 1986. – Т. 1–2.
11. , Макаров автоматизированные производственные системы в химической промышленности. – М.: Химия, 1990.
12. , Троицкая воздушного бассейна от загрязнений вредными веществами химических предприятий. – М.: Химия, 1979.
13. Лебедев и технология основного органического и нефтехимического синтеза. – М.: Химия, 1975.
14. Инженерное оформление химических процессов. – М.: Химия, 1969.
15. , X., Семенов и практика химической энерготехнологии. – М.: Химия, 1988.
16. Общая химическая технология: в 2 ч. / под ред. . – 4-е изд., перераб. и доп. – М.: Высш. шк., 1984. – Ч. 1–2.
17. Позин минеральных удобрений. – 5-е изд. перераб. – Л.: Химия, 1983.
18. Производство азотной кислоты в агрегатах большой единичной мощности / под ред. . – М.: Химия, 1985.
19. Процессы и аппараты химической технологии: в 5 т. Т. 1: Основы теории процессов химической технологии / под ред. A. M. Кутепова. – М.: Логос, 2000.
20. Синтез аммиака/, , и др. – М.: Химия, 1982.
21. , Волжинский реакторы в примерах и задачах. – Л.: Химия, 1986.
22. Технология неорганических веществ и минеральных удобрений / Е. Я. Мельников, В. П. Сaтганова, A. M. Наумова и др. – М.: Химия, 1983.
23. Франк-Каменецкий и теплопередача в химической кинетике. – М.: Наука, 1987.
24. Химия нефти и газа/ под ред. и . – Л.: Химия, 1981.
25. , Кнорре химической кинетики. – 4-е изд., перераб. и доп. – М.: Высш. шк., 1984.
26. , , Беренгартен химическая технология: учебник для вузов. – 3-е изд., перераб. и доп. – М.: ИКЦ «Академкнига», 2003.
27. Бесков химическая технология. – М.: ИКЦ «Академкнига», 2005.
Юрий Борисович Швалёв
Валерий Васильевич Коробочкин
ОБЩАЯ ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ
Химические процессы и реакторы
Учебное пособие
Редактор
Подписано к печати Формат 60×84/16. Бумага «Классика». Печать RISO. Усл.печ.л. 10,46. Уч.-изд.л. 9,47. Заказ . Тираж экз. | ||
| Томский политехнический университет Система менеджмента качества Томского политехнического университета сертифицирована NATIONAL QUALITY ASSURANCE по стандарту |
|
|
![]()

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 |




