К тяжелым металлам относят более 40 химических элементов периодической системы с атомными массами свыше 50 а. е.м. Иногда тяжелыми металлами называют элементы, которые имеют плотность более 7-8 г/см3 (кроме благородных и редких), а I - иногда и металлы с плотностью 5 г/см3 (таблица 38). Оба определения условны, и перечни тяжелых металлов по этим формальным признакам не совпадают. Число наиболее опасных тяжелых металлов, если учитывать их токсичность, стойкость и способность накапливаться во внешней среде, а также масштабы распространения, значительно меньше. Это — ртуть, свинец, кадмий, кобальт, никель, цинк, олово, сурьма, медь, молибден, ванадий, мышьяк.
Поступление тяжелых металлов в биосферу вследствие техногенного рассеяния осуществляется разнообразными путями. Важнейшим из них является выброс при высокотемпературных процессах (черная и цветная металлургия, обжиг цементного сырья, сжигание минерального топлива). Кроме того, источником загрязнения биоценозов могут служить орошение водами с повышенным содержанием тяжелых металлов, внесение осадков бытовых сточных вод в почвы в качестве удобрения, вторичное загрязнение вследствие выноса тяжелых металлов из отвалов рудников или металлургических предприятий водными или воздушными потоками, поступление больших, количеств тяжелых металлов при постоянном внесении высоких доз органических, минеральных удобрений и пестицидов, содержащих тяжелые металлы.
Рассеивание металлов может происходить на сотни и тысячи километров, приобретая межконтинентальные масштабы. В глобальных масштабах происходит процесс, называемый сегодня «металлическим прессом на биосферу». Ведущая роль в переносе металлов-загрязнителей принадлежит циркуляционным процессам, которые, в свою очередь, определяют особенности их пространственного распределения.
Техногенные загрязнения включают в кругооборот значительно большие количества тяжелых металлов по сравнению с их природными величинами, усугубляют опасность воздействия на человека уже не биотических, а токсических концентраций указанных элементов через почву, воду, воздух, растительные и животные организмы.
ПЕСТИЦИДЫ
Человек создал много химических препаратов, преследуя свои хозяйственные и иные цели. Многочисленную группу ядохимикатов представляют пестициды.
Пестициды (от лат. pestis — зараза и caedere — убивать), ядохимикаты, химические препараты для защиты сельскохозяйственных растений от вредителей, болезней и сорняков, а также для уничтожения паразитов сельскохозяйственных животных, вредных грызунов и др. К пестицидам относятся также средства, привлекающие или отпугивающие насекомых, регулирующие рост и развитие растений, применяемые для удаления листьев, цветов, завязей и др.
Дефолианты (от лат. de — движение вниз и folium — лист), химические вещества (бутифос, бутилкаптакс, тидрел, пуривел, хлорад магния, диоксин и др.), предназначенные для провоцирования искусственного опадания листвы растений (например, для облегчения механизированной уборки хлопка). Без строжайшего соблюдения доз, мер предосторожности дефолианты представляют серьезную опасность для человека и животных.
Зооциды (от греч. zoon — животное и... цид(ы)), химические вещества, предназначенные для уничтожения вредных, преимущественно позвоночных, животных-грызунов (родентициды), в частности мышей и крыс (ратициды), а также птиц (авициды), сорной рыбы (ихтиоциды) и др.
Арборициды (от лат. arbos — дерево и...цид(ы)), химические вещества, предназначенные для уничтожения нежелательной древесной или кустарной растительности.
Акарициды (от греч. akari — клещ и...цид(ы)), химические вещества, предназначенные для уничтожения вредных клещей. Различают 2 группы акарицидов: 1) специфического действия, уничтожают только клещей и безвредны для других членистоногих (неорон, кельтан, тедион, эфирсуль); 2) неспецифические— уничтожают не только клещей, но и насекомых (инсектоакарициды).
Инсектициды (от лат. insecta — насекомые и...цид(ы)), пестициды, предназначенные для борьбы с нежелательными (с точки зрения человека) в хозяйствах и природных сообществах насекомыми.
Фунгициды (от лат. fungus — гриб и...цид(ы)), химические вещества, предназначенные для борьбы с грибами — возбудителями болезней, разрушающих, древесные конструкции и повреждающих хранящиеся материальные ценности.
Детергенты (от лат. detergeo — стираю), химические соединения, понижающие поверхностное натяжение воды и используемые в качестве моющего средства или эмульгатора. Детергенты — широко распространенные и опасные для человека, животных и растений химические загрязнители воды, водоемов, почв.
Пестициды применяются в различных формах: растворы, суспензии, аэрозоли, пены, газы, пары, пыль, порошки, пасты, гранулы, капсулы.
Попадание пестицидов в атмосферу осуществляется непосредственно при их использовании в виде газов, паров, аэрозолей или при распылении любых форм пестицидов с самолета. С воздушными массами они могут переноситься на большие расстояния и вызывать загрязнение окружающей среды там, где пестициды вообще не применялись или использовались в меньших количествах.
Все пестициды являются ядовитыми веществами не только для определенной формы жизни, но и для полезных насекомых и микроорганизмов, животных, птиц и человека. В идеальном случае пестицид, оказав требуемое воздействие на вредителя, должен был сразу разрушиться, образовав безвредные продукты разложения. Однако большинство пестицидов представляют собой устойчивые трудноразлагаемые соединения, у которых непосредственно используется 4-5% внесенного количества, а остальная масса рассеивается в агроэкосистеме, попадая в почвы, растения и другие компоненты окружающей среды, что создает сложные экологические проблемы.
При внесении в почву пестициды подвергаются многочисленным влияниям биотического и небиотического характера, которые определяют их дальнейшее поведение, трансформацию и в конечном счете минерализацию. Под устойчивостью пестицида понимают его способность определенное время сохраняться в почвах, измеряемую периодом полураспада, то есть временем, необходимым для разрушения 50% внесенного в почву пестицида. Характер и скорость процессов разложения зависят от химической природы препарата, а также от водно-физических характеристик и химического состояния почвы.
диоксины
В большую группу диоксинов и диоксиноподобных соединений входят как сами полихлорированные дибензо- р-диоксины (ПХДД) и дибензофураны (ПХДФ), которые по своей химической структуре являются трициклическими ароматическими соединениями, так и полихлорированные бифенилы (ПХВ), поливинилхлорид (ПВХ) и ряд других веществ, содержащих в своей молекуле атомы хлора. Это чужеродные живым организмам соединения, попадающие в окружающую среду с продукцией или отходами многих технологий. Диоксины найдены везде — в воздухе, почве, донных отложениях, рыбе, молоке (в том числе и грудном), овощах и т. д.
Отличительная черта представителей этой группы соединений — чрезвычайно высокая устойчивость к химическому и биологическому разложению, они способны сохраняться в окружающей среде в течение десятков лет и переносятся по пищевым цепям. Эти вещества — супертоксиканты, они являются универсальными клеточными ядами, поражающими все живое.
Диоксины не производятся промышленно, но они возникают при производстве других химических веществ в виде примесей, например: при синтезе гексахлорфенола, хлорированных фенолов, гербицидов на основе гексахлорбензола и хлордифениловых эфиров. Известна трагедия вблизи г. Севезо (Италия), где на заводе произошел выброс трихлорфенола, содержащего примерно 2-3 кг ТХДД. Более 2/3 этого количества отложилось на площади в 15 га на расстоянии около 500 м от завода. Период полураспада ТХДД в почве составляет примерно 10-12 лет. Источником поступления диоксинов в окружающую среду является и нарушение правил захоронения промышленных отходов, в результате чего также происходит сильное загрязнение почв.
К другим источникам диоксинов относятся: термическое разложение технических продуктов, сжигание осадков сточных вод, муниципальных, медицинских и Опасных отходов (например, ПХБ и изделий из ПВХ); металлургическая и металлообрабатывающая промышленность, выхлопные газы автомобилей, целлюлозно-бумажная промышленность, лесные пожары (леса, обработанные хлорфенольными пестицидами), хлорирование питьевой воды и др. Известное еще с начала XX в. заболевание, называемое хлоракне, было квалифицировано в 30-е гг. как профессиональная болезнь рабочих хлорных производств. Хлоракне — тяжелая форма угрей, уродующих кожу лица. Заболевание может длиться годами и практически не поддается лечению. Пик выброса диоксинов пришелся на 60-70-е гг. XX в., в результате расширения производства отбеленной бумаги, а также веществ, в технологии синтеза которых использовался хлор.
У человека (как в результате профессиональной деятельности, так и влияния окружающей среды) в целом описано довольно много признаков и симптомов различных заболеваний, которые можно свести к следующим:
кожные проявления — хлоракне, гиперпигментация и др.;
нарушение работы различных физиологических систем — расстройство пищеварения (рвота, тошнота, непереносимость алкоголя и жирной пищи), нарушения в сердечно-сосудистой системе, мочевыводящих путях, поджелудочной железе и др.;
неврологические эффекты — головные боли, невропатия, потеря слуха, обоняния, вкусовых ощущений, нарушение зрения;
психические эффекты — нарушение сна, депрессия, немотивированные приступы гнева.
Общее состояние проблемы загрязнения среды диоксинами отражено в Государственном докладе «О состоянии окружающей природной среды Российской Федерации»: «Среди химических веществ, загрязняющих Природные среды, особое место занимают вещества 1 класса опасности, или чрезвычайно опасные, для которых установлены минимальные значения предельно допустимых концентраций... Выборочные обследования локальных источников диоксинов и родственных им веществ, проведенные Роскомгидрометом в 1993 г., показали их присутствие в поверхностных водах, питьевой воде, городских почвах и атмосферном воздухе (таблица 39).
Таблица 39
Содержание диоксинов в поверхностных и питьевых водах
Объект исследования | Содержание в долях ПДЛ |
Вода р. Шани | 1,7-21,6 |
Вода Учинского водохранилища | 1,5 |
Питьевая вода г. Москва | |
Новозападная водопроводная станция | 0,5 |
Восточная водопроводная станция | 1,1-4,0 |
Питьевая вода г. Кондрово | 1,7-3,5 |
Питьевая вода г. Чапаевск | <0,7 |
Несмотря на то, что диоксины в питьевой воде обследованных городов присутствуют в количествах, не превышающих ПДК, сам факт наличия токсичных веществ, обладающих способностью накапливаться в живом организме, требует особого внимания.
СОЕДИНЕНИЯ СЕРЫ, ФОСФОРА И АЗОТА
При оценке загрязнения биосферы соединениями фосфора важны техногенные пути их поступления. Значительные количества фосфорных соединений входят в состав моющих средств и с их остатками попадают в сточные воды. Стиральные порошки содержат 10-12% пирофосфата калия или от 4-5 до 40-50% триполифосфата натрия и некоторые другие фосфорсодержащие компоненты. Фосфор также входит в состав инсектицидов, например, хлорофоса. Вместе с промышленными и бытовыми сточными водами соединения фосфора могут поступать в почвы и почвенно-грунтовые воды.
В биосфере азот присутствует в газообразной форме, в виде соединений азотной и азотистой кислот, солей аммония, а также входит в состав разнообразных органических соединений.
Техногенные выбросы азота в воздушную среду в основном включают оксид азота и его диоксид. Оксиды азота активно участвуют в фотохимических реакциях, продуцируя озон и азотную кислоту.
В настоящее время большую проблему представляет нарушение толщины озонового слоя, на уменьшение которого могут оказывать влияние неполные оксиды азота, вступающие в реакцию окисления от N2O до NO2 и использующие кислород озонового слоя. Разрушение озонового экрана связывают с оксидом азота, который служит источником образования других оксидов, катализирующих фотохимическую реакцию разложения молекул озона.
О значительном загрязнении соединениями азота свидетельствует повышение уровня концентрации нитратов : в природных водах в 2-4 раза и более, а также повышение концентраций аммонийного и нитратного азота до токсичных уровней, что может привести к специфическим заболеваниям типа метгемоглобинемии людей и животных.
Как правило, максимальное содержание нитратов обнаруживают в продукции, выращенной на приусадебных участках и арендуемых полях и огородах, где внесение удобрений не контролируется. При взаимодействии нитритов и аминов в живых организмах образуются нитрозамины, являющиеся канцерогенами и способные вызывать нарушения хромосомного аппарата и наследственные уродства.
Фосфор и азот влияют на водные экосистемы. Эвтрофирование, или ненормальное повышение биологической продуктивности водных объектов и почвы, происходит в результате накопления избытка биогенных элементов (веществ).
В большинстве водных экосистем лимитирующим биогенным элементом является фосфор, в меньшей степени азот; в такой экосистеме наблюдается низкая продуктивность и как следствие — чистая прозрачная вода, обогащенная кислородом. На дне появляется осадок, растительность начинает вторгаться в экосистему с берегов, экосистема «стареет» и «умирает»: водоем мелеет и зарастает.
Признаком «болезни» является развитие сине-зеленых водорослей или других фотосинтезирующих водорослей, вызывающих «цветение» воды. Вода в пресноводных водоемах становится непригодной не только для питья, но и для промышленных нужд, возникает ряд опасностей и неразрешимых пока проблем.
Вследствие эвтрофирования некоторые наземные экосистемы также перерождаются: из них исчезают виды растений, характерные для условий местопроизрастания.
Диоксид серы составляет 95% всех техногенных выбросов серосодержащих веществ в атмосферу.
Сернистый газ, окисляясь и взаимодействуя с водой, выпадает в виде кислых дождей. Осадки подкисляют почвы. Из почвенного поглощающего комплекса водород вытесняет обменные основания (Ca2+, Mg2+). Увеличивается фитотоксичность почв за счет увеличения подвижного алюминия. Сера закрепляется в почве в форме алунита КА13(ОН)6(SO4)2. Часть серы сорбируется фульвокислотами. Значительно повышается растворимость всех гумусовых веществ, происходит их вымывание из минеральных горизонтов.
Резко изменяется состав и функции микробиоты: уменьшается масса бактерий, увеличивается масса грибов, среди них появляются фитопатогенные виды; снижается скорость денитрификации и азотфиксации, снижается численность и активность почвенной фауны. Блокируется цикл азота на стадии аммиака. Подавляется разложение органических остатков. Модергумусные почвы трансформируются в грубогумусные, усиливается процесс подзолообразования.
В итоге этих изменений плодородие почвы сначала несколько повышается за счет покрытия дефицита серы и азота, а затем значительно и устойчиво снижается. В сельском хозяйстве почвенное плодородие можно восстановить известкованием почвы и соответствующей агротехникой с внесением удобрений. В лесном хозяйстве воздушное загрязнение в сочетании с ухудшением почвенных условий приводит не только к падению прироста древесины, но и к усыханию древостоев и дигрессии лесных биогеоценозов.

ФРЕОНЫ
Фреоны (хладоны) — это группа фторсодержащих ;(могут также содержать хлор и бром) углеводородов жирного ряда; газы или летучие жидкости. Благодаря своим термодинамическим свойствам фреоны нашли широкое применение в практике как хладоносители в холодильных машинах.
При контакте с открытым пламенем фреоны разлагаются с образованием токсичных дифтор - и фторхлорфосгена, устойчивы к действию серной кислоты и концентрированных щелочей, не взаимодействуют с большинством металлов. Фреоны нетоксичны для организма, Однако их воздействие на окружающую среду может иметь и негативные последствия — образование озоновой «дыры».
Хладоны обладают привлекательными физико-химическими свойствами, малотоксичны, просты в использовании, не обладают коррозирующим действием, не образуют взрывоопасных смесей с воздухом, имеют исключительно высокую пламеподавляющую способность.
Хладоны применяют в качестве хладагентов, пропеллентов в аэрозольных упаковках косметических Средств, как компоненты огнетушащих составов, растворители и т. д. В промышленных масштабах хладоны стали применять с начала 30-х гг. XX в.
В 1974 г. учеными было высказано предположение о ом, что хладоны разрушают озоновый слой, защищающий земные организмы от губительного действия ультрафиолетового излучения Солнца. Обоснованность гипотезы (Rowland F. S., Molina M. J.) была подтверждена прямыми измерениями.
Озоноразрушающее действие хладонов приводит к образованию так называемых озоновых дыр, т. е. к снижению концентрации озона, что расценивается как серьезная экологическая опасность. В 1987 г. достигнуто международное соглашение — Монреальский протокол, обязывающий все страны-участницы соглашения с 1994 г. ограничить, а к 2000 г. полностью прекратить производство и применение всех озоноразрушающих материалов.
8.2. ВОЗДУХ КАК ФАКТОР СРЕДЫ ОБИТАНИЯ
Воздушная среда, в которой осуществляется деятельность человека, характеризуется физическими параметрами, химическим составом, ионным составом и другими показателями.
Физические параметры воздуха: температура, относительная влажность, скорость, барометрическое давление. Первые три параметра определяют процесс терморегуляции организма, т. е. поддержание температуры тела в пределах 36-37°С. Она обеспечивает равновесие между количеством тепла, непрерывно образующимся в организме в процессе обмена веществ, и излишками тепла, непрерывно отдаваемыми в окружающую среду, т. е. поддерживает тепловой баланс организма человека.
Терморегуляция — физиологический процесс, контролируемый центральной нервной системой. Различают химическую и физическую терморегуляцию.
Основное значение имеет физическая терморегуляция, посредством которой осуществляется отдача тепла организмом в окружающую среду. Этот процесс может идти тремя путями:
1. В виде инфракрасных лучей, излучаемых поверхностью тела в направлении окружающих предметов с более низкой температурой (радиация); таким путем теряется » 45% всей тепловой энергии, вырабатываемой организмом;
2. Нагревом воздуха, омывающего поверхность тела (конвекция), при этом теряется » 30% тепла;
3. Испарением пота, теряется » 13% тепла через органы дыхания и около 5% тепла расходуется на нагревание принимаемой пищи, воды и вдыхаемого воздуха.
Теплоотдача радиацией и конвекцией происходит в том случае, если температура окружающего воздуха ниже температуры тела. В противном случае теплоотдача возможна только испарением пота. Причем скорость испарения зависит от относительной влажности воздуха. Если влажность воздуха превышает 80%, теплоотдача испарением пота затруднена и может наступить перегрев организма, именуемый тепловой гипертермией и судорожной болезнью, которые в дальнейшем могут привести к тепловому удару, протекающему с потерей сознания, повышением температуры тела человека до 40-41°С и другими признаками тяжелого заболевания. Интенсивное потоотделение чревато угрозой дегидратации (обезвоживания) организма. Потери воды за счет испарения при температуре окружающей среды 37,8°С в состоянии покоя человека достигали 300 г. ч.-1 При движении они более значительны.
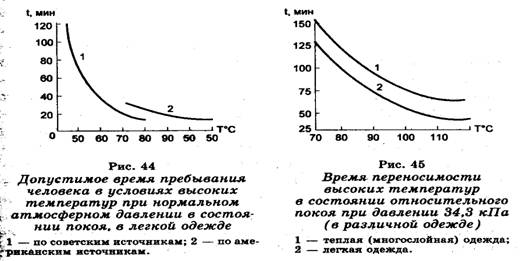
Если температура воздуха и окружающих стен больше 60°С, организм человека не способен сохранять тепловой баланс даже за счет потоотделения, вследствие чего начинается процесс накопления тепла в организме. Допускаемая продолжительность воздействия высоких температур при нормальном атмосферном давлении (» 101 кПа) приведена на рис. 44, а при пониженном барометрическом давлении — на рис. 45.
Неблагоприятное воздействие на организм человека оказывает не только высокая, но и низкая температура воздуха. Переохлаждения (гипотермия) вызывают заболевания периферической нервной системы. Наибольший процент обморожений и смертельных случаев в результате переохлаждения наблюдается при сочетании низкой температуры, высокой влажности и большой подвижности воздуха.

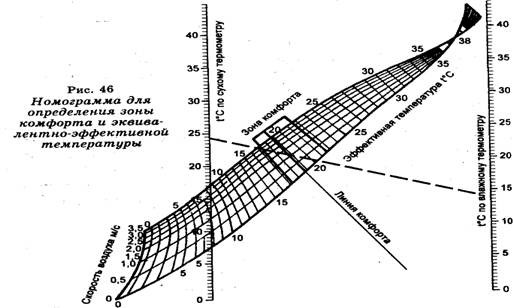
Совместное действие температуры, влажности и подвижности воздуха определяют через эквивалентно-эффективную температуру по специальной диаграмме (рис. 46).
Физические параметры воздуха необходимо учитывать при организации всех видов деятельности. Особое значение имеют параметры микроклимата помещений, т. е. температура, относительная влажность и подвижность воздуха. Кроме того, следует иметь ввиду, что скорость воздуха при определенной величине представляет серьезную опасность для сооружений, технических устройств, конструкций, так как может создавать большие ветровые нагрузки, способные производить разрушительные действия.
Что касается барометрического давления, то его величина по понятным соображениям не нормируется, хотя его колебания оказывают существенное влияние на здоровье людей.
Нормальное кислородное обеспечение организма возможно при снижении давления до 25-26 кПа. На высоте 3000 м человек подвергается опасности заболеть «горной болезнью». От повышенного барометрического давления патологические симптомы появляются у человека при давлении более 392...843 кПа. Интервал давлений порядка 73-126 кПа особых беспокойств здоровым людям не доставляет. Для безопасности человека важно не само давление, укладывающееся в указанные пределы, а скорость его изменения.
Химический состав. Чистый воздух имеет следующий химический состав в % по объему: азот » 78,08; кислород » 20,94; аргон, неон и другие инертные газы » 0,94; углекислый газ » 0,03; прочие газы » 0,01. В воздухе могут находиться вредные вещества различного происхождения в виде газов, паров, аэрозолей, в том числе радиоактивные.
Вредное вещество — вещество, которое при контакте с организмом человека в случае нарушения требований ^безопасности может вызывать заболевания или отклонения в состоянии здоровья, обнаруживаемые современными методами как в процессе контакта с ним, так и в отдаленные сроки жизни настоящего и последующего поколений. Из данного определения следует, что все химические соединения потенциально являются вредными веществами. Вредные вещества можно классифицировать по разным признакам:
По характеру воздействия на организм: общетоксические; раздражающие; сенсибилизирующие; канцерогенные; мутагенные; влияющее на репродуктивную функцию.
По классам химических соединений: органические; неорганические; элементоорганические.
По степени токсичности: чрезвычайно токсичные; высокотоксичные; умеренно токсичные; малотоксичные.
По степени воздействия на организм: чрезвычайно опасные; высокоопасные; умеренно опасные; малоопасные.
Для предотвращения негативных последствий воздействия загрязняющих веществ на отдельные компоненты природной среды необходимо знать их предельные уровни, при которых возможна нормальная жизнедеятельность и функционирование организма. Основной величиной экологического нормирования содержания вредных химических соединений в компонентах природной среды является предельно допустимая концентрация (ПДК). ПДК — это такое содержание вредного вещества в окружающей среде, которое при постоянном контакте или при воздействии за определенный промежуток времени практически не влияет на здоровье человека и не вызывает неблагоприятных последствий у его потомства. При определении ПДК учитывается не только влияние загрязняющего вещества на здоровье человека, но и его воздействие на животных, растения, микроорганизмы, а также на природные сообщества в целом.
Для санитарной оценки воздушной среды используется несколько видов предельно допустимых концентраций вредных веществ, которые установлены на основе рефлекторных реакций организма человека на присутствие в воздухе вредных веществ.
ПДКрз — предельно-допустимая концентрация вредного вещества в воздухе рабочей зоны, мг/м3. Эта концентрация не должна вызывать у работающих при ежедневном вдыхании в течение 8 ч за все время рабочего стажа каких-либо заболеваний или отклонений от нормы в состоянии здоровья, которые могли бы быть обнаружены современными методами исследования непосредственно во время работы или в отдаленные сроки. При этом рабочей зоной считается пространство высотой 2 м над уровнем пола или площадки, на которой расположены места постоянного или временного пребывания работающих.
ПДКмр — максимальная разовая концентрация вредного вещества в воздухе населенных мест, мг/м3, которая не должна вызывать рефлекторных реакций в организме человека.
ПДКсс — среднесуточная предельно допустимая концентрация вредного вещества в воздухе населенных мест, мг/м3. Эта концентрация вредного вещества не должна оказывать прямого или косвенного вредного воздействия на организм человека в условиях неопределенно долгого круглосуточного вдыхания.
В настоящее время действуют «ПДК вредных газов, паров и аэрозолей в воздухе рабочей зоны», установленные для 445 загрязняющих веществ, и «ПДК вредных веществ в атмосферном воздухе населенных мест», включающие 109 загрязняющих веществ.
В качестве примера дадим характеристику некоторым загрязняющим веществам.
Пыли. В зависимости от происхождения принято различать органические и неорганические пыли. К органическим относятся растительная и животная пыль, а также пыль некоторых синтетических веществ. К неорганическим относятся металлическая и минеральная (кварц, асбест, цемент и др.) пыли.
При оценке токсического действия пыли необходимо учитывать такие факторы, как дисперсность, форма частиц, растворимость, химический состав. Наибольшую опасность представляют пыли с частицами размером до 5 мкм, частицы этого размера задерживаются в легких, проникая в альвеолы, и частично или полностью растворяются в лимфе. Частицы большого размера задерживаются в верхних дыхательных путях и выводятся наружу при выдохе или откашливаний. В зависимости от химического состава пыль может оказывать отравляющее или механическое действие. К пылям вредных химических веществ относятся аэрозоли ДДТ, хромового ангидрида, свинца, ртути и др. Аэрозоли этих соединений могут не только оказывать местное воздействие на верхние дыхательные пути, но и проникать в легкие и желудочно-кишечный тракт и вызывать общее отравление организма.
Неядовитые пыли при значительных концентрациях также оказывают вредное воздействие на организм человека. Они засоряют или раздражают слизистые оболочки глаз, кожу, верхние дыхательные пути и вызывает различные легочные заболевания — пневмокониозы. В зависимости от природы пыли пневмокониозы могут Быть различных видов: силикоз — при действии пыли Свободного диоксида кремния; антракоз — при вдыхании угольной пыли; асбестоз — при вдыхании асбестовой пыли.
Аммиак (NH3) — бесцветный газ с резким запахом. Хорошо растворим в воде, перевозится и хранится в сжиженном состоянии. Аммиак является горючим газом, горит при наличии постоянного источника огня. Пары аммиака образуют с воздухом взрывоопасные смеси. Емкости с аммиаком могут взрываться при нагревании. Общетоксические эффекты в основном обусловлены действием аммиака на нервную систему. Последствиями тяжелой интоксикации является снижение интеллектуального уровня с выпадением памяти, неврологические симптомы: тремор, нарушение равновесия, тики, понижение болевой и тактильной чувствительности, головокружение, нистагм, гиперрефлексия. Последствиями острого отравления могут быть помутнение хрусталика, роговицы, даже ее прободение и потеря зрения, охриплость или полная потеря голоса и различные хронические заболевания (бронхит, эмфизема легких и др.). В случае малых концентраций наблюдается незначительное раздражение глаз и верхних дыхательных путей. При средних концентрациях наблюдается сильное раздражение в глазах и в носу, частое чихание, слюнотечение, небольшая тошнота и головная боль, покраснение лица и потоотделение. При воздействии очень высоких концентраций уже через несколько минут наступают мышечная слабость с повышенной рефлекторной возбудимостью, резко снижается слух.
ПДКмр - 0,2 мг/м3, ПДКсс — 0,2 мг/м3.
Окись углерода (СО) — бесцветный газ без запаха и вкуса, плохо растворяется в воде; в сжиженном состоянии — бесцветная прозрачная жидкость. СО — негорюч. Пределы воспламеняемости окиси углерода в смеси с воздухом 12,5-74,2%, смесь двух объемов с одним объемом кислорода взрывается при наличии открытого пламени. Окись углерода — вещество преимущественно общеядовитого действия — яд гемоглобина. СО вытесняет кислород из оксигемоглобина, содержание кислорода может снижаться до 8% (аноксемия). Окись углерода способна оказывать непосредственное токсическое действие на клетки, нарушая тканевое дыхание. СО влияет на углеводный и фосфорный обмен. При действии окиси углерода наблюдается тяжесть и ощущение сдавливания головы, сильная боль во лбу и висках, головокружение, шум в ушах, покраснение и жжение кожи лица, дрожь, чувство слабости и страха, жажда, учащение пульса, пульсация височных артерий, тошнота, рвота. В дальнейшем появляется оцепенелость, слабость и безучастность, нарастает сонливость. Температура тела может повышаться до 38-40°С.
ПДКмр — 3 мг/м3, ПДКсс — 1 мг/м3
Хлор (С12) — зеленовато-желтый газ с характерным резким удушливым запахом, малорастворим в воде, растворим в четыреххлористом титане и четыреххлористом кремнии. Является сильным окислителем. Хлор тяжелее воздуха, скапливается в подвалах, низинах местности, хранится и перевозится в сжиженном состоянии. Хлор взрывоопасен в смеси с водородом, негорюч, но пожароопасен. Емкости с хлором могут взрываться ;при нагревании, хлор поддерживает горение многих органических веществ. Хлор — вещество преимущественно удушающего действия, раздражает дыхательные пути, Сможет вызвать отек легких. При действии хлора в крови нарушается содержание свободных аминокислот. При незначительных концентрациях хлора наблюдается покраснение конъюнктивы, мягкого неба и глотки, бронхит, легкая одышка, охриплость, чувство давления в груди. При воздействии малых и средних концентраций хлора наблюдаются загрудинные боли, жжение и резь в глазах, слезотечение, мучительный сухой кашель, увеличивается одышка, пульс учащается, начинается отделение мокроты со слизью и отхаркивание пенистой желтой или красноватой жидкости. Иногда отравление, перенесенное на ногах, через несколько дней заканчивается смертью.
ПДКмр — 0,1 мг/м3, ПДКсс = 0,03 мг/м3
Для обеспечения охраны воздушной среды установлена еще одна нормативная величина, характеризующая объем вредных веществ, выбрасываемых в атмосферу отдельными источниками загрязнения, — предельно допустимый выброс (ПДВ). ПДВ— это объем (количество) загрязняющего вещества, выбрасываемого отдельным источником за единицу времени, превышение которого ведет к превышению ПДК в среде, окружающей источник загрязнения, и, как следствие, к неблагоприятным последствиям в окружающей среде и к риску для здоровья людей.
Воздух характеризуется ионным составом. Ионизация воздуха — процесс превращения нейтральных атомов и молекул воздушной среды в электрически заряженные частицы (ионы). Ионы в воздухе могут образовываться вследствие естественной, технологической и искусственной ионизации.
Естественная ионизация происходит в результате воздействия на воздушную среду космических излучений и частиц, выбрасываемых радиоактивными веществами при их распаде. Естественное ионообразование происходит повсеместно и постоянно во времени.
Технологическая ионизация происходит при воздействии на воздушную среду радиоактивного, рентгеновского и ультрафиолетового излучения, термоэмиссии, фотоэффекта и других ионизирующих факторов, обусловленных технологическими процессами. Образовавшиеся при этом ионы распространяются в основном в непосредственной близости от технологической установки.
Искусственная ионизация осуществляется специальными устройствами — ионизаторами. Ионизаторы обеспечивают в ограниченном объеме воздушной среды заданную концентрацию ионов определенной полярности.
Характеристиками ионов являются подвижность и заряд. Подвижность ионов выражается коэффициентом пропорциональности «К» (см/сек) (см/В) между скоростью ионов и напряженностью электрического поля, воздействующего на ион. Подвижность ионов зависит от их массы: чем больше масса, тем меньше скорость перемещения иона в электрическом поле. По подвижности весь спектр ионов условно делят на пять диапазонов:
- легкие К > 1,0,
- средние 1,0 > К > 0,01,
- тяжелые 0,01 > К > 0,001,
- ионы Ланжевена 0,001 > К > 0,0002,
- сверхтяжелые ионы 0,0002 > К.
Каждый ион имеет положительный или отрицательный электрический заряд (полярность).
Наряду с возникновением происходит непрерывное исчезновение ионов. Факторами, определяющими исчезновение легких ионов, являются: рекомбинация двух легких ионов разных полярностей; адсорбция легких shob на незаряженных ядрах конденсации; рекомбинация легкого и тяжелого ионов зарядами противоположных знаков и др.
В зависимости от соотношения процессов ионизации деионизации устанавливается определенная степень онизированности воздуха. Степень ионизированности воздушной среды определяется количеством ионов каждой полярности в одном кубическом сантиметре воздуха. Определение количества ионов и их полярности осуществляется счетчиками ионов. По результатам измерения высчитывается показатель полярности. Показателем полярности П является отношение разности числа ионов положительной n+ и отрицательной n - полярности к их сумме, т. е.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |




