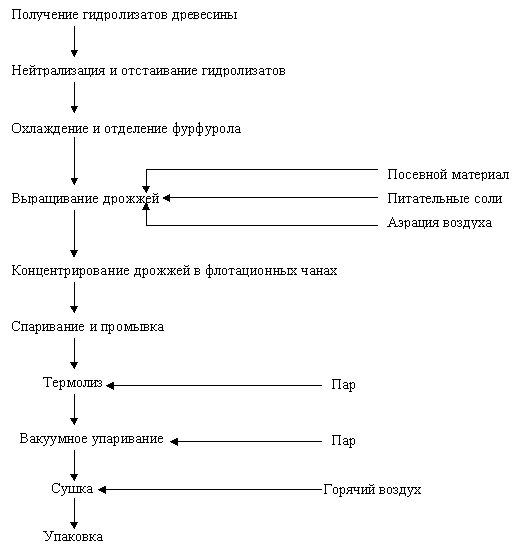
Схема получения кормовых дрожжей из гидролизатов древесины приведена ниже:
 |
Лекция № 14
Технология получения аминокислот
Методы получения аминокислот, лизин, триптофан
Методы получения аминокислот
Восемь аминокислот организм животных не может синтезировать, поэтому их называют биологически незаменимыми аминокислотами. К ним относятся фенилаланин, изолейцин, лейцин, лизин, метионин, треонин, триптофан и валин. Эти аминокислоты должны регулярно и в нужном количестве поступать в организм вместе с пищевыми продуктами. Недостаток одной из этих аминокислот в пище может стать фактором, лимитирующим рост и развитие организма.
В растительных продуктах, составляющих основу питания человека и животных, в недостаточном количестве может быть лизин, метионин и иногда триптофан. Препараты этих аминокислот имеют большое значение в формировании правильного питания человека и в сбалансированности кормов для домашних животных. В пищевой промышленности и кулинарии многих стран в качестве специи используется натриевая соль глутаминовой кислоты, придающая ощущение сытости. Препараты аминокислот используют в медицине, например для парентерального питания больных и для исследовательских работ в качестве реагентов.
Аминокислоты можно получить химическим синтезом, но в этом случае образуется трудно разделимая рацемическая смесь L - и. D-форм аминокислот. Биологически активными и потому используемыми в питании человека и животных являются L-аминокислоты, исключение составляет только метионин. В Советском Союзе освоен метод промышленного получения D-, L-метионина химическим синтезом.
Аминокислоты можно получить и гидролизом природных белков с последующим выделением аминокислот из гидролизата. Однако запасы белков ограничены, кроме того, при кислотном гидролизе некоторые аминокислоты, например триптофан, разрушаются. В будущем, возможно, будут получать аминокислоты из белков микробного происхождения, химически или ферментативно гидролизуя их.
Аминокислоты можно получить и из соответствующих кетокислот, химически или микробиологически аминируя их. Однако проблема получения L-аминокислот путем аминирования до сих пор практически не решена.
Лизин
Лизин в организме является не только структурным элементом белка, но и выполняет ряд важных биохимических функций — является предшественником карнитина и оксилизина. Лизин способствует транспорту кальция и стронция в клетки и др. В настоящее время во многих странах препарат лизина добавляют к хлебу для повышения его биологической ценности, а также для улучшения внешнего вида. Доказано, что лизин улучшает аппетит, способствует секреции пищеварительных ферментов, предотвращает кариес зубов у детей.
Лизин является самой дефицитной в кормах животных незаменимой аминокислотой. Установлено, что добавка лизина в количестве 0,1—0,4% к кормам значительно увеличивает продуктивность домашних животных.
Для биосинтеза лизина используют гомосериндефицитные мутанты ауксотрофных бактерий родов Brevibacterium, Micro-coccus, Corynebacterium и др.
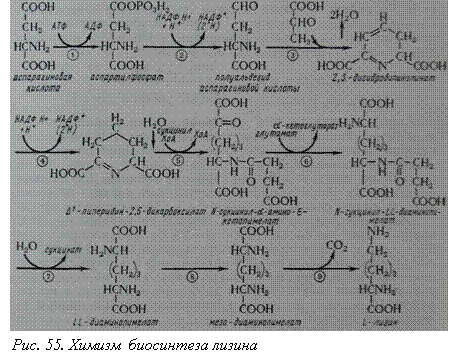
Химизм образования молекулы лизина показан на рис. 55.
 В Институте микробиологии им. А. Кирхенштейна разработаны основы непрерывной ферментации лизина в мелассно-кукурузной среде при помощи культуры Brevibacte-rium 22 и 22 L. При гомогенной ферментации по методу хемостата выявлено, что равновесное состояние системы устанавливается при скорости протока 0,05≤D≤0,20 ч-1, при этом концентрация лизина составляет 6—8 г/л, содержание биомассы около 8 г/л. Проточная культура обладает повышенной лизинсинтезирующей способностью (на 20—25% выше по сравнению с периодической), поэтому рациональной является комбинированная технология получения лизина: непрерывная ферментация на стадии приготовления посевного материала и периодический процесс главной ферментации.
В Институте микробиологии им. А. Кирхенштейна разработаны основы непрерывной ферментации лизина в мелассно-кукурузной среде при помощи культуры Brevibacte-rium 22 и 22 L. При гомогенной ферментации по методу хемостата выявлено, что равновесное состояние системы устанавливается при скорости протока 0,05≤D≤0,20 ч-1, при этом концентрация лизина составляет 6—8 г/л, содержание биомассы около 8 г/л. Проточная культура обладает повышенной лизинсинтезирующей способностью (на 20—25% выше по сравнению с периодической), поэтому рациональной является комбинированная технология получения лизина: непрерывная ферментация на стадии приготовления посевного материала и периодический процесс главной ферментации.
При наличии хорошо герметизированной и автоматически управляемой ферментационной аппаратуры можно осуществить трехступенчатый процесс, который обеспечивает 20— 30 г/л лизина при выходе культуральной жидкости из третьего аппарата (табл. 16).
Высокую концентрацию лизина (до 60 г/л) в культуральной жидкости можно получить на мелассной среде, если во время ферментации вести подкормку путем дробной подачи части питательной среды при соблюдении точной регуляции культивирования. Мелассу можно заменить, на сахарозу, диффузионный сок сахарной свеклы, глюкозу или гидролизаты крахмала, древесины, торфа, а также на уксусную кислоту.
Для получения кристаллического лизина клеточную массу центрифугируют, а культуральную жидкость пропускают через катионнт КУ-2 или КВ-4-Р-2. Лизин элюируют 2,0—3,5%-ным раствором NH4OH, элюат упаривают в вакууме при температуре 600С до 1/20 — 1/30 части исходного объема. Затем при помощи НС1 устанавливают рН 4,5—5,0, охлаждают до 14—18°С и кристаллизуют.
Фильтрацией или центрифугированием кристаллов получают технический лизин, содержащий 94—96% лизина монохлоргидрата. Для получения чистого лизина кристаллы технического лизина в небольшом количестве воды нагревают до 70°С, добавляют активированный уголь, перемешивают и фильтруют. При помощи НС1 устанавливают рН 4,9, раствор упаривают и кристаллизуют. Кристаллы сушат при температуре 60°С. Полученный таким образом лизин содержит 99,9% лизина монохлоргидрата. 0,1% золы и не более 0,001% тяжелых металлов.
После отделения лизина из фильтрата еще выделяют бетаин, используемый в медицине (препарат асидин), а также в животноводстве.
Лизин можно получать, работая по двухступенчатому методу. На первой ступени при помощи микробиологического синтеза (аналогичного биосинтезу лизина) или химического синтеза (из голуола. керосина и др.) получают α, ε-диаминопимелиновую кислоту. На второй ступени проводят ферментативное декарбоксилирование α, ε -диаминопимелиновой кислоты.
Триптофан
Триптофан используют в медицине, а также как реагент в биохимических исследованиях; в небольших количествах он требуется для нужд животноводства. Триптофан получают из антраниловой кислоты, используя особые штаммы дрожжей Candida или Hansunella.
Антраниловая кислота ядовита. Синтезируя триптофан, упомянутые дрожжи освобождают клетки от этого вредного соединения, превращая его в важную для биосинтеза белков аминокислоту.
Для размножения дрожжей можно использовать мелассу, диффузионный сок сахарной свеклы, сахарозу или другие среды, содержащие усваиваемые источники углерода.
Активный штамм дрожжей — продуцент триптофана — сохраняют на скошенном суслоагаре и пересевают один раз в месяц. После пересева выдерживают 48 ч в термостате при 28— 300С, затем сохраняют в холодильнике. Далее проводят подготовку посевного материала для двухступенчатой ферментации.
Состав питательной среды для колб следующий (в г/л): меласса 104; мочевина 5; К2НРО4 0,1; MgSO4 0,05; СаСl2 0,1; рН 7,5—8. Колбы выдерживают на качалке 24 ч при 28—30°С. После 24 ч выращивания содержимое колб первой стадии в стерильных условиях переносят в качалочные колбы емкостью 750 мл, содержащие по 100 мл питательной среды указанного выше состава.
После 24 ч выращивания на качалке биомасса дрожжей второй стадии используется для дальнейшего накопления дрожжевой массы в ферментаторе.
Процесс ферментации в ферментаторах проводят так. Производственную питательную среду, содержащую (в г/л) мелассы 62.3; мочевины 5; K2HPО4 0,1; СаСl2 0.1; MgSO4 0,05. стерилизуют 30 мин при 0,1 МПа (1 кгс. смс), рН среды 7.5—8. После охлаждения до 300С туда в стерильных условиях переносят посевной материал, который содержит не менее 3—5 г, л сухой биомассы. В ферментаторе в течение 24 ч дрожжи культивируют при аэрации не менее 7 г О2/(л-ч).
В качестве пеногасителя можно использовать подсолнечное масло, кашалотовыи жир или кремнийорганическое соединение.
Через 24 ч в культуральную жидкость добавляют антраниловую кислоту в виде 5%-ного спиртового раствора и мочевину з виде 50%-ного раствора. После внесения антраниловой кислоты начинается вторая стадия ферментации — биосинтез L-трипто-фана. Уровень аэрации снижается до 3—4 г О;/(л-ч). После добавления в среду антраннловой кислоты и мочевины через 4 ч добавляют мелассу в виде 25%-ного раствора. На дальнейшем этапе ферментации добавки проводят в следующем порядке: мелассный раствор добавляют через каждые 12 ч. антраниловую кислоту одновременно с источником азота вносят через каждые 6 ч.
Через 144 ч ферментацию прекращают.
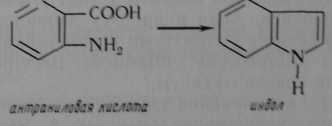 |
Механизм трансформации антраниловой кислоты в триптофан может быть представлен следующим образом. Вначале из антраниловой кислоты ферментативно образуется индол
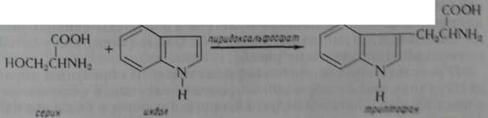 |
По мнению и , триптофан образуется при конденсации серина и индола в присутствии пиридоксальфосфата:
После осаждения биомассы триптофан из культуральной жидкости выделяют при помощи ионообменных смол и затем элюируют раствором аммиака в изопропиловом спирте.
В Институте микробиологии им. А. Кирхенштейна АН ЛатвССР разработан метод получения кормового концентрата триптофана. В его состав входит также дрожжевая биомасса.
Лекция 15
Генетика. Трансформация. Посттрансляционная модификация белков. Регуляция белкового синтеза.
Значительная часть синтезируемых клеткой белков в зависимости от их функционального назначения либо переносится через мембраны, либо встраивается в них. Проникновение белков через биологические мембраны, равно как и их встраивание в мембраны, осуществляется с помощью сигнальных пептидов. Такое предположение впервые было высказано в начале 70-х годов Г. Блобелем. В настоящее время эта гипотеза подтверждена экспериментально.
Сигнальные пептиды представлены фрагментами полипептидных цепей белков в их N-концевой части протяженностью 15-30 аминокислотных остатков. Центральная часть сигнальных пептидов содержит остатки гидрофобных аминокислот, а концевые последовательности обогащены гидрофильными аминокислотными радикалами. Такая структура обеспечивает, при наличии не менее 7 гидрофобных радикалов подряд, беспрепятственное внедрение сигнальных пептидов в липопротеиновую мембрану в зоне рецептора сигнального пептида и последующий перенос белка через нее или закрепление в ней. Установлено, что перенос белков через биологические мембраны может осуществляться либо либо одновременно с трансляцией белка в рибосоме (котрансляционно), ибо по завершении трансляции и отделения белка от рибосомы (пострансляционно), но в любом случае ведущая роль принадлежит сигнальному пептиду (рис.101). Последний отщепляется по завершении переноса при участии сигналопептидазы.
Сигнальная гипотеза Блобеля позволила по-иному подойти к проблеме активного транспорта макромолекул. Однако последняя не сводится только к сигнальной гипотезе: получены данные о существовании специальных белков – поринов, обеспечивающих перенос макромолекул. Расширились представления о мембранных белках, распознающих сигнальные пептиды, а некоторые из них (М=34 и 54 кДа) выделены и охарактеризованы; изучена группа белков (М=кДа), заякоривающих новообразованные белки в мембране; обнаружены рибонуклеопротеиновые частицы, составленнные из 7,8 РНК и нескольких (до 6) пептидов, тоже узнающие сигнальные последовательности в белках.
Посттрансляционная модификация белков
Не все белки, образовавшиеся в результате рибосомального синтеза, обладают полностью завершенной структурой. Во многих случаях они синтезируются в виде предшественников и лишь после протеолитического отщепления пептидного фрагмента приобретают законченную форму. Примерами такого рода посттрансляционной модификации белков может служить отщепление сигнальных пептидов по завершении переноса белков через билогические мембраны (рис.101), фрагментирование белковых предшественников при образовании из них функционально активных белков, например трипсина из трипсиногена, инсулина из проинсулина, или биологически активных пептидов, например гормонов и рилизинг-факторов. Аналогичный характер носит посттрансляционная модификация белков, сводящаяся к протеолитическому отщеплению N - концевого формилметионина или метионина, с которых, как показано выше, начинается сборка полипептидных цепей в процессе рибосомального синтеза белков.
Вместе с тем широко представлена посттрансляционная модификация белков по аминокислотным радикалам. К их числу относятся: гидроксилирование радикала пролина при переходе проколлагена в коллаген; ацетилирование N - концевой аминокислоты в белковой молекуле, как, например, при биосинтезе яичного альбумина; метилирование радикалов лизина и аргинина при посредстве S-аденозил-L-метионин: протеин N-метил- или О-метилтрансферазы, особенно широко представленное при посттрансляционной модификации гистонов, негистоновых ядерных белков и рибосомальных белков; присоединение олигосахаридных фрагментов к радикалам аспарагина, серина и треонина при биосинтезе гликопротеинов; амидирование радикалов аспарагиновой и глутаминовой кислоты, что связывают с изменчивостью белков в онтогинезе и, в частности, при старении; карбоксилирование радикалов глутаминовой кислоты по γ-углеродному атому, в результате чего в белке возникают остатки γ-карбоксилглутаминовой кислоты, необходимые для связывания Са2+; аденилирование и уридилирование радикалов тирозина. К посттрансляционным процессам, имеющим важнейшее значение для регуляции метаболической активности генома, относятся фосфолирование гистонов и негистоновых белков хроматина. Один из примеров котрансляционной модификации белков приведен на рис.102.
Регуляция белкового синтеза
Исходя из матричной гипотезы биосинтеза белка, Ф. Жакоб и Ж. Моно (1961) впервые предложили весьма многообещающую схему регуляции белкового синтеза. Следуя концепции один ген – одна мРНК – один белок, Ф. Жакоб и Ж. Моно связали узловой пункт регуляции белкового синтеза с ДНК, входящий в состав генетического аппарата клетки. В генетическом аппарате клетки существуют сообщества структурных генов, так называемых оперонов, каждый из которых ответственен за взаимосвязанный синтез ряда специфических белков. Деятельность оперона в качестве поставщика мРНК контролируется геном-оператором, который либо разрешает, либо запрещает запуск гомологической репликации серии мРНК на ДНК-матрице. В свою очередь, функция гена-оператора контролируется пространственно изолированным от него геном-регулятором, который продуцирует мРНК, необходимую для синтеза белка-репрессора. Именно белок-репрессор, будучи присоединен к гену-оператору, блокирует его функцию. Более того, сам белок-репрессор подвержен действию аллостерических эффекторов, которые, соединяясь с ним, так изменяют его третичную структуру, что либо стимулируют, либо ингибируют возникновение комплекса между репрессором и геном-оператором. В качестве аллостерических эффектов часто выступают субстраты (индуцированный синтез ферментов). Сказанное иллюстрирует схема 4. В нее включены также информосомы, на уровне которых тоже осуществляется регуляция биосинтеза белков.
Данная схема отражает только часть тех факторов, котрые принимают участие в регуляции биосинтеза белков. Эта регуляция осуществляется также на уровне метаболитов при активировании и переносе аминокислот; на уровне макромолекул при биосинтезе ДНК, различных видов РНК и рибосом; на уровне субклеточных структур (формирование полисом, роль белково-липидных мембран и т. п.), клетки (ядерноцитоплазменные взаимоотношения и др.), органа и организма (гормональная регуляция) и, наконец, на уровне среды (например, зависимость точности кода белкового синтеза от температуры).
Лекция №16
Получение витаминов, антибиотиков и ферментативных препаратов
Витамины группы В, рибофлавин, классификации антибиотиков, технические препараты ферментов
Получение витаминов
Микроорганизмы содержат много витаминов, которые чаще всего входят в состав ферментов. Состав и количество витаминов в биомассе зависят от биологических свойств данной культуры микроорганизмов и условий культивирования. Некоторые витамины микроорганизмы синтезируют, другие напротив усваивают в готовом виде из окружающей среды. Культура, способная синтезировать какой-либо витамин, называется аутотрофной по отношению к нему, если культура не способна синтезировать данный витамин, она является аутогетеротрофной.
Витамины группы В. Сравнительно богаты витаминами группы В дрожжи (хлебопекарные, пивные, кормовые).
Изменяя условия среды, содержание отдельных витаминов можно увеличить.
Количество витаминов в клетках, а также их выделение из последних можно изменить при помощи микроэлементов. Например, небольшие добавки марганца способствуют накоплению инозита в клетках. Так, повышенные дозы кобальта (100— 500 мкг хлорида кобальта на 100 г) увеличивают содержание пиридоксина (витамин В6) в культуральной жидкости.
Рибофлавин. Для получения препарата витамина В2 используют культуру дрожжей Candida guilliermondia, бактерии Clostridium acetobutylicum, даже продуцент лизина Brevibacterium и др. Однако наибольшую продуктивность в биосинтезе рибофлавина имеет дрожжеподобная культура Eremothecium ash-buii, дающая до 6000 мкг рибофлавина на 1 г сухого вещества питательной среды.
Рибофлавин накапливается в клетках микроорганизмов либо в виде флавинадениннуклеотида, либо в свободном виде. В последнем случае он представляет собой желтые кристаллы, находящиеся в вакуолях. Максимального количества биомассы культура Eremothecium ashbuii достигает на второй день культивирования. В это время наблюдается интенсивное спорообразование и синтез рибофлавина.
При старении культуры, особенно через 4—5 сут культивирования, клетки начинают автолизироваться и рибофлавин переходит в среду.
Биосинтез рибофлавина полностью еще не выяснен. Считают, что кольца В и С в молекуле рибофлавина образуются так же, как и пуриновые основания, и накопление рибофлавина в клетках и окружающей среде происходит в результате чрезмерно активного синтеза пуринов. Предшественником рибофлавина, думается, мог бы быть диаминоурацил. Кроме того, из продукта гликолиза — пировиноградной кислоты — может образоваться ацетоин или диацетил, которые, возможно, участвуют в образовании кольца А молекулы рибофлавина.
Для получения кормового препарата рибофлавина культуральную жидкость упаривают в вакууме до 30—40% сухих веществ и сушат в распылительных или валково-вакуумных сушилках. Для получения кристаллического препарата рибофлавина культуральную жидкость нагревают до 95—100°С, так как в этих условиях весь рибофлавин выходит из клеток. Затем раствор центрифугируют, центрифугат охлаждают до 18—20°С, устанавливают рН среды 4,5—5,0 и осаждают рибофлавин из раствора при помощи гидросульфита. После декантации осадок промывают, центрифугируют, сушат и размельчают. Полученный технический препарат можно использовать в животноводстве. Медицинский препарат рибофлавина получают перекристаллизацией его из раствора технического рибофлавина в соляной кислоте.
Получение антибиотиков
Антибиотики — органические соединения. Они синтезируются живой клеткой и способны в небольших концентрациях замедлить развитие или полностью уничтожить чувствительные к ним виды микроорганизмов. Их продуцируют не только клетки микроорганизмов и растений, но и клетки животных. Антибиотики растительного происхождения называют фитонцидами. Это хлорелин, томатин, сативин, получаемый из чеснока, и алин, выделяемый из лука.
По химическому строению антибиотики также делят на группы (по и ):
1. Алифатические антибиотики — нистатин, микостатин, фун-гицидин. Нистатин продуцируют Streptomy-ces fungicidicus, Str. naursei. Он действует на дрожжи и грибы, но не влияет на бактерии.
2. Алициклические антибиотики — тетрациклин — действуют на стафилококки, стрептококки, салмонеллы и др. Его продуцент Str. viridofaciens.
Тетрациклин получают также путем дехлорирования хлор-тетрациклина. Если в В-кольце молекулы тетрациклина у верхнего атома углерода имеется —ОН группа, тогда это соединение (также широко известное антибиотическое вещество) называют окситетрациклином. Его продуцируют Str. rimosus и другие культуры.
Если у верхнего атома углерода D-кольца молекулы тетрациклина находится атом хлора, то это вещество называется хлортетрациклином или биомицином. Оно используется не только в медицине, но и как стимулятор при откармливании домашних животных.
3. Антибиотики — хиноны (например, фумигатин, продуцируемый многими видами Aspergillus), воздействуют на стафилококки, стрептококки, Vibrio choleras и др.
Азотосодержащие гетероциклические антибиотики — пенициллин и его производные продуцируются Penicillium potatum и особенно P. chrysogoiium. Он воздействует на грамположи-тельные бактерии — Salmonella, Pseudomonas, Staphylococcus, Candida albicans, Mycobaelerium tuberculosis, Streptococcus faeca-lis. Vibrio и др.
5. Стрептомицины и им подобные антибиотики. Стрептомицин продуцируют Streptomyces griseus или Actinomyces strepto-mycini (пo классификации советских ученых). Он воздействует на грамотрицательные бактерии, а также на некоторые грам-положительные бактерии.
6. Содержащие кислород гетероциклические антибиотики — гризеофульвнн (продуцирует Penicillium griseofulvum) и др.
7. Антибиотики — полипептиды — грамицидин, полимиксин и др. По строению они являются циклопептидами из остатков L и D-минокислот. Полимиксин продуцируют Bacillus polymyxa, В. aerosporus и др.
В настоящее время производят очень много различных антибиотиков. В качестве примера ниже приводится технология получения пенициллина и кормового биомицина.
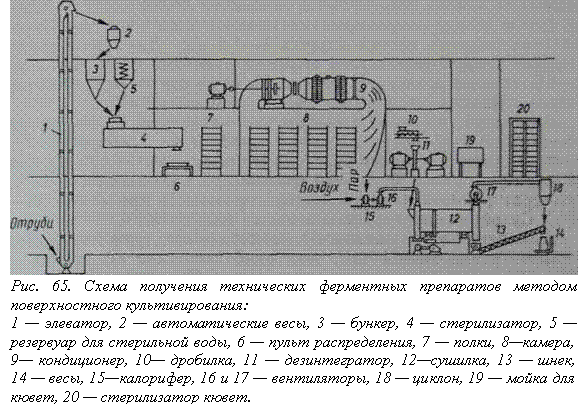
Получение ферментативных препаратов
Для получения ферментных препаратов используют как микроскопические грибы, так и бактерии и дрожжи. Иногда получение технического ферментного препарата кончается проведением процесса ферментации, например в спиртовой промышленности для осахаривания крахмала используют жидкую культуру As-pergillus niger, выращенную глубинным методом культивирования на спиртовой барде с добавками крахмала (1%) и различных солей. Впоследствии ее добавляют в жидком виде в количестве 10—12% к осахариваемому затору. Однако активность ферментов в культуральной жидкости быстро снижается. Поэтому широко практикуют получение сухих технических ферментных препаратов.
Технические препараты ферментов. Комплексный амилолитический ферментный препарат получают см выращивания плесневых грибов на твердой питательной среде с последующей сушкой и измельчением полученной массы. Более активный препарат фермента получают путем экстракции такого «грибного солода» с последующим выпариванием и сушкой. Еще более активные ферментные препараты можно выделить из культуральной жидкости путем осаждения амилазы ацетоном и дальнейшим высушиванием коагулята при температуре 27—28СС. Для осаждения фермента часто используют и сульфат аммония. Предварительно культуральную жидкость выпаривают при температуре 400C до 40%-ного содержания сухих веществ. Коагулят сушат вместе с наполнителем. В Японии для пищевых нужд используют технический препарат амилазы, полученный адсорбцией фермента из культуральнон жидкости особо обработанным крахмалом. Затем амилазу вместе с крахмалом лиофилизируют.
Препарат, содержащий пектиназу, получают из отходов производства лимонной кислоты — мицелия Aspergillus niger, высушивая его или коагулируя из экстракта белковую фракцию мицелия. Этот препарат используют для осветления соков и увеличения их выхода при обработке ягод и фруктов.
 |
Лекция №17
Биохимическая очистка
1. Биохимическое превращение загрязнений неприродного типа.
Проблема расширения биохимического производства тесно связана с проблемой полной очистки сточных вод и снижения отрицательного воздействия их на окружающую природу.
В практике обезвреживания сточных вод химических и электрохимических производств широко применяют метод биологической очистки, основанный на способности гетеротрофных микроорганизмов использовать в качестве источников питания разнообразные неорганические и органические соединения, подвергая их биохимическим превращениям.
Известно, что ни одно из органических соединений, образующихся в результате жизнедеятельности различных организмов, не накапливается на Земле. Важнейшую роль в превращении этих органических соединений играют микроорганизмы. Многообразие функций микроорганизмов привело к формированию «доктрин катаболической безотказности микроорганизмов», т. к. любое органическое соединение, имеющееся в природе, используется какими-либо микроорганизмами.
Широкое распространение получил биологический метод с использованием процесса метаболизма бактерий активного ила, т. е. использование ферментов, которые необходимы для метаболизма в данных условиях, в присутствии специфического органического соединения или комплекса органических соединений. Поэтому учитывается не только способность микроорганизмов к синтезу ферментов, но и возможность изменения их активности. Использование свойств адаптации бактерий активного ила позволяет успешно решить вопросы биологической очистки сточных вод химических производств, содержащих сложные органические соединения неприродного происхождения. Именно этим обусловлено широкое внедрение методов биологической очистки в различные отрасли химической промышленности (очистка сточных вод при производстве: капролактама, метанола, карбамида, аммиака, формамина, белково-витаминного концентрата, полимерных материалов и т. д.).
Биохимическое превращение загрязняющих веществ микроорганизмами активного ила обусловлено процессами обмена веществ бактерий, их типом дыхания и питания.
Биоценоз активного ила формируется преимущественно гетеротрофными микроорганизмами, особенностью которых является способность усваивать углерод из готовых органических соединений самой различной химической структуры.
Вещества, имеющую различную химическую структуру, проходят в бактериальную клетку с различной степенью легкости.
Известно, что углеводорода легко проникают в бактериальную клетку. Соединения, содержащие амино - и оксигруппы, труднее проникают в клетку, а следовательно, их питательная ценность значительно снижается. Чем больше молекула вещества содержит полярных групп, тем труднее она проникает в клетку. Например, этиловый спирт CH3CH2OH, имеющий одну оксигруппу, проникает в клетку значительно легче, чем этиленгликоль (CH2OH CH2OH), имеющий две оксигруппы. Глицерин, имеющий три оксигруппы (CH2OH CHOH CH2OH), поступающий в клетку медленно.
Состав и свойства активного ила.
Активный ил представляет собой экосистему, включающую сложный комплекс микроорганизмов различных классов, простейших микроскопических червей, водорослей; количественное и качественное формирование экосистемы диктуется искусственными условиями существования. Микрофлора активных илов, очищающих многокомпонентные сточные воды химических производств, различна и зависит от состава очищаемых сточных вод, технологического режима работы аэротенков и условий эксплуатации всего комплекса очистных сооружений.
Количественные закономерности формирования экосистемы активного ила определяются технологическим режимом работы аэротенков. Общее количество микроорганизмов в сооружениях прямо пропорционально окислительной мощности. Качественный и количественный состав микрофлоры активного ила, очищающего сточные воды химического производства, а также биохимические свойства бактерий, определяющие величину удельной скорости окисления активного ила, зависят от условий его обитания. Они являются управляемыми параметрами и формируются в зависимости от управляющих параметров: химического состава очищаемых сточных вод, постоянства концентраций основных специфических загрязняющих веществ и оптимальных параметров технологического режима.
К физическим свойствам активного ила, характеризующим его качество, относится способность ила к оседанию. Она выражается показателем (иловый индекс), который представляет собой отношение объема активного ила в миллилитрах после 30-ти минутного отстаивания к 1 г. сухого вещества активного ила при разбавлении иловой смеси до 1 г/л. Хорошим является индекс не более 100. Резкие колебания илового индекса, особенно его увеличение до 150–200, свидетельствуют о неблагоприятных, нестабильных условиях работы аэротенки.
Качество активного ила характеризуют также его морфологические свойства. Благоприятные, стабильные условия существования активного ила обуславливают хорошую его осаждаемость, прозрачную надиловую жидкость, пластичную структуру илового осадка.
Показателем качества всей экосистемы активного ила является инерционность экосистемы. Она проявляется в способности нивелировать одиночные возмущающие отрицательные воздействия.
Адаптированный активный ил с оптимальными биохимическими, физическими и морфологическими показателями, эксплуатированный в условиях стабильного оптимального технологического режима, обладает значительной инерционной емкостью и способен «гасить» краткосрочные резкие нарушения технологического режима очистки (рис. 15, 16).
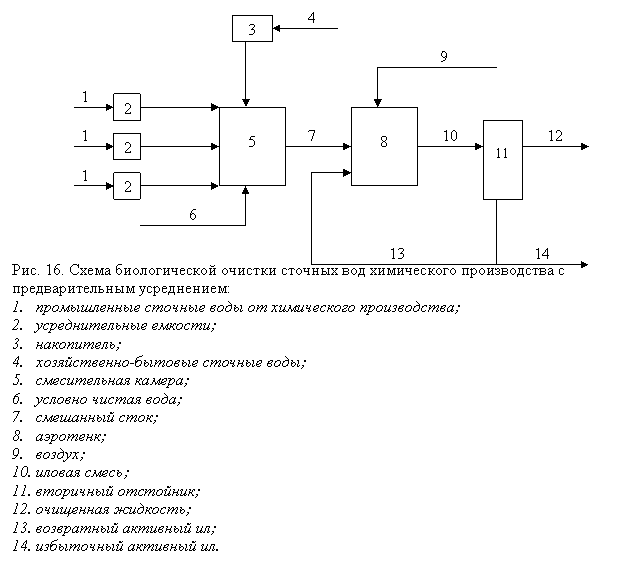
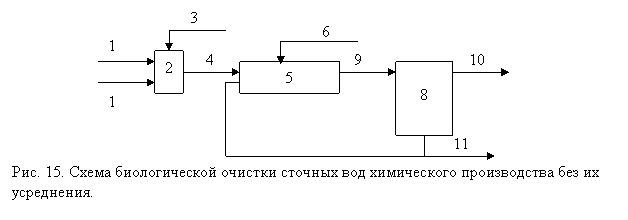
Технология очистки сточных вод активным илом.
Сточные воды химических производств содержат сложный комплекс различных соединений органического и неорганического происхождения, различающихся составом, свойствами и фазово-дисперсным состоянием.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |





