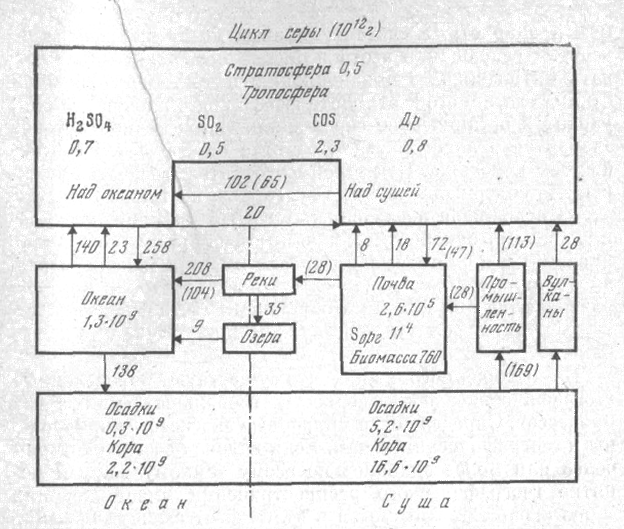
Рис.14. Основные резервуары (1012 г) и глобальные потоки соединений серы (Заварзин, 1984, 1012 г./год)
Возбудители процесса сульфатредукции относятся к разным родам анаэробных бактерий: Desulfovibrio — подвижные изогнутые палочки, не образующие спор, Desulfotomaculum — споровые палочки. Среди представителей первого рода есть галофилы, среди вторых — термофилы. Найдены сульфатредукторы и среди кокков (Desulfococcus, Desulfosarcina). Распространены сульфатредуцирующие бактерии в почвах с режимом, приводящим к длительному анаэробиозу, например в почвах затопляемых рисовых полей, а также в болотах, илах, лиманных грязях, в пластовых водах сопровождающих нефтяные месторождения. В подзолах мало сульфатов, и биогенным путем сульфиды в них не накапливаются. В щелочных и нейтральных почвах образуются нерастворимые сульфиды.
Накопление сульфида железа приводит к образованию черного ила. С жизнедеятельностью сульфатвосстанавливающих бактерий связывают процесс биогенного содонакопления. Провинции, где формируются содовые солончаки, приурочены к низменным местам, например, к поймам рек, понижениям вокруг болот. Если коренные породы в этих местах обогащены сульфатами, то в анаэробных условиях при затоплении и разложении органического вещества образуется H2S, который затем путем химических реакций преобразуется в Na2S и далее в соду:
Na2S + Н2О + СО2 > Nа2СОз.
Сульфатредуцирующие бактерии способны к образованию карбонатных минералов. В определенных условиях их клетки бывают инкрустированы кристаллами кальцита.
Окисление сероводорода и других недоокисленных соединений серы происходит с участием разных специфических групп серных бактерий. В аэробных условиях окисление производят бесцветные серобактерии и тионовые, в анаэробных — фотосинтезирующие пурпурные и зеленые бактерии.
Бесцветные серобактерии сходны по строению с нитчатыми цианобактериями. Основное их отличие от последних — отсутствие пигмента. Нити серобактерий либо свободно плавают в воде (Beggiatoa), либо прикрепляются одним концом к неподвижным предметам, к растениям или водорослям (Thiothrix). Они обитают в кислородной зоне водоемов и производят окисление поступающего из анаэробной зоны H2S до S2, которую откладывают внутри клеток. Так как для их обильного развития требуется градиент О2 и H2S, то они образуют в толще воды пленку на границе аэробной и анаэробной зон. В Черном море, например, такая пленка, была обнаружена на глубине 200 м. Энергии окисления H2S до S2 оказывается достаточно для биологического связывания СО2. Поэтому серобактерии — хемолитоавтотрофы, использующие химическую энергию окисления неорганической серы в виде H2S для синтеза органических веществ из СО2. Впервые это явление исследовал в 1888 г. С этой работой связано открытие хемосинтеза у микроорганизмов.
Фотосинтезирующие серные бактерии, как и бесцветные нитчатые серобактерии, в основном обитатели водоемов, но в отличие от последних они анаэробы. Наличие в клетках пигментов бактериопурпурина или бактериохлорофилла обусловливает соответственно красную или зеленую окраску этих бактерий. Пурпурные бактерии (Chromatium) откладывают серу внутри клеток, а зеленые {Chlorobium} — вне клеток. В почвенных условиях они имеют небольшое значение, но могут быть активны на затопляемых участках почв рисовых полей. Фотосинтезирующие бактерии замыкают анаэробный цикл серы за счет окисления поступающего из анаэробной зоны H2S, образуемого сульфатредуцирующими бактериями.
Одноклеточные тионовые бактерии широко распространены в почвах. Впервые в чистую культуру тионовые бактерии выделил в 1904 г. М. Бейеринк, который дал им название Thiobacillus. Это название до сих пор сохраняется за одной из групп тионовых бактерий, хотя известно, что они не образуют спор. К настоящему времени среди тионовых бактерий описаны новые роды — Thiospirillum, Sulfolobus и Thiomicrospira. Эти бактерии в аэробных условиях окисляют H2S, сульфиды, тиосульфат, тетратионат, молекулярную серу и роданистые соединения до серной кислоты. Энергия окисления используется на синтез органических веществ из СОз через цикл Кальвина, как у всех автотрофных организмов. Акцептором электрона и водорода у них может выступать свободный кислород (Thiobacillus thiooxidans) или в анаэробных условиях — кислород нитратов (Th. denitrificans). Бактерии Th. ferrooxidans окисляют восстановленные соединения не только серы, но и железа. Среди тионовых бактерий есть уникальные виды, способные развиваться в очень кислых почвах с рН 3 и даже ниже (Th. Thiooxidans) или в щелочных (Th. thioparus).
Тионовые бактерии благодаря образованию сильной серной кислоты участвуют в природном сернокислотном выветривании, увеличивают подвижность нерастворимых фосфатов. Под действием этих бактерий происходит подкисление почв при добавлении серы к почвам со щелочной реакцией.
Тионовые бактерии используются и в практической деятельности для выщелачивания металлов из руд. Бактериальное выщелачивание металлов за счет окисления содержащихся в руде сульфидов позволяет вести добычу металла из бедного минерального сырья. Бактериальные методы выщелачивания обеспечивают один из этапов гидрометаллургии при минимальных энергозатратах.
Помимо биологического цикла серы в атмосфере Земли происходят превращения серусодержащих газов без участия живых организмов. Сера в виде сернистого газа образуется в результате сжигания нефти, а частично появляется в форме H2S и SO2 при извержении вулканов. Эти соединения окисляются в атмосфере, и образующаяся серная кислота возвращается на поверхность Земли и в почву. Вокруг промышленных районов таким путем происходит сильное подкисление почв вплоть до полной гибели растительности вблизи некоторых химических предприятий. Это одна из проблем охраны почв от техногенных загрязнений.
ПРЕВРАЩЕНИЯ КАЛИЯ
Калий — один из важнейших элементов, необходимых для растений. Он участвует в обменных процессах при синтезе аминокислот и белков, в реакциях фотосинтеза. Калий в значительной степени регулирует использование растениями азота. Между тем он относится к элементам, содержание которых в доступной форме в почве ниже потребности в них растений, и поэтому необходимо внесение калия в составе минеральных удобрений NPK
Усваиваемый калий составляет всего 1—2% от его общего количества в почве. Основной запас калия находится в минералах и в составе органоминеральных комплексов. Первичные минералы, содержащие калий, это слюды (биотит и мусковит) и полевые шпаты (ортоклазы и микроклины). Калий входит и во вторичные минералы: каолин, монтмориллонит, вермикулит. Освобождение калия из минералов происходит в процессе биологического выветривания. Процессы разложения минералов при взаимодействии с почвенными микроорганизмами и их метаболитами постоянно идут во всех почвах. В основе этих взаимодействий лежат разные механизмы: растворение сильными минеральными кислотами, образующимися при нитрификации, при окислении серы тионовыми бактериями; воздействие органических кислот — продуктов брожений и неполных окислении углеводов грибами; взаимодействие с внеклеточными аминокислотами, которые выделяются в среду многими почвенными микроорганизмами. С минералами взаимодействуют и продукты разложения микроорганизмами растительных остатков — полифенолы, таннины, полиурониды, флавоноиды, а также продукты микробного биосинтеза, например полисахариды. Некоторые из этих веществ действуют в растворе (кислоты), другие in situ на поверхности минералов (кислые гетерополисахариды). В опытах и с микроклином (8,7% К), биотитом (8,28% К) и бентонитом (1,89% К) в раствор вносили почвенные бактерии и через 100 дней обнаруживали освобождение из минералов более 50% калия. Рентгеноструктурный анализ подтвердил изменение крупных и мелких частиц алюмосиликатов под действием бактерий. Особенно активны в разрушении алюмосиликатов слизистые бактерии, выделяющие большое количество кислых полисахаридов. Среди них постоянно обнаруживается споровая палочка Bacillus circulans. Из неспоровых в превращении минералов участвуют представители рода Arthrobacter. В общем же это процессы неспецифические в которых участвуют разнообразные почвенные микроорганизмы.
ПРЕВРАЩЕНИЯ ЖЕЛЕЗА
Железо относится к элементам с переменной валентностью, и это обусловливает его разную подвижность в восстановительных и окислительных условиях. В первом случае оно активно мигрирует, во втором — инертно. Таким образом, основную роль в миграции железа в почве играет окислительно-восстановительная обстановка. В виде железоорганических соединений железо мигрирует легко, в виде FeS04 — слабо, а трехвалентное железо подвержено коллоидной миграции. Железо в почве содержится в следующих формах: в составе минералов (биотит, амфибол, пироксен); окисное нерастворимое (лимонит, гетит); растворимое — FеСОз (вивианит); псевдорастворимое — железо-гумусовые комплексы. В дерново-подзолистых почвах иллювиальные горизонты содержат 4—7% железа, а в красноземе его запас составляет 8-17%.
Участие микроорганизмов в превращениях железа в почве может быть прямым и косвенным. Рассмотрим несколько примеров.
1. Окисление железа в кислой среде происходит с участием специфических железобактерий, например Thiobacillus ferrooxidans. Процесс окисления Fe2+- Fe3+ идет за счет кислорода воздуха и с образованием энергии, которая используется в форме АТФ для фиксации: СО2 по типу хемосинтеза. Истинные железобактерии — хемолитоавтотрофы.
2. Окисление железа в нейтральной среде (в почвах гумидной зоны) - процесс побочный для осуществляющих его микроорганизмов и идет без использования ими энергии этого окисления. Как показала , он проводится микробами-гетеротрофами, которые удаляют этим путем образующуюся в их метаболических процессах перекись водорода. Эта функция у них проявляется только в специфических экологических условиях. К этой группе микроорганизмов относятся представители самых разных групп прокариот. Из них в почве распространены микоплазмы и представители рода Arthrobacter, а в воде — нитчатые, скользящие и цианобактерии.
Микоплазмы (класс Mollicutes) —сапрофиты, но в олиготрофных условиях способны паразитировать на других прокариотах или эукариотных организмах, например на грибах. Они окисляют железо и марганец, откладывая окислы на поверхности. Это мелкие полиморфные клетки, прорастающие нитями. К ним относятся Metallogenium symbioticum и Gallionella ferruginea.
Артробактерии — типичные почвенные бактерии со сложным циклом развития. К ним относятся многие бактерии, образующие отложения железа, которые были по-разному описаны на основании морфологических наблюдений их развития на стеклах обрастания или педоскопах: Siderocapsa, Siderobacter, Sideronema, Naumaniella, Ferribacterium.
3. Разложение железогумусовых комплексов в почве производят гетеротрофные микроорганизмы, осаждающие железо в виде конкреций и прослоек. Наиболее типичный для этого процесса организм - почвенная бактерия Seliberia stellata, описанная . Морфологически — это стебельковая бактерия, у которой стебельки закручены спирально, а отдельные клетки собираются в розетки.
4. Мобилизация железа из почвенных минералов происходит; за счет тех же механизмов, которые приводят к освобождению калия, т. е. благодаря образованию микроорганизмами слизей, фенольных соединений, щелочей. При этом образуются комплексные соединения, в которых железо мигрирует и аккумулируется в определенных горизонтах почв.
5. Восстановление железа при сопряженном окислении органического вещества или водорода происходит в анаэробных условиях с участием гетеротрофных микроорганизмов-полифагов (Bacillus или Clostridium) или анаэробных водородных бактерий из Pseudomonas, у которых Fe3+ - выступает в качестве акцептора электрона и может быть заменен молекулярным кислородом в аэробных условиях, или кислородом нитратов — в анаэробных. Восстановленное железо образует нерастворимый минерал — вивианит.
Таким образом, в превращениях железа в почве участвуют в основном микроорганизмы с неспецифическими функциями. Истинные железобактерии — группа облигатно-ацидофильных автотрофных бактерий, участвующие также и в превращениях серы.
ПРЕВРАЩЕНИЯ МАРГАНЦА
Марганец относится к группе необходимых для жизни микроэлементов. Его потребности покрываются микродозами, а в условиях его избытка наблюдается токсический эффект. В почве марганец находится в рассеянном состоянии в разных формах, в том числе и в виде металлорганических комплексов. Как и железо, он имеет переменную валентность и по-разному подвижен в зависимости от этого. Мигрирует марганец в почве главным образом в двухвалентной форме, в этой же форме он и усваивается растениями и микроорганизмами. В трех - и четырехвалентном состоянии марганец входит в состав железомарганцевых конкреций.
Бактерий, аналогичных железоокисляющим хемолитоавтотрофам в природе не обнаружено, хотя известны микроорганизмы, способные к аккумуляции и отложению марганца.
Превращения марганца в почве включают процессы его мобилизации из устойчивых природных соединений — минералов почвообразующих пород, образование и разрушение металлорганических комплексных соединений, биогенное окисление и аккумуляцию микроорганизмами, восстановление. Наиболее изученный микроорганизм, участвующий в окислении и аккумуляции марганца, — Metallogenium. В окислительных процессах, разрушении минералов и в разложении органоминеральных комплексных соединений с марганцем участвуют почвенные грибы, гетеротрофные бактерии, простекобактерии рода Pedomicrobium. Восстановление окислов марганца осуществляют факультативно-анаэробные микроорганизмы, которые понижают окислительно-восстановительный потенциал среды. Специфических восстановителей марганца типа денитрификаторов нет.
ПРЕВРАЩЕНИЯ АЛЮМИНИЯ
Алюминий — один из наиболее распространенных элементов на нашей планете и по содержанию в земной коре стоит на третьем месте после кислорода и кремния. В почве он находится в составе первичных и вторичных минералов, гидроокиси и алюмоорганических соединений, которые взаимно связаны (рис. 15). Мобилизация алюминия из кристаллических решеток алюмосиликатных минералов происходит при участии почвенных микроорганизмов, метаболиты которых либо образуют комплексные соединения непосредственно с алюминием либо выносят другие элементы из минералов, а алюминий, освобождаясь, связывается в металлорганические комплексы продуктами разложения растений или гумусовыми кислотами почв. В основе такого преобразования лежат реакции хелатизации. В форме металлорганических соединений алюминий приобретает подвижность и мигрирует в широком диапазоне рН. Эти процессы наиболее выражены в почвах зон влажного климата и связаны с подзоло - и латеритообразованием. В подзолистых почвах алюминий мигрирует в виде комплексных соединений с гумусовыми кислотами и накапливается в значительных количествах в иллювиальном горизонте в форме алюмоорганических комплексов с фульвокислотами.
Алюмоорганические соединения не только образуются в самой почве, но и поступают в нее с растительными остатками в виде комплексов алюминия с органическими кислотами, аминокислотами, белками. Далее в зависимости от экологических условий алюмоорганические соединения в почве претерпевают различные превращения: 1) выносятся за пределы почвенного профиля; 2) минерализуются; 3) закрепляются в составе гумусовых веществ. Первые два процесса характерны для почв влажных субтропиков, третий — для почв подзолистой зоны.
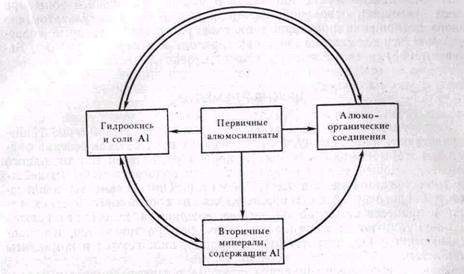
Рис. 15. Превращения алюминия (по , 1980)
Процессы минерализации алюмоорганических комплексных соединений связаны с жизнедеятельностью почвенных микроорганизмов. Экспериментальных работ в этой области пока очень мало. с сотрудниками показала, что в разложении этих веществ участвует комплекс грибов с организмами группы микоплазм — Metallogenium. В присутствии органоминеральных соединений алюминия или железа гифы грибов Penicillium sp. в симбиозе с Metallogenium покрываются отложениями гидроокисей соответствующего металла. Из этого можно заключить, что в определенной экологической обстановке микроорганизмы типа Metallogenium могут участвовать в накоплении железа и алюминия, а также марганца (см. выше) в почвенном профиле.
Накопление железа и алюминия в почвах тропической зоны при выносе кремния и оснований является, по-видимому, результатом активного поглощения полуторных окислов растениями, которые «перекачивают» эти элементы из нижних горизонтов в верхние.
ДРУГИЕ ЭЛЕМЕНТЫ
За счет включения разных механизмов почвенные микроорганизмы участвуют, по-видимому, в превращениях всех без исключения элементов, которые имеются в земной коре. Практически нет ни одного элемента, который тем или иным путем не подвергался бы воздействию микроорганизмов или их метаболитов. Одни элементы вовлекаются в биологический круговорот, входя в состав органических веществ, в процессе ассимиляции, другие окисляются, восстанавливаются или аккумулируются, третьи осаждаются или растворяются, извлекаются из минералов, подвергаются миграции, включаются в комплексы и т. д. и т. п.
Очень важны превращения, связанные с микроэлементами, которые необходимы микроорганизмам в очень малых дозах, но при этом роль их необычайно велика, так как они входят в состав ферментов и определяют их активность. Такова, например, роль молибдена, входящего в активный центр ферментов азотного цикла — нитрогеназы и нитратредуктазы; кобальта, ответственного за функции витамина B12; меди, которая включается в простетическую группу ферментов— оксидаз.
Известен ряд микроэлементов, которые не входят непосредственно в молекулы ферментов, но косвенно влияют на их активность и направление обмена веществ. К таковым относятся мышьяк, цинк, бор и др. Мышьяк, например, входит в состав всех живых клеток в микроколичествах. Его превращения в почве связаны с деятельностью микроорганизмов. Содержание мышьяка в почвах обычно невысокое — от 0,001 до 0,0001%. Оно наиболее высоко в черноземах и в органогенных горизонтах почв лесной зоны. Количество мышьяка увеличивается очень сильно за счет техногенных процессов. В его превращениях, аккумуляции и миграции участвуют грибы и бактерии. Окисление арсенита в арсенат — процесс биологический, о чем свидетельствует угнетение его азидом натрия, подавляющим дыхание. Среди бактерий, обусловливающих процесс окисления арсенитов, были описаны неспоровые грамотрицательные палочки из группы псевдомонад. Некоторые микроорганизмы ответственны за удаление мышьяка из почвы путем образования газообразных его соединений. Часть мышьяка фиксируется (иммобилизуется) клетками микроорганизмов за счет включения в обменные внутриклеточные реакции.
Бор в почвах в основном входит в состав органических соединений, из которых он освобождается микроорганизмами. Роль бора проявляется в образовании и функционировании клубеньков на бобовых растениях, так как он участвует в развитии сосудистой системы растений. Бор влияет на азотфиксацию клубеньковых бактерий, азотобактера и цианобактерий, а также стимулирует развитие многих аэробных и анаэробных бактерий и грибов. При малом содержании бора в почве или в условиях, затрудняющих его выведение из органических соединений, микроорганизмы выступают как конкуренты высших растений в отношении этого элемента, прочно удерживая его в своих клетках в составе органических веществ.
Для многих элементов известны только отдельные звенья превращений, связанных с деятельностью почвенных микроорганизмов. Есть сведения, например, о связывании цинка органическими соединениями в метаболизме грибов; о включении кобальта в молекулу B12 при синтезе этого витамина и др.
Микроорганизмы способны к аккумуляции в своих клетках элементов, которые содержатся в микроколичествах в почвах. Методом радиоавтографии показано, что микробные клетки накапливают естественно-радиоактивные элементы, такие как уран, торий, радий. На пленке после периода экспонирования микробных колоний, выращенных в присутствии указанных элементов, подсчитывают число треков — следов радиоактивного распада элементов, аккумулированных микроорганизмами.
Тионовая бактерия Thiobacillus ferrooxidans вызывает окисление сульфидов и косвенно влияет на миграцию таких элементов, как Cu, Zn, Ni и других, путем создания активного химического окислителя Fe2(SO4)3. Его взаимодействия с соединениями урана и ванадия изменяют валентное состояние этих элементов.
Известна роль микроорганизмов в процессах фракционирования стабильных изотопов некоторых элементов — углерода, азота, селена, лития. Примером может служить деятельность бактерий участвующих в превращениях серы. Первичная сера Земли представлена сульфидами. Изотопный состав серы в горных породах подвержен значительным колебаниям. За стандарт изотопного состава серы принимается сера метеоритов. Отклонения в соотношении легких (32S) и тяжелых (33S, 34S, 36S) изотопов серы есть результат последующего разделения атомов разного веса. Появление кислорода в газовой оболочке Земли привело к образованию сульфатов. При их восстановлении биологическим путем сульфатредуцирующие бактерии производят фракционирование изотопов серы: в H2S они переводят атомы легкой серы 32S, а в остаточном сульфате накапливается избыток тяжелых изотопа 34S. Таким образом, изотопный состав серы океанических сульфатов утяжелен на несколько процентов по сравнению с серой метеоритов, а сульфидные месторождения обогащены легким изотопом серы. По возрасту биогенных отложений серных руд делают попытки определить время появления кислорода на Земле, так как оно примерно совпадает с началом сульфатредукции.
В естественных биогеохимических провинциях, где почва обогащена молибденом, медью, ванадием, свинцом, бором, марганцем, почвенные микроорганизмы проявляют повышенную способность к связыванию этих элементов по сравнению с обедненными провинциями, что связано, возможно, с адаптационными явлениями в отношении этих геохимических факторов среды.
Итак, вовлечение разных элементов в биологический круговорот идет разными путями и имеет разные механизмы. Углерод и азот вовлекаются в построение органических веществ и в основе их циклов лежат процессы синтеза и минерализации органических макромолекул, фиксация и возврат газообразных продуктов в атмосферу. Превращения фосфора и серы связаны с органическими веществами и разрушением минералов. В превращениях калия, железа, марганца, алюминия большую роль играют процессы разрушения и новообразования минералов, которые рассматриваются ниже. И превращения органических веществ, и разложение почвообразующих пород имеют две стороны: обеспечение растений элементами питания и роль в почвообразовании.
БИОЛОГИЧЕСКИЕ ПРОЦЕССЫ В ПОЧВООБРАЗОВАНИИ
Почвообразовательный процесс — это сложная совокупность явлений превращения и перемещения различных веществ в верхнем слое земной коры; взаимодействия малого биологического и большого геологического круговоротов веществ; баланса элементов, воды и тепла. Из разного сочетания этих явлений, которые в различной степени выражены в конкретных условиях, складывается определенный тип почвообразовательного процесса.
В каждом типе почвообразования можно выделить более общие процессы и частные, специфические. К общим относятся циклические процессы поступления и разложения органических веществ, биологической аккумуляции и выноса веществ из почвы, распада и синтеза вторичных минералов. Специфичны для каждого типа процессы гумусообразования и гумусонакопления, разложения первичных минералов и новообразования вторичных минералов. Среди частных почвообразовательных процессов выделяют макро - и микропроцессы. Первые охватывают всю почвенную толщу и ведут к образованию почвенного профиля, вторые сосредоточены в микрозонах, в отдельных очагах, что особенно характерно для некоторых микробиологических преобразований Процессы в пределах одного горизонта иногда называют мезопроцессами.
В последние годы в почвоведении развивается новое учение об элементарных почвенных процессах (ЭПП), основы которого были заложены трудами , , . Под такими процессами понимают те, которые относятся только к почве. Они являются общими для всех типов, но их разное сочетание дает все разнообразие почв. выделяет 13 таких элементарных почвенных процессов, другие исследователи – больше. Элементарными их назвали потому, что из них, как из кирпичиков, слагается весь почвообразовательный процесс. Эти процессы могут быть, в свою очередь, очень сложными. Некоторые из них имеют биологическую природу и в основе их лежит биохимический механизм.
(1980) предлагает по аналогии с ЭПП рассматривать и ЭПБП – элементарные почвенно-биологические процессы, относя к их числу следующие: 1 – разложение растительного опада; 2 – образование гумуса; 3 – разложение гумуса микроорганизмами; 4 – деструкция минералов почвообразующей породы почвенными микроорганизмами и их метаболитами; 5 – микробное минералообразование.
Кроме названных пяти процессов, которые обязательно проявляются во всех типах почв, есть еще ряд процессов характерных только для определенных типов почвообразования.
РАЗЛОЖЕНИЕ РАСТИТЕЛЬНЫХ ОСТАТКОВ И ФОРМИРОВАНИЕ ПОДСТИЛКИ
Разложение растительных остатков совершается как в толще почвы, так и на ее поверхности. Отмирающие корневые системы однолетних и многолетних растений, а также подземные части – луковицы, клубни, разлагаются в почве. Надземные части растений после отмирания в виде отпада и опада накапливаются на поверхности почвы. Из них формируется под лесами лесная подстилка, под травянистыми формациями ветошь и степной войлок.
Превращение опада в подстилку осуществляется сложным комплексом организмов, включая и представителей почвенной фауны. Характер разложения и его скорость определяются тремя главными факторами: составом растительного материала, водно-термическим режимом и комплексом организмов – разлагателей. В процессе разложения одна часть веществ полностью минерализуется, другая – консервируется, и третья часть включается в гумус. При этом синтезируется живая биомасса обитателей подстилки, живущих сапротрофно за счет разлагаемого мертвого органического субстрата. ниже 20.
По мере разложения происходит изменение опада и превращение его в аморфную массу. Это прослеживается на вертикальном профиле в виде слоев разной степени разложенности опада. Верхний слой — L — опавшие листья; средний ферментативный — F и нижний гумусовый — Н. Такая стратификация подстилки — результат последовательно сменяющих друг друга, «конвейерных», процессов, которые связаны со сменой работающих комплексов организмов. Это явление носит название сукцессии.
Для L-слоя характерно общее обилие и высокое экологическое разнообразие организмов, активность которых носит сезонный характер и выражается в цикличности процессов. В этом слое среди микроорганизмов преобладают эпифиты, попадающие в подстилку с опадом: высокая доля неспоровых бактерий и дрожжеподобных грибов, в частности Aureobasidium pullulans. Из макромицетов — шляпочные грибы родов Marasmius, Micena, Collybia. Много нематод, коллембол и панцирных клещей — орибатид. В L-слое происходят процессы разложения простых углеводов, пектина и белков.
В F-слое отмечается самое активное дыхание за счет очень высокой общей численности микроорганизмов. Велико и их разнообразие. Преобладающая группа — базидиальные грибы, а также представители экологической группы разрушителей целлюлозы: Chaetomium, Trichoderma, Mycogone. Им сопутствуют бактерии и члены сахаролитического комплекса — дрожжи и мукоровые грибы. В этом слое много представителей микрофауны — коллембол, клещей. Здесь идет более глубокий распад органических веществ, включая целлюлозу, хитин, лигнин. Одновременно протекают процессы синтеза гумусовых веществ.
В Н-слое происходит снижение интенсивности дыхания в результате уменьшения численности и разнообразия комплекса грибов в первую очередь. Остаются главным образом гумусовые сапрофиты. Из бактерий — споровые и много актиномицетов, которых почти нет в слое L. Здесь завершаются процессы распада, происходит усложнение гумусовых соединений. В гумусовом слое большую долю составляют выбросы дождевых червей и других беспозвоночных; они активно заселяются актиномицетами.
При переходе к минеральным горизонтам падает общая численность микроорганизмов и микроартропод, резко меняется состав экологических и таксономических групп.
Сукцессионные изменения, таким образом, касаются всех групп биоты — животных, грибов и бактерий — и отражаются на интенсивности и направленности процессов разложения. Особенно четко они прослеживаются на грибных комплексах. В группе мелких членистоногих (микроартропод) по мере сукцессии происходит замена доминирования поверхностных форм подстилочно-почвенными, а затем почвенными. Наиболее заметна эта смена у нематод, менее — у ногохвосток и меньше всего — у панцирных клещей.
Скорость поступления опада, как правило, выше, чем скорость его разложения. В разных условиях минерализация опада сильно различается. В субтропическом лесу, где круглый год положительные температуры и высокая влажность, ежегодный опад почти целиком «сгорает» и почва почти голая, без подстилки. В хвойных лесах севера с коротким периодом положительных температур опад разлагает медленнее и накапливается в силу климатических условий и из химического состава хвои. В целом процесс формирования подстилки сравним с поверхностным компостированием конвейерного характера.
ОБРАЗОВАНИЕ И РАЗЛОЖЕНИЕ ГУМУСА
Накопление отмерших растительных остатков в виде особого слоя подстилки или войлока на поверхности почвы создает особое хранилище элементов питания, которые по мере разложения постепенно поступают в почву. Они либо используются растениями и микроорганизмами, либо аккумулируются и стабилизируются в форме гумусовых веществ, определяющих почвенное плодородие. Гумус составляет 90% общего запаса органических веществ в почвах и представлен группой высокомолекулярных соединений разной химической природы, главным образом высокополимерных органических кислот. Азот в гумусе входит в состав аминокислот белковой фракции и в гетероциклы, которые не разрушаются при кислотном гидролизе.
Гумус сильно различается как по качеству, так и по количеству в почвах разных типов вследствие того, что он образуется из растительных остатков неодинакового химического состава и в различных условиях, а в его формировании участвует комплекс организмов, специфичный для каждой природной зоны.
Образование и накопление гумуса в почве — это суммарный итог многих биологических и абиогенных процессов. Исходный этап — разложение растительного опада и корневых остатков.
В лесных ландшафтах процессы трансформации активно протекают в верхних слоях, в подстилке; в травяных они опущены на глубину, где сосредоточена основная масса корней. В связи с этим различна доля участия животных и микроорганизмов в этих процессах.
Исследование процессов гумификации в связи с деятельностью почвообитающих организмов составляет экологическое направление в решении проблемы гумуса. Это направление берет начало с конца прошлого века, когда датчанин , работая с лесными почвами, описал три типа гумуса — муль, модер и мор, которые образуются как результат взаимодействия органических и минеральных соединений, с одной стороны, и почвенных организмов и растительности с другой.
Нейтральный (мягкий, муллевый) гумус образуется под широколиственным лесом. Он характерен для бурых лесных почв, где подстилка обычно не накапливается из-за активной ее переработки беспозвоночными животными с участием дождевых червей, а также высокой активности микроорганизмов. Мягкий гумус состоит из органоминеральных соединений и имеет слабокислую реакцию. Такой тип гумуса образуется также под травянистыми формациями. Соотношение C : N в этом гумусе обычно ниже 20.
Грубый гумус типа мор образуется в хвойных лесах, где процессы разложения опада протекают медленно, где бедна почвенная фауна, а в ее составе отсутствуют настоящие сапрофаги. Разложение подстилки осуществляется в основном грибами. При недостатке оснований образующиеся гумусовые кислоты не нейтрализуются. Гумус поэтому имеет кислую реакцию. Отношение С: N в грубом гумусе всегда выше 20.
Гумус типа модер — промежуточный между мягким и грубым гумусом. Он формируется под смешанными лесами. Органоминеральные комплексы менее насыщены основаниями, чем в муле. Образование гумуса типа модер протекает в условиях достаточно быстрой минерализации растительных остатков, в переработке которых участвуют почвенные беспозвоночные. Однако в этих почвах обычно отсутствуют дождевые черви.
Роль животных в разложении органических веществ в связи с гумусообразованием оценивается по-разному в зависимости от используемых методов. По дыханию (выделению СО2) беспозвоночные вместе с простейшими составляют 15%, а 85% — микроорганизмы. Биомасса почвенных животных в 100—120 раз меньше, чем растительных остатков. Однако лабораторные и полевые опыты свидетельствуют о сильном (в 6—8 раз) замедлении темпов разложения в отсутствие животных.
Биохимическая концепция гумусообразования, в разработку которой большой. вклад внесла , сводится к следующему. Микробное разложение растительных остатков сопровождается потерей массы (до 75%) и выделением СО2. Первоисточники структурных единиц гумусовых веществ — углеводы растительных тканей, переработанные микроорганизмами, лигнин, флавоноиды, таннины (полифенолы), а также азотсодержащие продукты микробного ресинтеза. В процессе формирования гумуса происходит конденсация структурных единиц с участием микробных (главным образом, грибных) ферментов полифенолоксидаз. В конечных процессах имеет место гетерополиконденсация и стабилизация за счет изомеризации и перегруппировок (рис. 64).
Микроорганизмы участвуют в гумусообразовании не только косвенно, благодаря процессам разложения, но и непосредственно включаясь в синтез гумусовых веществ.
На возможность участия темноокрашенных продуктов метаболизма микроорганизмов в образовании гумуса указывали еще (1886) и (1952). Более 60 лет назад писал о том, что преобладающая часть гумуса состоит из микробной плазмы.
Специфические вещества гумуса составляют 90% и представлены гуминовыми кислотами (50—80%) и полисахаридами. Гуминовые кислоты — гетерополиконденсаты с большим числом фенольных и индольных единиц (Кононова, 1963). Грибы могут образовывать циклические продукты из соединений с открытой цепью, а также разлагать лигнин до фенольных мономеров и дальше окислять их полифенолоксидазами.
К фенольному ядру присоединяются азотсодержащие молекулы и образуются темноокрашенные вещества — хромопротеиды меланоидного типа. Меланины по химическому составу очень близки к гуминовым кислотам: они не растворяются в органических растворителях, но извлекаются щелочами и осаждаются кислотами; обесцвечиваются окислителями, например, перекисью водорода, марганцовокислым калием
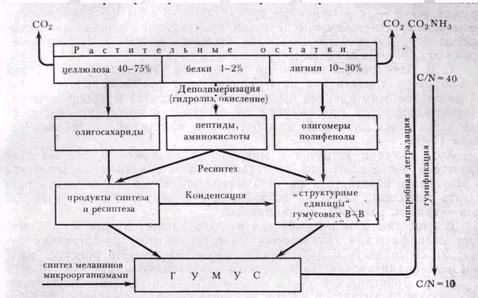
Рис.16. Схема образования и разложения гумуса (Бабьева, Зенова, 1983)
Те и другие имеют одинаковые спектры поглощения в ультрафиолетовом и видимом свете; у них сходный элементный состав и некоторые другие свойства. Меланины с такими характеристиками обнаружены у многих почвенных микромицетов родов Aspergillus, Cladosporium, Stachybotrys, Alternaria, Stemphylium, Aureobasidium и др. Пигменты синтезируются внутриклеточно и остаются во внешней среде после отмирания и лизиса мицелия, так как они устойчивы к микробной деградации.
Темные вещества меланинового характера образуют не только грибы, но и прокариоты. Они найдены у актиномицетов и некоторых бактерий, например у Azotobacter chroococcum.
Таким образом, возможен вклад микроорганизмов в образование гумуса не только через «производство структурных единиц» моно - и полимеров в процессе разложения растительных остатков, но и благодаря непосредственному синтезу гумусовых веществ типа черных пигментов — меланинов. В гумус включаются помимо микробных меланинов другие компоненты биомассы. Опытами с 14С было показано, что меченый углерод из микробной биомассы, внесенной в почву, через несколько месяцев обнаруживается в составе гумусовых кислот. Встает вопрос: какая доля гумуса почвы образуется из преобразованного растительного материала и какая — из микробной биомассы и продуктов обмена микроорганизмов? Ответа на этот вопрос пока дать нельзя. Он связан со многими проблемами почвенной биологии и биохимии и, прежде всего — с выяснением продуктивности почвенных микроорганизмов, энергетическим обеспечением продукционного процесса и скоростью оборачиваемости микробной биомассы в почвах. В настоящее время это спорные вопросы микробиологии почв.
пишет, что имеющиеся запасы гумуса в почвах можно рассматривать как интегральный итог продолжавшегося в течение длительного времени продукционного процесса микроорганизмов, сопровождавшегося разложением их остатков и консервацией наиболее устойчивых клеточных компонентов и продуктов микробного обмена (1980).
Хотя гумус и устойчив к микробному разложению, все же этот процесс в почве постоянно протекает, и часть гумуса минерализуется в результате воздействия на него микроорганизмов. Способность разлагать гумусовые вещества доказана для многих почвенных организмов — грибов, бактерий, актиномицетов.
В биологии почв имеются два взгляда на этот вопрос: 1) существует специфическая группировка микроорганизмов, разлагающих гумус; 2) способность к разложению гумусовых веществ присуща многим неспециализированным почвенным микроорганизмам.
делил микрофлору почв на зимогенную, привносимую с растительной массой, и автохтонную — собственно почвенную, живущую за счет разложения гумусовых веществ. Эту позицию развивает далее Е. 3. Теппер, связывающая функцию разложения гумуса в почве с деятельностью главным образом нокардий (1976).
Разные фракции гумуса неодинаково подвержены микробному разложению. Тот факт, что в почве обнаруживают гумус очень древнего возраста, свидетельствует о выпадении его из биологического круговорота. Наиболее активно разрушается гумус в присутствии доступных микроорганизмам водорастворимых органических соединений Возможно, гумус вовлекается в процессы кометаболизма и легче разлагается в условиях соокисления. Эти процессы могут проводить и неспецифические микроорганизмы. Многими экспериментальными работами показано участие в разрушении почвенного гумуса грибов из родов Aspergillus, Penicillium и др. При этом одни виды использовали препараты фульвокислот как источники углерода и азота, другие потребляли либо углерод, либо азот. В работах продемонстрировано отложение железа в культурах Pedomicrobium, Seliberia и некоторых других микроорганизмов на средах с железогумусовыми комплексами. Это свидетельствует о разрушении последних и использовании гуминовой части как источника органических веществ в обмене гетеротрофных бактерий.
УЧАСТИЕ ПОЧВЕННЫХ МИКРООРГАНИЗМОВ. В РАЗРУШЕНИИ И НОВООБРАЗОВАНИИ МИНЕРАЛОВ
Рассмотренные выше превращения калия, железа, алюминия, фосфора и серы а также редких элементов связаны с процессами разрушения и новообразования минералов в почвах. Эти процессы, с одной стороны обеспечивают потребности растений и почвенных микроорганизмов в элементах минерального питания, а с другой — влияют на такие свойства почвы, как ее поглотительная способность, структура, влагодержание. Таким образом, в совокупности процессы образования минералов и их деструкции формируют тот комплекс свойств, который определяет почвенное плодородие.
Минеральные элементы аккумулированы в литосфере и в ходе почвообразовательного процесса вовлекаются в биологический круговорот и попадают в биосферу. Именно в этом звене два круговорота — большой геологический и малый биологический — тесно сплетаются между собой.
Процессы извлечения зольных веществ из почвообразующих пород имеют значение не только на первых стадиях формирования почв, когда это единственный источник элементов питания, но и в тех условиях развитых почв, где имеет место активный вынос растворимых веществ из почвенного профиля.
Микроорганизмам почвы принадлежит важнейшая, хотя и не исключительная, роль в деструкции минералов почвообразующих пород. В этих процессах участвуют водоросли, лишайники, грибы, бактерии и актиномицеты. Особое значение имеют микроорганизмы-кислотообразователи, например, нитрификаторы, тионовые бактерии, микромицеты. Несомненно, велика роль лишайниковых кислот. Под корочками литофильных лишайников всегда можно обнаружить слой разрушенной горной породы.
О биохимических механизмах деструкции минералов было сказано в разделе о превращениях калия. В результате воздействия на минералы кислот, слизей и щелочей происходит либо полное растворение минерала с образованием аморфных продуктов распада, либо ионы калия, например, изоморфно замещаются ионами водорода и натрия без разрушения кристаллических решеток минерала. Химические элементы, входящие в состав минерала, извлекаются необязательно пропорционально их содержанию и соотношению в исходном материале. Биологическое выветривание может привести к преобразованию одного минерала в другой благодаря изменению химического состава при избирательном извлечении элементов. Например, при разложении алюмосиликатов с участием гетеротрофных бактерий происходит последовательное извлечение сначала щелочных элементов, затем щелочноземельных и в последнюю очередь — кремния и алюминия.
Устойчивость минералов к микробному разрушению определяется не только прочностью структуры кристаллической решетки, но и условиями среды, в которой протекает процесс, а также специфичностью микрофлоры и, следовательно, биохимическим механизмом ее воздействия.
ЛИТЕРАТУРА
1. Аристовская процессов почвообразования. Л.: Изд-во ЛГУ. 1980, 246 с.
2. , Зенова почв. М.:Изд-во Моск. Ун-та, 1983, 248 с.
3. Грабович прокариот в круговороте серы // Соросовский образовательный журнал, 1999, №12, с. 16-20.
4. , Павленко бактерий. Л.: Изд-во ЛГУ, 19c.
5. Громов мир архей // Соросовский Образовательный Журнал. 1997. № 4. C. 23-26.
6. Заварзин и состав атмосферы. М.: Наука, 1984.– 199 с.
7. , Колотилова в природоведческую микробиологию: Учебное пособие.– М.: Книжный дом «Университет», 2001. – 256 с.
8. Кальдерные микроорганизмы / Под ред. . M.: Наука, 19c.
9. Камшилов биосферы. Изд. Наука,1974.С. 254
10. Кондратьева и метилотрофы. М.: Изд-во МГУ, 19c.
11. Малахов - автотрофные животные // Соросовский Образовательный Журнал. 1997. № 9. C. 18-26.
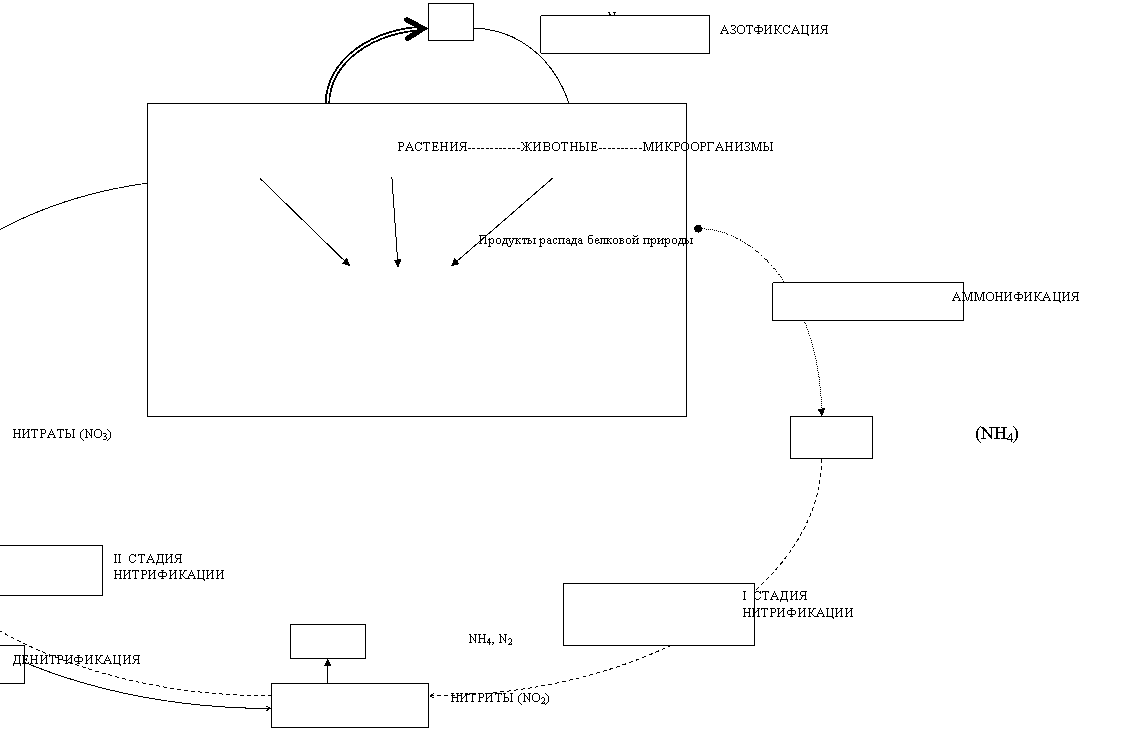
Рис. 8

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



