МЕТОДИЧЕСКИЕ УКАЗАНИЯ ДЛЯ СТУДЕНТОВ
К занятию по цитологии
Тема занятия: Роль цитологических исследований в гематологии. Структура и особенности функционирования костного мозга. Нормальный гемопоэз. Гемопоэтические факторы.
Гематология – это раздел медицины, изучающий кровь, органы кроветворения, и заболевания крови. Гематология изучает этиологию, диагностику, лечение, прогнозирование и предотвращение заболеваний системы крови, которые влияют на производство крови и ее компонентов, а именно клетки крови, гемоглобин, белки крови, и механизм коагуляции (свертывание крови).
Предметы и области изучения гематологии
1. Кровь
· Венозная кровь
· Венозная пункция
· Гемопоэз
· Клинический анализ крови
· пуповинная кровь
2. Красные кровяные клетки
· Формирование эритроцитов
· Эритропоэтин
· Метаболизм железа
· Гемоглобин
· Гликолиз
· Пентозофосфатный путь
3. Белые кровяные клетки
4. Тромбоциты
5. Ретикуло-эндотелиальная система
· Костный мозг человека
· Селезенка
· Печень
6. Лимфатическая система
7. Переливание крови
· Плазма крови
· Донорство крови
· группы крови
8. Гемостаз
· Свертывание крови
· Витамин K
9. Система комплемента
· Антитела
10. Аномалии молекулы гемоглобина или скорости синтеза гемоглобина
· Анемии (нехватка эритроцитов и гемоглобина)
· Гемобластозы
· коагулопатии (нарушения кровотечения и коагуляции)
· Серповидноклеточная анемия
Цель занятия: Знать структуру и особенности функционирования костного мозга, основные цитологические характеристики гемопоэтических элементов. Ознакомиться с основными гемопоэтическими факторами, а также причинами и следствием их недостаточности.
Знать:
· Расположение костного мозга в организме плода и взрослого человека
· Основные клеточные элементы костного мозга
· Стадии созревания клеток крови в костном мозге
· Основные гемопоэтические факторы и состояния, связанные с их недостаточностью
Уметь:
· Интерпретировать результаты миелограмм в норме и при различных заболеваниях системы кроветворения
· Ассоциировать изменения в организме с возможными изменениями в миелограмме и периферической крови
Кроветворением, или гемопоэзом, называют образование клеток крови. Различают эмбриональный гемопоэз, который происходит в эмбриональный период и приводит к развитию крови, как ткани, и постэмбриональный гемопоэз, который представляет собой процесс физиологической регенерации крови.
Костный мозг — это составляющая часть костей скелета, которая заполняет внутреннюю полость кости и осуществляет в организме функцию образования клеток крови. Существует 2 вида костного мозга: красный костный мозг, состоящий в основном из кроветворной миелоидной ткани и желтый, основой которого являются клетки жировой ткани.
Красный костный мозг образуется в организме человека в период эмбрионального развития. В этот период все кости организма содержат красный костный мозг, который активно функционирует. В подростковом возрасте кроветворная ткань в полостях трубчатых костей меняется на жировую, соответственно, костный мозг становится желтым. У взрослого человека красный костный мозг в норме содержится в плоских костях, позвонках, эпифазах и диафизах трубчатых костей.
Красный костный мозг — важнейший орган кроветворной системы, осуществляющий гемопоэз, или кроветворение — процесс создания новых клеток крови взамен погибающих и отмирающих.
Костный мозг — единственная ткань взрослого организма, в норме содержащая большое количество незрелых, недифференцированных и низкодифференцированных клеток, так называемых стволовых клеток, близких по строению к эмбриональным клеткам. Все другие незрелые клетки, например незрелые клетки кожи, всё же имеют большую степень дифференцировки и зрелости, чем клетки костного мозга, и имеют уже заданную специализацию.
Красный костный мозг состоит из фиброзной ткани (стромы) и собственно кроветворной ткани. В кроветворной ткани костного мозга выделяют несколько ростков гемопоэза, количество которых увеличивается по мере созревания. Зрелых ростков в красном костном мозге пять:
· Эритроцитарный
· Гранулоцитарный
· Лимфоцитарный
· Моноцитарный
· Мегакариоцитарный
Каждый из этих росков даёт, соответственно, следующие клетки и постклеточные элементы: эритроциты; эозинофилы, нейтрофилы и базофилы; лимфоциты; моноциты; тромбоциты.
Развитие ростков гемопоэза представляет собой сложный процесс дифференцировки клеток. Родоначальники всех ростков названы полипотентными клетками за их способность дифференцироваться в клетки всех ростков гемопоэза под действием цитокинов. Так же эти клетки называют колониеобразующими элементами (КОЭ) за их локальное расположение в костном мозге или стволовыми клетками крови (СКК). Количество полипотентных стволовых клеток, то есть клеток, которые являются самыми первыми предшественниками в ряду кроветворных клеток, в костном мозге ограничено, и они не могут размножаться, сохраняя полипотентность, и тем самым восстанавливать численность. Ибо при первом же делении полипотентная клетка выбирает путь развития, и её дочерние клетки становятся либо мультипотентными клетками, у которых выбор более ограничен (только в эритроцитарный или лейкоцитарный ростки), либо мегакариобластами и затем мегакариоцитами — клетками, от которых отшнуровываются тромбоциты.
Под действием цитокинов КОЭ начинают специализироваться, переходя на следующий этап — олигопотентные клетки, вариантов дифференцировки у них уже меньше. Второе название этих клеток — колониеобразующие единицы (КОЕ), поскольку они расположены более мелкими группами, чем КОЭ. КОЕ неоднородны между собой: выделяют колониеобразующие единицы гранулоцитарно-эритроцитарно-миелоцитарно-макрофагального (КОЕ-ГЭММ) и колониеобразующие единицы лимфоцитарного (КОЕ-Л) ростков. Дальнейшее развитие КОЕ ещё более специфично.
Под действием цитокинов КОЕ-ГЭММ даёт следующие три типа клеток: колониеобразующая единица гранулоцитов и моноцитов (КОЕ-ГМ), колониеобразующая единица эритроцитов (КОЕ-Э) и колониеобразующая единица мегакариоцитов (КОЕ-МГЦ). Эти переходы инициируются лейкопоэтином, эритропоэтином и тромбопоэтином соответственно. Эти КОЕ — последние, дальнейшие клетки ростков называются бластами, поскольку они уже становятся на один путь дифференцировки в одну конечную клетку. Так, КОЕ-ГМ развивается либо в промонобласт, либо в програнулобласт; КОЕ-Э развивается в эритробласт; КОЕ-МГЦ развивается в мегакариобласт. Таким образом, вкупе с лимфоидным ростков, получаются 5 вышеперечисленных ростков гемопоэза.
Клеточный состав костного мозга (миелограмма) и периферической крови в норме.
Клеточный состав костного мозга оценивается по результатам исследования пунктата грудины или подвздошной кости, полученного с помощью иглы . В костномозговом пунктате клеточные элементы представлены кроветворными и некроветворными клетками, клетками ретикулярной стромы и паренхимы. На долю представителей стромальных клеток (фибробласты, остеобласты, жировые и эндотелиальные клетки) приходится не более 2%. Общее количество клеток паренхимы костного мозга составляет 98-99%, причем в их число входят как морфологически нераспознаваемые родоначальные элементы, так и морфологически распознаваемые, начиная с бластных (миелобластов, эритробластов и др.) и заканчивая зрелыми клетками. Все ростки кроветворения начинаются с бластных элементов, продолжаются промежуточными формами созревания и заканчиваются зрелыми клетками; при этом количество бластных элементов каждого ростка варьирует в пределах от 0,1 до 1,1-1,7%. Темп созревания костномозговых элементов отражает соотношение созревающих и зрелых клеток. В миелограмме определяют также абсолютное количество различных клеток - миелокариоцитов (клеток, содержащих ядро), в сумме оно варьирует от 41,6 до 195 в 1 мкл (в тысячах) и мегакариоцитов - в норме 50-150 в 1 мкл. Процентное соотношение различных клеточных элементов в миелограмме составляет в норме: лимфоцитов - 4,3-13,7%, моноцитов - 0,7-3,1%, плазматических клеток - 0,1-1,8%.
Важно отметить, что родоначальные клетки всех ростков кроветворения (бласты), как правило, имеют сходные морфологические черты: крупное ядро с ядрышками, которое окружено узким ободком цитоплазмы. Вместе с тем имеются и отличия, которые позволяют отнести бласты к определенному ростку. Так, например, все виды миелобластов (нейтрофильные, базофильные, эозинофильные) содержат в цитоплазме зернистость, которая в нейтрофильных - мелкая и в небольшом количестве, в базофильных - крупная и почти черного цвета, в эозинофильных - коричневатого цвета. Эритробласт отличается ярко-базофильной цитоплазмой без зоны просветления вокруг ядра, отсутствием зернистости в цитоплазме; мегакариобласт - более грубой структурой ядра, ярко-базофильной отростчатой цитоплазмой без признаков зернистости; монобласт - бобовидной формой ядра с нежной сетчатой структурой, нежно-голубой цитоплазмой; лимфобласты обеих популяций (Т и В) - округлым или овальным ядром с 1-2 ядрышками, нежно-базофильной цитоплазмой с перинуклеарной зоной просветления, причем Т-лимфобласты содержат в цитоплазме небольшое количество азурофильных зерен. Для более точной идентификации бластов проводят цитохимические и иммунофенотипические исследования.
В созревающих клетках структура ядра более грубая, ядрышки отсутствуют или присутствуют их остатки, размеры ядра меньше, чем у родоначальной клетки, площадь цитоплазмы увеличена. В гранулоцитарном ростке изменяется форма ядра, которая из круглой сначала становится бобовидной, из бобовидной - палочковидной, из палочковидной - сегментированной. Зернистость в цитоплазме различается по цвету: в эозинофилах она оранжевая, в базофилах - черная, в нейтрофилах - розово-фиолетовая.
Таким образом, костномозговая пункция позволяет определить цитологический состав кроветворных клеток.
Клеточный состав костного мозга в норме, %
Показатель миелограммы | Среднее значение | Пределы нормальных колебаний |
Ретикулярные клетки | 0,9 | 0,1-1,6 |
Бласты | 0,6 | 0,1-1,1 |
Миелобласты | 1,0 | 0,2-1,7 |
Нейтрофильные клетки: промиелоциты миелоциты метамиелоциты | 2,5 9,6 11,5 | 1,0-4,1 7,0-12,2 8,0-15 |
палочкоядерные сегментоядерные | 18,2 18,6 | 12,8-23,7 13,1-24,1 |
Все нейтрофильные элементы | 60,8 | 52,7-68,9 |
Эозинофилы (всех генераций) | 3,2 | 0,5-5,8 |
Базофилы | 0,2 | 0-0,5 |
Эритробласты | 0,6 | 0,2-1,1 |
Пронормоциты | 0,6 | 0,1-1,2 |
Нормоциты: базофильные полихроматофильные оксифильные | 3,0 12,9 3.2 | 1,4-4,6 8,9-16,9 0,8-5,6 |
Все эритроидные элементы | 20,5 | 14,5-26,5 |
Лимфоциты | 9,0 | 4,3-13,7 |
Моноциты | 1,9 | 0,7-3,1 |
Плазматические клетки | 0,9 | 0,1-1,8 |
Для диагностики гипопластических состояний, выявления лейкозных инфильтратов и раковых метастазов, а также миелодиспластического синдрома и некоторых видов костной патологии используют трепанобиопсию подвздошной кости, которую проводят с помощью специального троакара. Она позволяет более точно установить тканевые соотношения «паренхима/жир/костная ткань», которые в норме составляют 1:0,75:0,45. В патологических условиях эти соотношения изменяются, иным становится клеточный состав паренхимы и костной ткани.
При действии больших доз ионизирующего излучения, как известно, в первую очередь страдают ткани, обладающие наибольшей пролиферативной активностью в организме. К таким тканям относится костный мозг человека. Таким образом, при острой лучевой болезни высокой степени тяжести большинство кроветворных клеток погибает, образуя картину малоклеточного (пустого) костного мозга. В препарате видны соединительнотканные септы и незначительное количество зрелых клеточных элементов. По мере восстановления в костном мозге появляются разнообразные бластные формы. Картина периферической крови при этом заболевании характеризуется панцитопенией и агранулоцитозом.
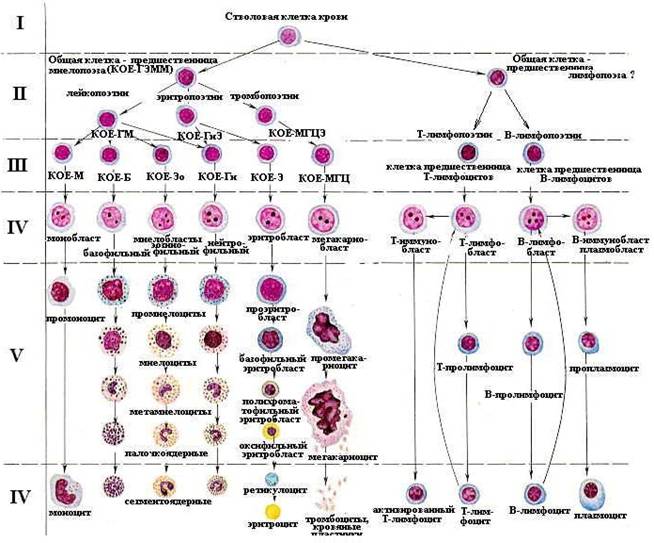
Рис. 1 Схема гемопоэза
Регуляция гемопоэза
Кроветворение регулируется:
· факторами роста, обеспечивающими пролиферацию и дифференцировку СКК и последующих стадий их развития,
· факторами транскрипции, влияющими на экспрессию генов, определяющих направление дифференцировки гемопоэтических клеток,
· витаминами, гормонами.
Факторы роста включают колониестимулирующие факторы (КСФ), интерлейкины и ингибирующие факторы. Они являются гликопротеинами, действующими и как циркулирующие гормоны, и как местные медиаторы, регулирующие гемопоэз и дифференцировку специфических типов клеток. Почти все факторы роста действуют на СКК, КОЕ, коммитированные и зрелые клетки. Однако отмечаются индивидуальные особенности действия этих факторов на клетки-мишени.
КСФ действуют на специфические клетки или группы клеток на различных стадиях дифференцировки. Например, фактор роста стволовых клеток влияет на пролиферацию и миграцию СКК в эмбриогенезе. В постнатальном периоде на гемопоэз оказывают влияние несколько КСФ, среди которых наиболее изучены факторы, стимулирующие развитие гранулоцитов и макрофагов (ГМ-КСФ, Г-КСФ, М-КСФ), а также интерлейкины.
Большинство указанных факторов выделено и применяется для лечения различных болезней. Для получения их используются биотехнологические методы.
Дифференцировка полипотентных клеток в унипотентные определяется действием ряда специфических факторов, поэтинов — эритропоэтинов (для эритробластов), гранулопоэтинов (для миелобластов), лимфопоэтинов (для лимфобластов), тромбопоэтинов (для мегакариобластов).
Большая часть эритропоэтина образуется в почках. Его образование регулируется содержанием в крови кислорода, которое зависит от количества циркулирующих в крови эритроцитов. Снижение числа эритроцитов и соответственно парциального давления кислорода, является сигналом для увеличения продукции эритропоэтина. Эритропоэтин действует на чувствительные к нему КОЕ-Э, стимулируя их пролиферацию и дифференцировку, что в конечном итоге приводит к повышению содержания в крови эритроцитов. При хронической болезни почек выработка эритропоэтина снижается, поэтому такие пациенты нуждаются в медикаментозном его введении.
Тромбопоэтин синтезируется в печени, стимулирует пролиферацию КОЕ-МГЦ, их дифференцировку и образование тромбоцитов.
Ингибирующие факторы дают противоположный эффект, т. е. тормозят гемопоэз; их недостаток может быть одной из причин лейкемии, характеризующейся значительным увеличением числа лейкоцитов в крови. Выделен ингибирующий лейкемию фактор (ЛИФ), который тормозит пролиферацию и дифференцировку моноцитов-макрофагов.
Витамины необходимы для стимуляции пролиферации и дифференцировки гемопоэтических клеток. Витамин В12 поступает с пищей и соединяется с внутренним фактором (Касла), который синтезируется париетальными клетками желудка. Образуемый при этом комплекс, в присутствии ионов Са2+, соединяется с рецепторами эпителиоцитов подвздошной кишки и всасывается. При всасывании в эпителиоциты поступает лишь витамин В12, а внутренний фактор освобождается. Витамин В12 поступает с кровью в костный мозг, где влияет на гемопоэз, и в печень, где может депонироваться. Нарушение процесса всасывания при различных заболеваниях желудочно-кишечного тракта может служить причиной дефицита витамина В12 и нарушений в гемопоэзе.
Пернициозная анемия - это синдром, связанный с недостатком B12 и фолиевой кислоты в организме. Характеризуется наличием в костном мозге большого количества крупных незрелых предшественниковэритроцитов (мегалобластов). Наблюдается также нарушение сегментации нейтрофилов (вплоть до полного отсутствия сегментации) и деформация ядер других гранулоцитов.
При дефиците витамина B12 на фоне анемической клинической картины (или без неё) могут возникнуть и неврологические расстройства из-за связанного с дефицитом витамина B12нарушения синтеза жирных кислот. Может наблюдаться демиелинизация и необратимая гибель нервных клеток. Симптомами такой патологии являются онемение или покалывание конечностей и атаксия.
ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
1. Предмет и области изучения гематологии
2. Костный мозг: виды, локализация, строение, функционирование
3. Стволовая клетка крови и ее дифференцировка
4. Колониеобразующие единицы костного мозга, их дифференцировка и взаимосвязь
5. Принципиальная схема костномозгового кроветворения
6. Способы взятия биологического материала для оценки миелограммы: преимущества и недостатки
7. Миелограмма в норме
8. Миелограмма при остром и хроническом лейкозах
9. Миелограмма при острой лучевой болезни
10. Регуляция гемопоэза: факторы роста
11. Регуляция гемопоэза: факторы транскрипции
12. Регуляция гемопоэза: витамины и гормоны
САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
1. Записать протокол практического занятия с указанием его цели и задачи. Дать определение гематологии, красного костного мозга, миелограммы. Внести в протокол принципиальную схему костномозгового кроветворения.
2. Расшифровать миелограммы при различных патологиях кроветворения. Дать заключение с внесением в протокол.




