ГОРМОНЫ В СИСТЕМЕ ИНТЕГРАЦИИ ФУНКЦИЙ ОРГАНИЗМА ЧЕЛОВЕКА. ОСНОВНЫЕ ПРИНЦИПЫ НЕЙРО-ГУМОРАЛЬНОЙ РЕГУЛЯЦИИ ОБМЕНА ВЕЩЕСТВ. МОЛЕКУЛЯРНО-КЛЕТОЧНЫЕ МЕХАНИЗМЫ ДЕЙСТВИЯ ГОРМОНОВ ПЕПТИДНО-БЕЛКОВОЙ ПРИРОДЫ НА КЛЕТКИ-МИШЕНИ. МОЛЕКУЛЯРНО-КЛЕТОЧНЫЕ МЕХАНИЗМЫ ДЕЙСТВИЯ КАТЕХОЛАМИНОВ И ДРУГИХ БИОГЕННЫХ АМИНОВ (ДОФАМИН, СЕРОТОНИН, ГИСТАМИН, МЕЛАТОНИН) НА КЛЕТКИ-МИШЕНИ
ОБЩЕЕ ПОНЯТИЕ О ГОРМОНАХ
Учение о гормонах выделено в самостоятельную науку – эндокринологию. Современная эндокринология изучает химическую структуру гормонов, образующихся в железах внутренней секреции, зависимость между структурой и функцией гормонов, молекулярные механизмы действия, а также физиологию и патологию эндокринной системы . Учреждены специализированные научно-исследовательские институты, лаборатории, издаются научные журналы; созываются международные конференции, симпозиумы и конгрессы, посвященные проблемам эндокринологии. В наши дни эндокринология превратилась в одну из самых бурно развивающихся разделов биологической науки. Она имеет свои цели и задачи, специфические методологические подходы и методы исследования. В нашей стране головным научным учреждением, объединяющим исследования по этим проблемам, является Эндокринологический научный центр РАМН.
http://www. /watch? v=8fh2HmdxQjQ&feature=related
Гормоны относятся к биологически активным веществам, определяющим в известной степени состояние физиологических функций целостного организма, макро - и микроструктуру органов и тканей и скорость протекания биохимических процессов. Таким образом, гормоны – вещества органической природы, вырабатывающиеся в специализированных клетках желез внутренней секреции, поступающие в кровь и оказывающие регулирующее влияние на обмен веществ и физиологические функции. В это определение необходимо внести соответствующие коррективы в связи с обнаружением типичных гормонов млекопитающих у одноклеточных (например, инсулин у микроорганизмов) или возможностью синтеза гормонов соматическими клетками в культуре ткани (например, лимфоцитами под действием факторов роста).
Одной из удивительных особенностей живых организмов является их способность сохранять постоянство внутренней среды – гомеостаз – при помощи механизмов саморегуляции, в которых одно из главных мест принадлежит гормонам. У высших животных координированное протекание всех биологических процессов не только в целостном организме, но и в микропространстве отдельной клетки и даже в отдельном субклеточном образовании (митохондрии, микросомы) определяется нейрогуморальными механизмами, сложившимися в процессе эволюции. При помощи этих механизмов организм воспринимает разнообразные сигналы об изменениях в окружающей и внутренней средах и тонко регулирует интенсивность процессов обмена. В регуляции этих процессов, в осуществлении последовательности протекания множества реакций гормоны занимают промежуточное звено между нервной системой и действием ферментов, которые непосредственно регулируют скорость обмена веществ. В настоящее время получены доказательства, что гормоны вызывают либо быструю (срочную) ответную реакцию, повышая активность предобразованных, имеющихся в тканях ферментов (это свойственно гормонам пептидной и белковой природы), либо, что более характерно, например, для стероидных гормонов, медленную реакцию, связанную с синтезом ферментов de novo. Как будет показано далее, стероидные гормоны оказывают влияние на генетический аппарат клетки, вызывая синтез соответствующей мРНК, которая, поступив в рибосому, служит матрицей для синтеза молекулы белка – фермента. Предполагают, что и другие гормоны (имеющие белковую природу) опосредованно через фосфорилирование негистоновых белков могут оказывать влияние на гены, контролируя тем самым скорость синтеза соответствующих ферментов. Таким образом, любые нарушения синтеза или распада гормонов, вызванные разнообразными причинными факторами, включая заболевания эндокринных желез (состояние гипо - или гиперфункции) или изменения структуры и функций рецепторов и внутриклеточных посредников, приводят к изменению нормального синтеза ферментов и соответственно к нарушению метаболизма. Зарождение науки об эндокринных железах и гормонах относится к 1855 г., когда Т. Аддисон впервые описал бронзовую болезнь, связанную с поражением надпочечников и сопровождающуюся специфической пигментацией кожных покровов. Клод Бернар ввел понятие о железах внутренней секреции, т. е. органах, выделяющих секрет непосредственно в кровь. Броун-Секар показал, что недостаточность функции желез внутренней секреции вызывает развитие болезней, а экстракты, полученные из этих желез, оказывают хороший лечебный эффект. В настоящее время имеются бесспорные доказательства, что почти все болезни желез внутренней секреции (тиреотоксикоз, сахарный диабет и др.) развиваются в результате нарушения молекулярных механизмов регуляции процессов обмена, вызванных недостаточным или, наоборот, избыточным синтезом соответствующих гормонов в организме человека. Термин «гормон» (от греч. hormao – побуждаю) был введен в 1905 г. У. Бейлиссом и Э. Старлингом при изучении открытого ими в 1902 г. гормона секретина, вырабатывающегося в двенадцатиперстной кишке и стимулирующего выработку сока поджелудочной железы и отделение желчи. К настоящему времени открыто более сотни различных веществ, наделенных гормональной активностью, синтезирующихся в железах внутренней секреции и регулирующих процессы обмена веществ. Установлены специфические особенности биологического действия гормонов: а) гормоны проявляют свое биологическое действие в ничтожно малых концентрациях (от 10–6 до 10–12 М); б) гормональный эффект реализуется через белковые рецепторы и внутриклеточные вторичные посредники (мессенджеры); в) не являясь ни ферментами, ни коферментами, гормоны в то же время осуществляют свое действие путем увеличения скорости синтеза ферментов de novo или изменения скорости ферментативного катализа; г) действие гормонов в целостном организме определяется в известной степени контролирующим влиянием ЦНС; д) железы внутренней секреции и продуцируемые ими гормоны составляют единую систему, тесно связанную при помощи механизмов прямой и обратной связей. Под влиянием разнообразных внешних и внутренних раздражителей возникают импульсы в специализированных, весьма чувствительных рецепторах. Импульсы затем поступают в ЦНС, оттуда в гипоталамус, где синтезируются первые биологически активные гормональные вещества, оказывающие «дистантное» действие, так называемые рилизинг-факторы. Особенностью рилизинг-факторов является то, что они не поступают в общий ток крови, а через портальную систему сосудов достигают специфических клеток гипофиза, при этом стимулируют (или тормозят) биосинтез и выделение тропных гормонов гипофиза, которые с током крови достигают соответствующей эндокринной железы и способствуют выработке необходимого гормона. Этот гормон затем оказывает действие на специализированные органы и ткани (органы-мишени), вызывая соответствующие химические и физиологические ответные реакции целостного организма. Наименее изученным до недавнего времени оставался последний этап этой своеобразной дуги – действие гормонов на внутриклеточный обмен. В настоящее время получены доказательства, что это действие осуществляется через так называемые гормональные рецепторы, под которыми понимают химические структуры соответствующих тканей-мишеней, содержащие высокоспецифические участки (углеводные фрагменты гликопротеинов и ганглиозидов) для связывания гормонов. Результатом подобного связывания является инициация рецепторами специфических биохимических реакций, обеспечивающих реализацию конечного эффекта соответствующего гормона. Рецепторы гормонов белковой и пептидной природы расположены на наружной поверхности клетки (на плазматической мембране), а рецепторы гормонов стероидной природы – в ядре. Общим признаком всех рецепторов независимо от локализации является наличие строго пространственного и структурного соответствия между рецептором и соответствующим гормоном.
http://www. /watch? v=3LW7TSBcFjE&feature=related
Молекулярные механизмы передачи гормонального сигнала и роль вторичных мессенджеров (посредников) в реализации гормонального эффекта подробно изложены в конце данной главы.
НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ ГОРМОНОВ
Химическая природа почти всех известных гормонов выяснена в деталях (включая первичную структуру белковых и пептидных гормонов), однако до настоящего времени не разработаны общие принципы их номенклатуры. Химические наименования многих гормонов точно отражают их химическую структуру и очень громоздкие. Поэтому чаще применяются тривиальные названия гормонов. Принятая номенклатура указывает на источник гормона (например, инсулин – от лат. insula – островок) или отражает его функцию (например, пролактин, вазопрессин). Для некоторых гормонов гипофиза (например, лютеинизирующего и фолликулостимулирующего), а также для всех гипоталамических гормонов разработаны новые рабочие названия.
http://www. /watch? v=kIPYVV4aThM&feature=related
Аналогичное положение существует и в отношении классификации гормонов. Гормоны классифицируют в зависимости от места их природного синтеза, в соответствии с которым различают гормоны гипоталамуса, гипофиза, щитовидной железы, надпочечников, поджелудочной железы, половых желез, зобной железы и др. Однако подобная анатомическая классификация недостаточно совершенна, поскольку некоторые гормоны или синтезируются не в тех железах внутренней секреции, из которых они секретируются в кровь (например, гормоны задней доли гипофиза, вазопрессин и окситоцин синтезируются в гипоталамусе, откуда переносятся в заднюю долю гипофиза), или синтезируются и в других железах (например, частичный синтез половых гормонов осуществляется в коре надпочечников, синтез простагландинов происходит не только в предстательной железе, но и в других органах) и т. д. С учетом этих обстоятельств были предприняты попытки создания современной классификации гормонов, основанной на их химической природе. В соответствии с этой классификацией различают три группы истинных гормонов: 1) пептидные и белковые гормоны, 2) гормоны – производные аминокислот и 3) гормоны стероидной природы. Четвертую группу составляют эйкозаноиды – гормоноподоб-ные вещества, оказывающие местное действие. Пептидные и белковые гормоны включают от 3 до 250 и более аминокислотных остатков. Это гормоны гипоталамуса и гипофиза (тиролиберин, соматолиберин, соматостатин, гормон роста, кортикотропин, тиреотропин и др.), а также гормоны поджелудочной железы (инсулин, глюкагон). Гормоны – производные аминокислот в основном представлены производными аминокислоты тирозина. Это низкомолекулярные соединения адреналин и норадреналин, синтезирующиеся в мозговом веществе надпочечников, и гормоны щитовидной железы (тироксин и его производные). Гормоны 1-й и 2-й групп хорошо растворимы в воде. Гормоны стероидной природы представлены жирорастворимыми гормонами коркового вещества надпочечников (кортикостероиды), половыми гормонами (эстрогены и андрогены), а также гормональной формой витамина D. Эйкозаноиды, являющиеся производными полиненасыщенной жирной кислоты (арахидоновой), представлены тремя подклассами соединений: простагландины, тромбоксаны и лейкотриены. Эти нерастворимые в воде и нестабильные соединения оказывают свое действие на клетки, находящиеся вблизи их места синтеза.
ГОРМОНЫ ГИПОТАЛАМУСА
Гипоталамус служит местом непосредственного взаимодействия высших отделов ЦНС и эндокринной системы. Природа связей, существующих между ЦНС и эндокринной системой, стала проясняться в последние десятилетия, когда из гипоталамуса были выделены первые гуморальные факторы, оказавшиеся гормональными веществами с чрезвычайно высокой биологической активностью.
http://www. /watch? v=hLeBNyB1qKU&feature=related
Потребовалось немало труда и экспериментального мастерства, чтобы доказать, что эти вещества образуются в нервных клетках гипоталамуса, откуда по системе портальных капилляров достигают гипофиза и регулируют секрецию гипофизарных гормонов, точнее их освобождение (возможно, и биосинтез). Эти вещества получили сначала наименование нейрогормонов, а затем рилизинг-факторов (от англ. release – освобождать), или либеринов. Вещества с противоположным действием, т. е. угнетающие освобождение (и, возможно, биосинтез) гипофизар-ных гормонов, стали называть ингибирующими факторами, или статинами. Таким образом, гормонам гипоталамуса принадлежит ключевая роль в физиологической системе гормональной регуляции многосторонних биологических функций отдельных органов, тканей и целостного организма.
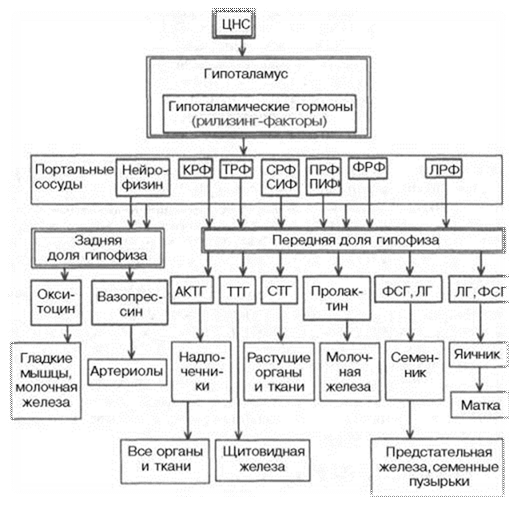
К настоящему времени в гипоталамусе открыто 7 стимуляторов (либерины) и 3 ингибитора (статины) секреции гормонов гипофиза, а именно: кортиколиберин, тиролиберин, люлиберин, фоллилиберин, соматолиберин, пролактолиберин, меланолиберин, соматостатин, пролактостатин и меланостатин (табл. 8.1). В чистом виде выделено 5 гормонов, для которых установлена первичная структура, подтвержденная химическим синтезом.
Большие трудности при получении гормонов гипоталамуса в чистом виде объясняются чрезвычайно низким содержанием их в исходной ткани. Так, для выделения всего 1 мг тиролиберина потребовалось переработать 7 т гипоталамусов, полученных от 5 млн овец.
Следует отметить, что не все гормоны гипоталамуса, по-видимому, строго специфичны в отношении одного какого-либо гипофизарного гормона. В частности, для тиролиберина показана способность освобождать, помимо тиротропина, также пролактин, а для люлиберина, помимо лютеи-низирующего гормона,– также фолликулостимулирующий гормон.
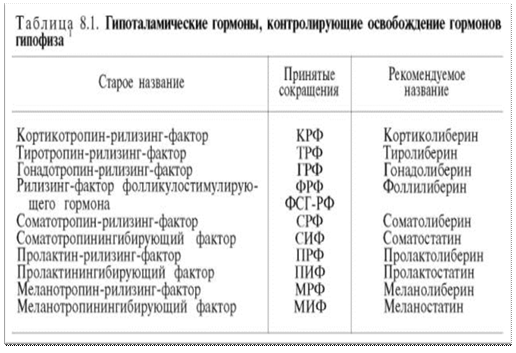
Гипоталамические гормоны не имеют твердо установленных наименований. Рекомендуется в первой части названия гормона гипофиза добавлять окончание «либерин»; например, «тиролиберин» означает гормон гипоталамуса, стимулирующий освобождение (и, возможно, синтез) тиротропина - соответствующего гормона гипофиза. Аналогичным образом образуют названия факторов гипоталамуса, ингибирующих освобождение (и, возможно, синтез) троп-ных гормонов гипофиза,- добавляют окончание «статин». Например, «соматостатин» означает гипоталамический пептид, ингибирующий освобождение (или синтез) гормона роста гипофиза - соматотропина.
http://www. /watch? v=-UaSfYKsFh0
Установлено, что по химическому строению все гормоны гипоталамуса являются низкомолекулярными пептидами, так называемыми олигопептидами необычного строения, хотя точный аминокислотный состав и первичная структура выяснены не для всех. Приводим полученные к настоящему времени данные о химической природе шести из известных 10 гормонов гипоталамуса.
1. Тиролиберин (Пиро-Глу–Гис–Про–NH2):

Тиролиберин представлен трипептидом, состоящим из пироглутаминовой (циклической) кислоты, гистидина и пролинамида, соединенных пептидными связями. В отличие от классических пептидов он не содержит свободных NH2- и СООН-групп у N - и С-концевых аминокислот.
2. Гонадолиберин является декапептидом, состоящим из 10 аминокислот в последовательности:
Пиро-Глу–Гис–Трп–Сер–Тир–Гли–Лей–Арг–Про–Гли-NН2
Концевая С-аминокислота представлена глицинамидом.
3. Соматостатин является циклическим тетрадекапептидом (состоит из 14 аминокислотных остатков):

Отличается этот гормон от двух предыдущих, помимо циклической структуры, тем, что не содержит на N-конце пироглутаминовой кислоты: дисульфидная связь образуется между двумя остатками цистеина в 3-м и 14-м положениях. Следует отметить, что синтетический линейный аналог соматостатина также наделен аналогичной биологической активностью, что свидетельствует о несущественности дисульфидного мостика природного гормона. Помимо гипоталамуса, соматостатин продуцируется нейронами центральной и периферической нервных систем, а также синтезируется в S-клетках панкреатических островков (островков Лангерганса) в поджелудочной железе и клетках кишечника. Он оказывает широкий спектр биологического действия; в частности, показано ингибирующее действие на синтез гормона роста в аденогипофизе, а также прямое тормозящее действие его на биосинтез инсулина и глюкагона в β- и α-клетках островков Лангерганса.
4. Соматолиберин недавно выделен из природных источников. Он представлен 44 аминокислотными остатками с полностью раскрытой последовательностью. Биологической активностью соматолиберина наделен, кроме того, химически синтезированный декапептид:
Н-Вал–Гис–Лей–Сер–Ала–Глу–Глн–Лиз–Глу–Ала-ОН.
Этот декапептид стимулирует синтез и секрецию гормона роста гипофиза соматотропина.
5. Меланолиберин, химическая структура которого аналогична структуре открытого кольца гормона окситоцина (без трипептидной боковой цепи), имеет следующее строение:
Н-Цис–Тир–Иле–Глн–Асн–Цис-ОН.
6. Меланостатин (меланотропинингибирующий фактор) представлен или трипептидом: Пиро-Глу–Лей–Гли-NН2, или пентапептидом со следующей последовательностью:
Пиро-Глу–Гис–Фен–Aрг–Гли–NН2.
Необходимо отметить, что меланолиберин оказывает стимулирующее действие, а меланостатин, напротив, ингибирующее действие на синтез и секрецию меланотропина в передней доле гипофиза. Помимо перечисленных гипоталамических гормонов, интенсивно изучалась химическая природа другого гормона – кортиколиберина . Активные препараты его были выделены как из ткани гипоталамуса, так и из задней доли гипофиза; существует мнение, что последняя может служить депо гормона для вазопрессина и окситоцина. Недавно выделен состоящий из 41 аминокислоты с выясненной последовательностью кортиколиберин из гипоталамуса овцы.
Местом синтеза гипоталамических гормонов, вероятнее всего, являются нервные окончания – синаптосомы гипоталамуса, поскольку именно там отмечена наибольшая концентрация гормонов и биогенных аминов. Последние рассматриваются наряду с гормонами периферических желез внутренней секреции, действующих по принципу обратной связи, в качестве основных регуляторов секреции и синтеза гормонов гипоталамуса. Механизм биосинтеза тиролиберина, осуществляющегося, скорее всего, нерибособальным путем, включает участие SH-содержащей синтетазы или комплекса ферментов, катализирующих циклизацию глутаминовой кислоты в пироглутаминовую, образование пептидной связи и амидирование проли-на в присутствии глутамина. Существование подобного механизма биосинтеза с участием соответствующих синтетаз допускается также в отношении гонадолиберина и соматолиберина.
Пути инактивации гормонов гипоталамуса изучены недостаточно. Период полураспада тиролиберина в крови крысы составляет 4 мин. Инактивация наступает как при разрыве пептидной связи (под действием экзо-и эндопептидаз сыворотки крови крысы и человека), так и при отщеплении амидной группы в молекуле пролинамида. В гипоталамусе человека и ряда животных открыт специфический фермент пироглутамилпептидаза, которая катализирует отщепление от тиролиберина или гонадолиберина молекулы пироглутаминовой кислоты.
Гипоталамические гормоны непосредственно влияют на секрецию (точнее, освобождение) «готовых» гормонов и биосинтез этих гормонов de novo. Доказано, что цАМФ участвует в передаче гормонального сигнала. Показано существование в плазматических мембранах клеток гипофиза специфических аденогипофизарных рецепторов, с которыми связываются гормоны гипоталамуса, после чего через систему аденилатциклазы и мембранных комплексов Са2+–АТФ и Mg2+–АТФ освобождаются ионы Са2+ и цАМФ; последний действует как на освобождение, так и на синтез соответствующего гормона гипофиза путем активирования протеинкиназы. Для выяснения механизма действия рилизинг-факторов, включая их взаимодействие с соответствующими рецепторами, большую роль сыграли структурные аналоги тиролиберина и гонадолиберина. Некоторые из этих аналогов обладают даже более высокой гормональной активностью и пролонгированным действием, чем природные гормоны гипоталамуса. Однако предстоит еще большая работа по выяснению химического строения уже открытых рилизинг-факторов и расшифровке молекулярных механизмов их действия.
ГОРМОНЫ ГИПОФИЗА
В гипофизе синтезируется ряд биологически активных гормонов белковой и пептидной природы, оказывающих стимулирующий эффект на различные физиологические и биохимические процессы в тканях-мишенях (табл. 8.2). В зависимости от места синтеза различают гормоны передней, задней и промежуточной долей гипофиза. В передней доле вырабатываются в основном белковые и полипептидные гормоны, называемые тропными гормонами, или тропинами, вследствие их стимулирующего действия на ряд других эндокринных желез. В частности, гормон, стимулирующий секрецию гормонов щитовидной железы, получил название «тиротропин».
В последние годы из ткани мозга животных было выделено более 50 пептидов, получивших название нейропептидов и определяющих поведенческие реакции. Показано, что эти вещества влияют на некоторые формы поведения, процессы обучения и запоминания, регулируют сон и снимают, подобно морфину, боль. Так, выделенный β-эндорфин (31 аминокислотный остаток с выясненной последовательностью) оказался почти в 30 раз активнее морфина в качестве обезболивающего средства. Ряд других пептидов оказывает снотворное действие, а 16-членный пептид, вызывающий у крыс страх темноты, был назван скотофобином. Выделен полипептид амелетин, который, наоборот, отучает крыс бояться резкого звука электрического звонка. Работы в этом направлении интенсивно ведутся во многих лабораториях. Вполне возможно, что скоро будут выделены и соответственно синтезированы искусственно для каждой формы поведения соответствующие нейропептиды, включая пептиды памяти.
Далее приводятся данные о структуре и функциях важнейших гормонов гипофиза и других желез внутренней секреции, имеющих белковую и пептидную природу.
Вазопрессин и окситоцин
Гормоны вазопрессин и окситоцин синтезируются рибосомальным путем, причем одновременно в гипоталамусе синтезируются 3 белка: нейрофизин I, II и III, функция которых заключается в нековалентном связывании окситоцина и вазопрессина и транспорте этих гормонов в нейросекреторные гранулы гипоталамуса. Далее в виде комплексов нейрофизин–гор-мон они мигрируют вдоль аксона и достигают задней доли гипофиза, где откладываются про запас; после диссоциации комплекса свободный гормон секретируется в кровь. Нейрофизины также выделены в чистом виде, и выяснена первичная структура двух из них (92 из 97 аминокислотных остатков соответственно); это богатые цистеином белки, содержащие по семь дисульфидных связей.
Химическое строение обоих гормонов было расшифровано классическими работами В. дю Виньо и сотр., впервые выделивших эти гормоны из задней доли гипофиза и осуществивших их химический синтез. Оба гормона представляют собой нонапептиды следующего строения:

Вазопрессин отличается от окситоцина двумя аминокислотами: он содержит в положении 3 от N-конца фенилаланин вместо изолейцина и в положении 8 – аргинин вместо лейцина. Указанная последовательность 9 аминокислот характерна для вазопрессина человека, обезьяны, лошади, крупного рогатого скота, овцы и собаки. В молекуле вазопрессина из гипофиза свиньи вместо аргинина в положении 8 содержится лизин, отсюда название «лизин-вазопрессин». У всех позвоночных, за исключением млекопитающих, идентифицирован, кроме того, вазотоцин. Этот гормон, состоящий из кольца с S—S мостиком окситоцина и боковой цепью вазопрессина, был синтезирован химически В. дю Виньо задолго до выделения природного гормона. Высказано предположение, что эволю-ционно все нейрогипофизарные гормоны произошли от одного общего предшественника, а именно аргинин-вазотоцина, из которого путем одиночных мутаций триплетов генов образовались модифицированные гормоны.

Основной биологический эффект окситоцина у млекопитающих связан со стимуляцией сокращения гладких мышц матки при родах и мышечных волокон вокруг альвеол молочных желез, что вызывает секрецию молока. Вазопрессин стимулирует сокращение гладких мышечных волокон сосудов, оказывая сильное вазопрессорное действие, однако основная роль его в организме сводится к регуляции водного обмена, откуда его второе название антидиуретического гормона. В небольших концентрациях (0,2 нг на 1 кг массы тела) вазопрессин оказывает мощное антидиуретическое действие – стимулирует обратный ток воды через мембраны почечных канальцев. В норме он контролирует осмотическое давление плазмы крови и водный баланс организма человека. При патологии, в частности атрофии задней доли гипофиза, развивается несахарный диабет – заболевание, характеризующееся выделением чрезвычайно больших количеств жидкости с мочой. При этом нарушен обратный процесс всасывания воды в канальцах почек. Относительно механизма действия нейрогипофизарных гормонов известно, что гормональные эффекты, в частности вазопрессина, реализуются через аденилатциклазную систему. Однако конкретный механизм действия вазопрессина на транспорт воды в почках пока остается неясным.
Меланоцитстимулирующие гормоны (МСГ, меланотропины)
Меланотропины синтезируются и секретируются в кровь промежуточной долей гипофиза. Выделены и расшифрованы первичные структуры двух типов гормонов – α- и β-меланоцитстимулирующие гормоны (α-МСГ и β-МСГ). Оказалось, чо у всех обследованных животных α-МСГ состоит из 13 остатков аминокислот, расположенных в одинаковой последовательности:
СН3-СО-NH-Сер–Тир–Сер–Мет–Глу–Гис–Фен–Арг–Трп–Гли–Лиз–Про–Вал-СО-NН2
В α-МСГ N-концевой серин ацетилирован, а С-концевая аминокислота представлена валинамидом. Состав и структура β-МСГ оказались более сложными. У большинства животных молекула β-МСГ состоит из 18 остатков аминокислот; кроме того, имеются видовые различия, касающиеся природы аминокислоты в положениях 2, 6 и 16 полипептидной цепи гормона. β-МСГ, выделенный из промежуточной доли гипофиза человека, оказался 22-членным пептидом, удлиненным на 4 аминокислотных остатка с N-конца:
Н-Ала–Глу–Лиз–Лиз–Асп–Глу–Гли–Про–Тир–Aрг–Мет–Глу–Гис–Фен– –Арг–Трп–Гли–Сер–Про–Про–Лиз–Асп-ОН
Физиологическая роль меланотропинов заключается в стимулировании меланиногенеза у млекопитающих и увеличении количества пигментных клеток (меланоцитов) в кожных покровах земноводных. Возможно также влияние МСГ на окраску меха и секреторную функцию сальных желез у животных.
Адренокортикотропный гормон (АКТГ, кортикотропин)
Еще в 1926 г. было установлено, что гипофиз оказывает стимулирующее влияние на надпочечники, повышая секрецию гормонов коркового вещества. Накопленные к настоящему времени данные свидетельствуют, что этим свойством наделен АКТГ, вырабатываемый базофильными клетками аденогипофиза. АКТГ, помимо основного действия – стимуляции синтеза и секреции гормонов коры надпочечников, обладает жиромобилизующей и меланоцитстимулирующей активностью.
Молекула АКТГ у всех видов животных содержит 39 аминокислотных остатков. Первичная структура АКТГ свиньи и овцы была расшифрована еще в 1954–1955 гг. Приводим уточненное строение АКТГ человека:
Н-Сер–Тир–Сер–Мет–Глу–Гис–Фен–Арг–Трп–Гли–Лиз–Про–Вал–Гли–Лиз–Лиз–Aрг–Aрг–Про–Вал–Лиз–Вал–Тир–Про–Асп–Ала–Гли–Глу–Асп–Глн–Сер–Ала–Глу–Ала–Фен–Про–Лей–Глу–Фен-ОН
Различия в структуре АКТГ овцы, свиньи и быка касаются только природы 31-го и 33-го остатков аминокислот, однако все они наделены почти одинаковой биологической активностью, как и АКТГ гипофиза человека. В молекуле АКТГ, как и других белковых гормонов, хотя и не открыты активные центры наподобие активных центров ферментов, однако предполагается наличие двух активных участков пептидной цепи, один из которых ответствен за связывание с соответствующим рецептором, другой – за гормональный эффект. Данные о механизме действия АКТГ на синтез стероидных гормонов свидетельствуют о существенной роли аденилатциклазной системы. Предполагают, что АКТГ вступает во взаимодействие со специфическими рецепторами на внешней поверхности клеточной мембраны (рецепторы представлены белками в комплексе с другими молекулами, в частности с сиаловой кислотой). Сигнал затем передается на фермент аденилатциклазу, расположенную на внутренней поверхности клеточной мембраны, которая катализирует распад АТФ и образование цАМФ. Последний активирует протеинкиназу, которая в свою очередь с участием АТФ осуществляет фосфорилирование холинэстеразы, превращающей эфиры холестерина в свободный холестерин, который поступает в митохондрии надпочечников, где содержатся все ферменты, катализирующие превращение холестерина в кортикостероиды.
Соматотропный гормон (СТГ, гормон роста, соматотропин)
Гормон роста был открыт в экстрактах передней доли гипофиза еще в 1921 г., однако в химически чистом виде получен только в 1956–1957 гг. СТГ синтезируется в ацидофильных клетках передней доли гипофиза; концентрация его в гипофизе составляет 5–15 мг на 1 г ткани, что в 1000 раз превышает концентрацию других гормонов гипофиза. К настоящему времени полностью выяснена первичная структура белковой молекулы СТГ человека, быка и овцы. СТГ человека состоит из 191 аминокислоты и содержит две дисульфидные связи; N- и С-концевые аминокислоты представлены фенилаланином. СТГ обладает широким спектром биологического действия. Он влияет на все клетки организма, определяя интенсивность обмена углеводов, белков, липидов и минеральных веществ. Он усиливает биосинтез белка, ДНК, РНК и гликогена и в то же время способствует мобилизации жиров из депо и распаду высших жирных кислот и глюкозы в тканях. Помимо активации процессов ассимиляции, сопровождающихся увеличением размеров тела, ростом скелета, СТГ координирует и регулирует скорость протекания обменных процессов. Кроме того, СТГ человека и приматов (но не других животных) обладает измеримой лактогенной активностью. Предполагают, что многие биологические эффекты этого гормона осуществляются через особый белковый фактор, образующийся в печени под влиянием гормона. Этот фактор был назван сульфирующим или тимидиловым, поскольку он стимулирует включение сульфата в хрящи, тимидина – в ДНК, уридина – в РНК и пролина – в коллаген. По своей природе этот фактор оказался пептидом с мол. массой 8000. Учитывая его биологическую роль, ему дали наименование «соматомедин», т. е. медиатор действия СТГ в организме. СТГ регулирует процессы роста и развития всего организма, что подтверждается клиническими наблюдениями. Так, при гипофизарной карликовости (патология, известная в литературе как пангипопитуитаризм; связана с врожденным недоразвитием гипофиза) отмечается пропорциональное недоразвитие всего тела, в том числе скелета, хотя существенных отклонений в развитии психической деятельности не наблюдается. У взрослого человека также развивается ряд нарушений, связанных с гипо - или гиперфункцией гипофиза. Известно заболевание акромегалия (от греч. akros – конечность, megas – большой), характеризующееся непропорционально интенсивным ростом отдельных частей тела, например рук, ног, подбородка, надбровных дуг, носа, языка, и разрастанием внутренних органов.

Болезнь вызвана, по-видимому, опухолевым поражением передней доли гипофиза.

http://www. /watch? v=VX2wgM4kUfM


Лактотропный гормон (пролактин, лютеотропный гормон)
Пролактин считается одним из наиболее «древних» гормонов гипофиза, поскольку его удается обнаружить в гипофизе низших наземных животных, у которых отсутствуют молочные железы, а также получить лактогенный эффект у млекопитающих. Помимо основного действия (стимуляция развития молочных желез и лактации), пролактин имеет важное биологическое значение – стимулирует рост внутренних органов, секрецию желтого тела (отсюда его второе название «лютеотропный гормон»), оказывает ренотропное, эритропоэтическое и гипергликемическое действие и др. Избыток пролактина, образующийся обычно при наличии опухолей из секретирую-щих пролактин клеток, приводит к прекращению менструаций (аменорея) и увеличению молочных желез у женщин и к импотенции – у мужчин. Расшифрована структура пролактина из гипофиза овцы, быка и человека. Это крупный белок, представленный одной полипептидной цепью с тремя дисульфидными связями, состоящий из 199 аминокислотных остатков. Видовые отличия в последовательности аминокислот касаются по существу 2–3 аминокислотных остатков. Раньше оспаривалось мнение о секреции лактотропина в гипофизе человека, поскольку предполагали, что его функцию якобы выполняет соматотропин. В настоящее время получены убедительные доказательства существования пролактина человека, хотя в гипофизе его содержится значительно меньше, чем гормона роста. В крови женщин уровень пролактина резко повышается перед родами: до 0,2 нг/л против 0,01 нг/л в норме.
Тиреотропный гормон (ТТГ, тиротропин)
В отличие от рассмотренных пептидных гормонов гипофиза, представленных в основном одной полипептидной цепью, тиротропин является сложным гликопротеином и содержит, кроме того, по две α- и β-субъединицы, которые в отдельности биологической активностью не обладают: мол. масса его около 30000. Тиротропин контролирует развитие и функцию щитовидной железы и регулирует биосинтез и секрецию в кровь тиреоидных гормонов. Полностью расшифрована первичная структура α- и β-субъединиц тиротропина быка, овцы и человека: α-субъединица, содержащая 96 аминокислотных остатков, имеет одинаковую аминокислотную последовательность во всех изученных ТТГ и во всех лютеинизирующих гормонах гипофиза; β-субъединица тиротропина человека, содержащая 112 аминокислотных остатков, отличается от аналогичного полипептида в ТТГ крупного рогатого скота аминокислотными остатками и отсутствием С-концевого метионина. Поэтому многие авторы специфические биологические и иммунологические свойства гормона объясняют наличием β-субъединицы ТТГ в комплексе с α-субъединицей. Предполагают, что действие тиротропина осуществляется, подобно действию других гормонов белковой природы, посредством связывания со специфическими рецепторами плазматических мембран и активирования аденилатциклазной системы
Гонадотропные гормоны (гонадотррпины)
К гонадотропинам относятся фолликулостимулирующий гормон (ФСГ, фоллитропин) и лютеинизирующий гормон (ЛГ, лютропин), или гормон, стимулирующий интерстициальные клетки . Оба гормона синтезируются в передней доле гипофиза и являются, как и тиротропин, сложными белками – гликопротеинами с мол. массой 25000. Они регулируют стероидо - и гаметогенез в половых железах. Фоллитропин вызывает созревание фолликулов в яичниках у самок и сперматогенез – у самцов. Лютропин у самок стимулирует секрецию эстрогенов и прогестерона, как и разрыв фолликулов с образованием желтого тела, а у самцов – секрецию тестостерона и развитие интерстициальной ткани. Биосинтез гонадотропинов, как было отмечено, регулируется гипоталамическим гормоном гонадолиберином.
Химическая структура молекулы лютропина расшифрована полностью. Лютропин состоит из двух α- и β-субъединиц. Структура α-субъединиц гормона у большинства животных совпадает. Так, у овцы она содержит 96 аминокислотных остатков и 2 углеводных радикала. У человека α-субъединица гормона укорочена на 7 аминокислотных остатков с N-конца и отличается природой 22 аминокислот. Расшифрована также последовательность аминокислот в β-субъединицах лютропина свиньи и человека. α- и β-cубъединицы в отдельности лишены биологической активности (по аналогии с большинством субъединиц ферментов). Только их комплекс, образование которого, вероятнее всего, предопределено первичной структурой их, приводит к формированию биологически активной макромолекулярной структуры за счет гидрофобных взаимодействий.
Липотропные гормоны (ЛТГ, липотропины)
Среди гормонов передней доли гипофиза, структура и функция которых выяснены в последнее десятилетие, следует отметить липотропины, в частности β- и γ-ЛТГ. Наиболее подробно изучена первичная структура β-липо-тропина овцы и свиньи, молекулы которого состоят из 91 аминокислотного остатка и имеют существенные видовые различия в последовательности аминокислот. К биологическим свойствам β-липотропина относятся жиро-мобилизующее действие, кортикотропная, меланоцитстимулирующая и ги-покальциемическая активность и, кроме того, инсулиноподобный эффект, выражающийся в повышении скорости утилизации глюкозы в тканях. Предполагают, что липотропный эффект осуществляется через систему аденилатциклаза–цАМФ–протеинкиназа, завершающей стадией действия которой является фосфорилирование неактивной триацилглицерол-липазы. Этот фермент после активирования расщепляет нейтральные жиры на диацилглицерол и высшую жирную кислоту.
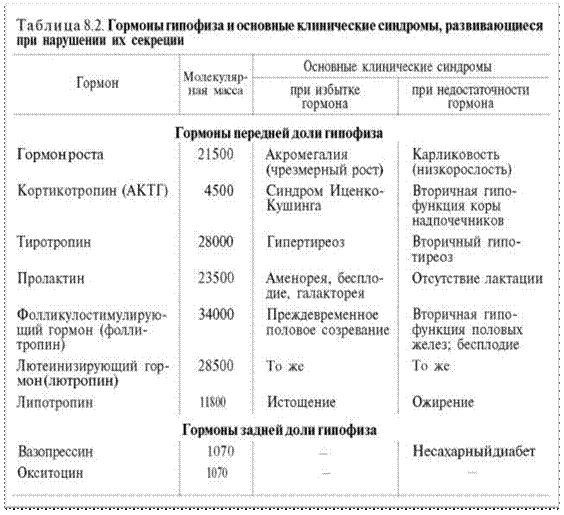
Перечисленные биологические свойства обусловлены не β-липотропином, оказавшимся лишенным гормональной активности, а продуктами его распада, образующимися при ограниченном протеолизе. Оказалось, что в ткани мозга и в промежуточной доле гипофиза синтезируются биологически активные пептиды, наделенные опиатоподобным действием. Приводим структуры некоторых из них:
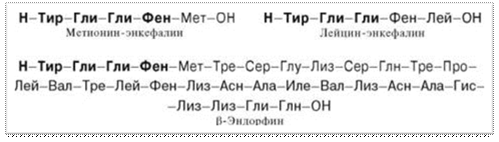
Общим типом структуры для всех трех соединений является тетра-пептидная последовательность на N-конце. Доказано, что β-эндорфин (31 АМК) образуется путем протеолиза из более крупного гипофизарного гормона β-липотропина (91 АМК); последний вместе с АКТГ образуется из общего предшественника – прогормона, названного проопиокортином (является, таким образом, препрогормоном), имеющим молекулярную массу 29 кДа и насчитывающим 134 аминокислотных остатка. Биосинтез и освобождение проопиокортина в передней доле гипофиза регулируется кортиколиберином гипоталамуса. В свою очередь из АКТГ и β-липотропина путем дальнейшего процессинга, в частности ограниченного про-теолиза, образуются соответственно α- и β-меланоцитстимулирующие гормоны (α- и β-МСГ). С помощью техники клонирования ДНК, а также метода определения первичной структуры нуклеиновых кислот Сенджера в ряде лабораторий была раскрыта нуклеотидная последовательность мРНК–предшественника проопиокортина. Эти исследования могут служить основой для целенаправленного получения новых биологически активных гормональных лечебных препаратов.
Ниже представлены пептидные гормоны, образующиеся из β-липотропина путем специфического протеолиза.

Учитывая исключительную роль β-липотропина как предшественника перечисленных гормонов, приводим первичную структуру β-липотропина свиньи (91 аминокислотный остаток):
Н–Глу–Лей–Ала–Гли–Ала–Про–Про–Глу–Про–Ала–Aрг–Асп–Про–Глу–Ала–Про–Ала–Глу–Гли–Ала–Ала–Ала–Aрг–Ала–Глу–Лей–Глу–Тир–Гли–Лей–Вал–Ала–Глу–Ала–Глу–Ала–Ала–Глу–Лиз–Лиз–Асп–Глу–Гли–Про–Тир–Лиз–Мет–Глу–Гис–Фен–Арг–Трп–Гли–Сер–Про–Про–Лиз–Асп–Лиз–Aрг–Тир–Гли–Гли–Фен–Мет–Тре–Сер–Глу–Лиз–Сер– –Глн–Тре–Про–Лей–Вал–Тре–Лей–Фен–Лиз–Асн–Ала–Иле–Вал–Лиз–Асн–Ала–Гис–Лиз–Лиз–Гли–Глн–ОН
Повышенный интерес к указанным пептидам, в частности энкефалинам и эндорфинам, диктуется их необычайной способностью, подобно морфину, снимать болевые ощущения. Эта область исследования – поиск новых природных пептидных гормонов и(или) их направленный биосинтез – является интересной и многообещающей для развития физиологии, нейробиологии, неврологии и клиники.
ГОРМОНЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
Поджелудочная железа относится к железам со смешанной секрецией. Внешнесекреторная функция ее заключается в синтезе ряда ключевых ферментов пищеварения, в частности амилазы, липазы, трипсина, химо-трипсина, карбоксипептидазы и др., поступающих в кишечник с соком поджелудочной железы. Внутрисекреторную функцию выполняют, как было установлено в 1902 г. , панкреатические островки (островки Лангерганса), состоящие из клеток разного типа и вырабатывающие гормоны, как правило, противоположного действия. Так, α- (или А-) клетки продуцируют глюкагон, β- (или В-) клетки синтезируют инсулин, δ-(или D-) клетки вырабатывают соматостатин и F-клетки – малоизученный панкреатический полипептид. Далее будут рассмотрены инсулин и глюка-гон как гормоны, имеющие исключительно важное значение для жизнедеятельности организма .
Инсулин
Инсулин, получивший свое название от наименования панкреатических островков (лат. insula – островок), был первым белком, первичная структура которого была раскрыта в 1954 г. Ф. Сэнджером. В чистом виде инсулин был получен в 1922 г. после его обнаружения в экстрактах панкреатических островков Ф. Бантингом и Ч. Бестом. Молекула инсулина, содержащая 51 аминокислотный остаток, состоит из двух полипептидных цепей, соединенных между собой в двух точках дисульфидными мостиками. Строение инсулина и его предшественника проинсулина приведено в главе 1 (см. рис. 1.14). В настоящее время принято обозначать цепью А инсулина 21-членный пептид и цепью В – пептид, содержащий 30 остатков аминокислот. Во многих лабораториях осуществлен, кроме того, химический синтез инсулина. Наиболее близким по своей структуре к инсулину человека является инсулин свиньи, у которого в цепи В вместо треонина в положении 30 содержится аланин.
Существенных различий в аминокислотной последовательности в инсулине от разных животных нет. Инсулины различаются аминокислотным составом цепи А в положениях 8–10.
Согласно современным представлениям, биосинтез инсулина осуществляется в β-клетках панкреатических островков из своего предшественника проинсулина, впервые выделенного Д. Стайнером в 1966 г. В настоящее время не только выяснена первичная структура проинсулина, но и осуществлен его химический синтез (см. рис. 1.14). Проинсулин представлен одной полипептидной цепью, содержащей 84 аминокислотных остатка; он лишен биологической, т. е. гормональной, активности. Местом синтеза проинсулина считается фракция микросом β-клеток панкреатических островков; превращение неактивного проинсулина в активный инсулин (наиболее существенная часть синтеза) происходит при перемещении проинсулина от рибосом к секреторным гранулам путем частичного протеолиза (отщепление с С-конца полипептидной цепи пептида, содержащего 33 аминокислотных остатка и получившего наименование соединяющего пептида, или С-пептида). Длина и первичная структура С-пептида подвержена большим изменениям у разных видов животных, чем последовательность цепей А и В инсулина. Установлено, что исходным предшественником инсулина является препроинсулин, содержащий, помимо проинсулина, его так называемую лидерную, или сигнальную, последовательность на N-конце, состоящую из 23 остатков аминокислот; при образовании молекулы проинсулина этот сигнальный пептид отщепляется специальной пептидазой. Далее молекула проинсулина также подвергается частичному протеолизу, и под действием трипсиноподобной протеиназы отщепляются по две основные аминокислоты с N - и С-конца пептида С – соответственно дипептиды Aрг–Aрг и Лиз– –Aрг (см. рис. 1.14). Однако природа ферментов и тонкие механизмы этого важного биологического процесса – образование активной молекулы инсулина окончательно не выяснены.
Синтезированный из проинсулина инсулин может существовать в нескольких формах, различающихся по биологическим, иммунологическим и физико-химическим свойствам. Различают две формы инсулина: 1) свободную, вступающую во взаимодействие с антителами, полученными к кристаллическому инсулину, и стимулирующую усвоение глюкозы мышечной и жировой тканями; 2) связанную, не реагирующую с антителами и активную только в отношении жировой ткани. В настоящее время доказано существование связанной формы инсулина и установлена локализация ее в белковых фракциях сыворотки крови, в частности в области трансферринов и α-глобулинов. Молекулярная масса связанного инсулина от 60000 до 100000. Различают, кроме того, так называемую форму А инсулина, отличающуюся от двух предыдущих рядом физико-химических и биологических свойств, занимающую промежуточное положение и появляющуюся в ответ на быструю, срочную потребность организма в инсулине.
В физиологической регуляции синтеза инсулина доминирующую роль играет концентрация глюкозы в крови. Так, повышение содержания глюкозы в крови вызывает увеличение секреции инсулина в панкреатических островках, а снижение ее содержания, наоборот,– замедление секреции инсулина. Этот феномен контроля по типу обратной связи рассматривается как один из важнейших механизмов регуляции содержания глюкозы в крови. На секрецию инсулина оказывают влияние, кроме того, электролиты (особенно ионы кальция), аминокислоты, глюкагон и секретин. Приводятся доказательства роли циклазной системы в секреции инсулина. Предполагают, что глюкоза действует в качестве сигнала для активирования аденилат-циклазы, а образовавшийся в этой системе цАМФ – в качестве сигнала для секреции инсулина.
При недостаточной секреции (точнее, недостаточном синтезе) инсулина развивается специфическое заболевание – сахарный диабет.
http://www. /watch? v=V1LjRi8Nvv4
http://www. /watch? v=ZsTSoLhl3Y4&feature=related
http://www. /watch? v=nBJN7DH83HA&feature=related

Помимо клинически выявляемых симптомов (полиурия, полидипсия и полифагия), сахарный диабет характеризуется рядом специфических нарушений процессов обмена. Так, у больных развиваются гипергликемия (увеличение уровня глюкозы в крови) и гликозурия (выделение глюкозы с мочой, в которой в норме она отсутствует). К расстройствам обмена относят также усиленный распад гликогена в печени и мышцах, замедление биосинтеза белков и жиров, снижение скорости окисления глюкозы в тканях, развитие отрицательного азотистого баланса, увеличение содержания холестерина и других липидов в крови. При диабете усиливаются мобилизация жиров из депо, синтез углеводов из аминокислот (глюконеогенез) и избыточный синтез кетоновых тел (кетонурия). После введения больным инсулина все перечисленные нарушения, как правило, исчезают, однако действие гормона ограничено во времени, поэтому необходимо вводить его постоянно. Клинические симптомы и метаболические нарушения при сахарном диабете могут быть объяснены не только отсутствием синтеза инсулина. Получены доказательства, что при второй форме сахарного диабета, так называемой инсулинрезистентной, имеют место и молекулярные дефекты: в частности, нарушение структуры инсулина или нарушение ферментативного превращения проинсулина в инсулин. В основе развития этой формы диабета часто лежит потеря рецепторами клеток-мишеней способности соединяться с молекулой инсулина, синтез которого нарушен, или синтез мутантного рецептора.
У экспериментальных животных введение инсулина вызывает гипогликемию (снижение уровня глюкозы в крови), увеличение запасов гликогена в мышцах, усиление анаболических процессов, повышение скорости утилизации глюкозы в тканях. Кроме того, инсулин оказывает опосредованное влияние на водный и минеральный обмен.
Механизм действия инсулина окончательно не расшифрован, несмотря на огромное количество фактических данных, свидетельствующих о существовании тесной и прямой зависимости между инсулином и процессами обмена веществ в организме. В соответствии с «унитарной» теорией все эффекты инсулина вызваны его влиянием на обмен глюкозы через фермент гексокиназу. Новые экспериментальные данные свидетельствуют, что усиление и стимуляция инсулином таких процессов, как транспорт ионов и аминокислот, трансляция и синтез белка, экспрессия генов и др., являются независимыми. Это послужило основанием для предположения о множественных механизмах действия инсулина.

Рис. Инсулиновый рецептор (схема). Две α-цепи на наружной поверхности мембраны клетки и две трансмембранные β-цепи. Связывание инсулина с α-цепями запускает аутофосфорилирование остатков тирозина в β-цепях; активный тирозинкиназный домен затем участвует в фосфорилировании неактивных белков-мишеней в цитозоле.
http://www. /watch? v=VLiTbb6MaEU&NR=1
Наиболее вероятной в настоящее время представляется мембранная локализация первичного действия почти всех белковых гормонов, включая инсулин. Получены доказательства существования специфического рецептора инсулина на внешней плазматической мембране почти всех клеток организма, а также образования инсулинрецепторного комплекса. Рецептор синтезируется в виде предшественника – полипептида (1382 аминокислотных остатка, мол. масса 190000), который далее расщепляется на α-и β-субъединицы, т. е. на гетеродимер (в формуле α2–β2), связанные дисульфидными связями. Оказалось, что если α-субъединицы (мол. масса 135000) почти целиком располагаются на внешней стороне биомембраны, выполняя функцию связывания инсулина клетки, то β-субъединицы (мол. масса 95000) представляют собой трансмембранный белок, выполняющий функцию преобразования сигнала. Концентрация рецепторов инсулина на поверхности достигает 20000 на клетку, и период их полужизни составляет 7–12 ч.
Самым интересным свойством рецептора инсулина, отличным от всех других рецепторов гормонов белковой и пептидной природы, является его способность аутофосфорилирования, т. е. когда рецептор наделен сам протеинкиназной (тирозинкиназной) активностью. При связывании инсулина с α-цепями рецептора происходит активирование тирозинкиназной активности β-цепей путем фосфорилирования их тирозиновых остатков. В свою очередь активная тирозинкиназа β-цепей запускает каскад фосфо-рилирования–дефосфорилирования протеинкиназ, в частности мембранных или цитозольных серин - или треонинкиназ, т. е. протеинкиназ и белков-мишеней, фосфорилирование в которых осуществляется за счет ОН-групп серина и треонина. Соответственно имеют место изменения клеточной активности, в частности активация и ингибирование ферментов, транспорт глюкозы, синтез полимерных молекул нуклеиновых кислот и белков и т. д. Следует подчеркнуть, однако, что тонкие молекулярные механизмы путей передачи сигнала от инсулинрецепторного комплекса на множество внутриклеточных процессов пока не раскрыты. Вполне возможно участие в подобных процессах ряда внутриклеточных вторичных мессенджеров, в частности циклических нуклеотидов, производных фосфатидилинозитолов и др. Нельзя исключить, кроме того, возможности существования внутриклеточного посредника или медиатора действия инсулина (особого внутриклеточного рецептора), контролирующего транскрипцию генов и соответственно синтез мРНК. Предполагают, что действием инсулина и участием в регуляции экспрессии генов или в транскрипции специфических мРНК может быть объяснена его роль в таких фундаментальных процессах жизнедеятельности, как эмбриогенез и дифференцировка клеток высших организмов.
http://www. /watch? v=6fmYLF-uiNI
Глюкагон
Глюкагон впервые был обнаружен в коммерческих препаратах инсулина еще в 1923 г., однако только в 1953 г. венгерский биохимик Ф. Штрауб получил этот гормон в гомогенном состоянии. Глюкагон синтезируется в основном в α-клетках панкреатических островков поджелудочной железы, а также в ряде клеток кишечника.
http://www. /watch? v=FEsTIOIufiQ
Он представлен одной линейно расположенной полипептидной цепью, в состав которой входит 29 аминокислотных остатков в следующей последовательности:
Н–Гис–Сер–Глн–Гли–Тре–Фен–Тре–Сер–Асп–Тир–Сер–Лиз–Тир–Лей–Асп–Сер–Aрг–Aрг–Ала–Глн–Асп–Фен–Вал–Глн–Трп–Лей–Мет–Асн––Тре–ОН
Первичная структура глюкагонов человека и животных оказалась идентичной; исключение составляет только глюкагон индюка, у которого вместо аспарагина в положении 28 содержится серин. Особенностью структуры глюкагона является отсутствие дисульфидных связей и цистеина. Глюкагон образуется из своего предшественника проглюкагона, содержащего на С-конце полипептида дополнительный октапептид (8 остатков), отщепляемый в процессе постсинтетического протеолиза. Имеются данные, что у проглюкагона, так же как и у проинсулина, существует предшественник – препроглюкагон (мол. масса 9000), структура которого пока не расшифрована.
По биологическому действию глюкагон, как и адреналин, относятся к гипергликемическим факторам, вызывает увеличение концентрации глюкозы в крови главным образом за счет распада гликогена в печени. Органами-мишенями для глюкагона являются печень, миокард, жировая ткань, но не скелетные мышцы. Биосинтез и секреция глюкагона контролируются главным образом концентрацией глюкозы по принципу обратной связи. Таким же свойством обладают аминокислоты и свободные жирные кислоты. На секрецию глюкагона оказывают влияние также инсулин и инсулиноподобные факторы роста.
В механизме действия глюкагона первичным является связывание со специфическими рецепторами мембраны клеток, образовавшийся глю-кагонрецепторный комплекс активирует аденилатциклазу и соответственно образование цАМФ. Последний, являясь универсальным эффектором внутриклеточных ферментов, активирует протеинкиназу, которая в свою очередь фосфорилирует киназу фосфорилазы и гликогенсинтазу. Фосфорили-рование первого фермента способствует формированию активной гликоген-фосфорилазы и соответственно распаду гликогена с образованием глюкозо--1-фосфата, в то время как фосфорилирование гликогенсинта-зы сопровождается переходом ее в неактивную форму и соответственно блокированием синтеза гликогена. Общим итогом действия глюкагона являются ускорение распада гликогена и торможение его синтеза в печени, что приводит к увеличению концентрации глюкозы в крови. Гипергликемический эффект глюкагона обусловлен, однако, не только распадом гликогена. Имеются бесспорные доказательства существования глюконеогенетического механизма гипергликемии, вызванной глюкагоном. Установлено, что глюкагон способствует образованию глюкозы из промежуточных продуктов обмена белков и жиров. Глюкагон стимулирует образование глюкозы из аминокислот путем индукции синтеза ферментов глюконеогенеза при участии цАМФ, в частности фосфоенолпируваткарбок-сикиназы – ключевого фермента этого процесса. Глюкагон в отличие от адреналина тормозит гликолитический распад глюкозы до молочной кислоты, способствуя тем самым гипергликемии. Он активирует опосредованно через цАМФ липазу тканей, оказывая мощный липолитический эффект. Существуют и различия в физиологическом действии: в отличие от адреналина глюкагон не повышает кровяного давления и не увеличивает частоту сердечных сокращений. Следует отметить, что, помимо панкреатического глюкагона, в последнее время доказано существование кишечного глюкагона, синтезирующегося по всему пищеварительному тракту и поступающего в кровь. Первичная структура кишечного глюкагона пока точно не расшифрована, однако в его молекуле открыты идентичные N-концевому и среднему участкам панкреатического глюкагона аминокислотные последовательности, но разная С-концевая последовательность аминокислот.
Таким образом, панкреатические островки, синтезирующие два противоположного действия гормона – инсулин и глюкагон, выполняют ключевую роль в регуляции обмена веществ на молекулярном уровне.
Гормоны мозгового вещества надпочечников

О способности экстрактов из надпочечников повышать кровяное давление было известно еще в XIX в., однако только в 1901 г. Дж. Такамине и сотр. выделили из мозгового слоя надпочечников активное начало, идентифицированное с адреналином.
http://www. /watch? v=4g25d7_Afmc
Это был первый гормон, полученный в чистом кристаллическом виде. Спустя более 40 лет, в 1946 г., из мозгового вещества был выделен еще один гормон – норадреналин, который до этого был синтезирован химическим путем. Помимо этих двух главных гормонов, в надпочечниках в следовых количествах синтезируется еще один гормон – изопропиладреналин. Все указанные гормоны имеют сходное строение.

Эти гормоны по строению напоминают аминокислоту тирозин, от которого они отличаются наличием дополнительных ОН-групп в кольце и у β-углеродного атома боковой цепи и отсутствием карбоксильной группы. Действительно, получены экспериментальные доказательства, что предшественником гормонов мозгового вещества надпочечников является тирозин, подвергающийся в процессе обмена реакциям гидроксилирования, декарбоксилирования и метилирования с участием соответствующих ферментов.
http://www. /watch? v=06jbq3bxKE0&feature=related
Биосинтез катехоламинов (адреналин и норадреналин) может быть представлен в виде следующей упрощенной схемы:

В мозговом веществе надпочечников человека массой 10 г содержится около 5 мг адреналина и 0,5 мг норадреналина. Содержание их в крови составляет соответственно 1,9 и 5,2 нмоль/л. В плазме крови оба гормона присутствуют как в свободном, так и в связанном, в частности, с альбуминами состоянии. Небольшие количества обоих гормонов откладываются в виде соли с АТФ в нервных окончаниях, освобождаясь в ответ на их раздражение. Адреналин и норадреналин, как и дофамин, относятся к катехоламинам, т. е. к классу органических веществ, оказывающих сильное биологическое действие. Кроме того, все они оказывают мощное сосудосуживающее действие, вызывая повышение артериального давления, и в этом отношении действие их сходно с действием симпатической нервной системы. Известно мощное регулирующее влияние этих гормонов на обмен углеводов в организме. Так, в частности, адреналин вызывает резкое повышение уровня глюкозы в крови, что обусловлено ускорением распада гликогена в печени под действием фермента фосфорилазы. Адреналин, как и глюкагон, активирует фосфорилазу не прямо, а через систему аденилатциклаза-цАМФ-протеинкиназа. Гипергликемическйй эффект норадреналина значительно ниже – примерно 5% от действия адреналина. Параллельно отмечаются накопление гексозофосфатов в тканях, в частности в мышцах, уменьшение концентрации неорганического фосфата и повышение уровня ненасыщенных жирных кислот в плазме крови. Имеются данные о торможении окисления глюкозы в тканях под влиянием адреналина. Это действие некоторые авторы связывают с уменьшением скорости проникновения (транспорта) глюкозы внутрь клетки. Механизм действия катехоламинов, включающий α- и β-адренергические рецепторы, аденилатциклазную систему и другие факторы, рассмотрен в конце данной главы.
Известно, что и адреналин, и норадреналин быстро разрушаются в организме; с мочой выделяются неактивные продукты их обмена, главным образом в виде 3-метокси-4-оксиминдальной кислоты, оксоадренохрома, метоксинорадреналина и метоксиадреналина. Эти метаболиты содержатся в моче преимущественно в связанной с глюкуроновой кислотой форме. Ферменты, катализирующие указанные превращения катехоламинов, выделены из многих тканей и достаточно хорошо изучены, в частности моноаминоксидаза (МАО), определяющая скорость биосинтеза и распада кате-холаминов, и катехолметилтрансфераза, катализирующая главный путь превращения адреналина, т. е. о-метилирование за счет S-аденозилметиони-на. Приводим структуру двух конечных продуктов распада катехоламинов:

МОЛЕКУЛЯРНЫЕ МЕХАНИЗМЫ ПЕРЕДАЧИ ГОРМОНАЛЬНОГО СИГНАЛА
Несмотря на огромное разнообразие гормонов и гормоноподобных веществ, в основе биологического действия большинства гормонов лежат удивительно сходные, почти одинаковые фундаментальные механизмы, передающие информацию от одних клеток к другим. Далее будут представлены примеры механизмов действия гормонов пептидной (включая производные аминокислот) и стероидной природы. В современных представлениях о тонких молекулярных механизмах биологического действия большинства гормонов огромную роль сыграли исследования Э. Сазерленда и открытие циклического аденозинмонофосфата.
Известно, что направленность и тонкая регуляция процесса передачи информации обеспечиваются прежде всего наличием на поверхности клеток рецепторных молекул (чаще всего белков), узнающих гормональный сигнал. Этот сигнал рецепторы трансформируют в изменение концентраций внутриклеточных посредников, получивших название вторичных мессенджеров, уровень которых определяется активностью ферментов, катализирующих их биосинтез и распад.
По своей химической природе рецепторы почти всех биологически активных веществ оказались гликопротеинами, причем «узнающий» домен (участок) рецептора направлен в сторону межклеточного пространства, в то время как участок, ответственный за сопряжение рецептора с эффекторной системой (с ферментом, в частности), находится внутри (в толще) плазматической мембраны. Общим свойством всех рецепторов является их высокая специфичность по отношению к одному определенному гормону (с константой сродства от 0,1 до 10 нМ). Известно также, что сопряжение рецептора с эффекторными системами осуществляется через так называемый G-белок, функция которого заключается в обеспечении многократного проведения гормонального сигнала на уровне плазматической мембраны. G-белок в активированной форме стимулирует через аденилатцик-лазу синтез циклического АМФ, который запускает каскадный механизм активирования внутриклеточных белков.
Общим фундаментальным механизмом, посредством которого реализуются биологические эффекты «вторичных» мессенджеров внутри клетки, является процесс фосфорилирования – дефосфорилирования белков при участии широкого разнообразия протеинкиназ, катализирующих транспорт концевой группы от АТФ на ОН-группы серина и треонина, а в ряде случаев – тирозина белков-мишеней. Процесс фосфорилирования представляет собой важнейшую посттрансляционную химическую модификацию белковых молекул, коренным образом изменяющую как их структуру, так и функции. В частности, он вызывает изменение структурных свойств (ассоциацию или диссоциацию составляющих субъединиц), активирование или ингибирование их каталитических свойств, в конечном итоге определяя скорость химических реакций и в целом функциональную активность клеток.
Аденилатциклазная мессенджерная система
Наиболее изученным является аденилатциклазный путь передачи гормонального сигнала. В нем задействовано мимимум пять хорошо изученных белков: 1) рецептор гормона; 2) фермент аденилатциклаза, выполняющая функцию синтеза циклического АМФ (цАМФ); 3) G-белок, осуществляющий связь между аденилатциклазой и рецептором; 4) цАМФ-зависимая протеинкиназа, катализирующая фосфорилирование внутриклеточных ферментов или белков-мишеней, соответственно изменяя их активность; 5) фосфодиэстераза, которая вызывает распад цАМФ и тем самым прекращает (обрывает) действие сигнала.
Получены в чистом виде α- и β-адренергические рецепторы из плазматических мембран клеток печени, мышц и жировой ткани. Показано, что связывание гормона с β-адренергическим рецептором приводит к структурным изменениям внутриклеточного домена рецептора, что в свою очередь обеспечивает взаимодействие рецептора со вторым белком сигнального пути – ГТФ-связывающим.
ГТФ-связывающий белок – G-белок – представляет собой смесь 2 типов белков: активного Gs(от англ. stimulatory G) и ингибиторного Gi с мол. массой 80000–90000. В составе каждого из них имеется три разные субъединицы (α-, β- и γ-), т. е. это гетеротримеры. Показано, что β-субъеди-ницы Gsи Giидентичны (мол. масса 35000); в то же время α-субъединицы, являющиеся продуктами разных генов (мол. масса 45000 и 41000), оказались ответственными за проявление G-белком активаторной и ингибиторной активности соответственно. Гормонрецепторный комплекс сообщает G-белку способность не только легко обменивать эндогенный связанный ГДФ на ГТФ, но и переводить Gs-белок в активированное состояние, при этом активный G-белок диссоциирует в присутствии ионов Mg2+на β-, γ-субъединицы и комплекс α-субъединицы Gsв ГТФ-форме; этот активный комплекс затем перемещается к молекуле аденилатциклазы и активирует ее. Сам комплекс затем подвергается самоинактивации за счет энергии распада ГТФ и реассоциации β- и γ-субъединиц с образованием первоначальной ГДФ-формы Gs.

Рис. Аденилатциклазный путь передачи гормонального сигнала.
Рец - рецептор; G - G-белок; АЦ-аденилатциклаза.
http://www. /watch? v=oBL0OC3IavI
Аденилатциклаза представляет собой интегральный белок плазматических мембран, его активный центр ориентирован в сторону цитоплазмы и катализирует реакцию синтеза цАМФ из АТФ:

Каталитический компонент аденилатциклазы, выделенный из разных тканей животных, представлен одним полипептидом с мол. массой 120000– 150000; в отсутствие G-белков он практически неактивен; содержит две SH-группы, одна из которых вовлечена в сопряжение с Gs-белком, а вторая необходима для проявления каталитической активности. В молекуле фермента имеется несколько аллостерических центров, через которые осуществляется регуляция активности низкомолекулярными соединениями: ионами Mg2+, Mn2+и Са2+, аденозином и форсколином. Под действием фосфоди-эстеразы цАМФ гидролизуется с образованием неактивного 5'-АМФ.
Протеинкиназа – это внутриклеточный фермент, через который цАМФ реализует свой эффект. Протеинкиназа может существовать в 2 формах. В отсутствие цАМФ Протеинкиназа представлена в виде тетрамерного комплекса, состоящего из двух каталитических (С2) и двух регуляторных (R2) субъединиц с мол. массами 49000 и 38000 соответственно; в этой форме фермент неактивен. В присутствии цАМФ протеинкиназный комплекс обратимо диссоциирует на одну R2-субъединицу и две свободные каталитические субъединицы С; последние обладают ферментативной активностью, катализируя фосфорилирование белков и ферментов, соответственно изменяя клеточную активность.


Рис. Ковалентная регуляция гликогенфосфорилазы.
Следует отметить, что в клетках открыт большой класс цАМФ-зависи-мых протеинкиназ , названных протеинкиназами А; они катализируют перенос фосфатной группы на ОН-группы серина и треонина (так называемые серин-треонин-киназы). Другой класс протеинкиназ, в частности активируемый инсулиновым рецептором (см. ранее), действует только на ОН-группу тирозина. Однако во всех случаях добавление высокозарядной и объемной фосфатной группы вызывает не только конформационные изменения фосфорилированных белков, но изменяет их активность или кинетические свойства. Активность многих ферментов регулируется цАМФ-зависимым фосфо-рилированием, соответственно большинство гормонов белково-пептидной природы активирует этот процесс. Однако ряд гормонов оказывает тормозящий эффект на аденилатциклазу, соответственно снижая уровень цАМФ и фосфорилирование белков. В частности, гормон соматостатин, соединяясь со своим специфическим рецептором – ингибиторным G-белком (Gi, являющимся структурным гомологом Gs-белка (см. ранее), ингиби-рует аденилатциклазу и синтез цАМФ, т. е. вызывает эффект, прямо противоположный вызываемому адреналином и глюкагоном. В ряде органов простагландины (в частности, РGЕ1) также оказывают ингибиторный эффект на аденилатциклазу, хотя в том же органе (в зависимости от типа клеток) и тот же PGE1может активировать синтез цАМФ. Более подробно изучен механизм активирования и регуляции мышечной гликогенфосфорилазы, активирующей распад гликогена. Выделяют 2 формы: каталитически активную – фосфорилазаа и неактивную – фосфо-рилаза b. Обе фосфорилазы построены из двух идентичных субъединиц (мол. массой 94500), в каждой остаток серина в положении 14 подвергается процессу фосфорилирования–дефосфорилирования, соответственно активированию и инактивированию (рис. 8.6).
Под действием киназы фосфорилазы b, активность которой регулируется цАМФ-зависимой протеинкиназой, обе субъединицы молекулы неактивной формы фосфорилазы b подвергаются ковалентному фосфорилиро-ванию и превращаются в активную фосфорилазу а. Дефосфорилирование последней под действием специфической фосфатазы фосфорилазы а приводит к инактивации фермента и возврату в исходное состояние.
В мышечной ткани открыты 3 типа регуляции гликогенфосфорилазы. Первый тип – ковалентная регуляция, основанная на гормонзависимом фосфорилировании–дефосфорилировании субъединиц фосфорилазы.

Рис. Аллостерическая регуляция гликогенфосфорилазы.
Второй тип – аллостерическая регуляция. Она основана на реакциях аденилирования–деаденилирования субъединиц гликогенфосфорилазы b (соответственно активирование–инактивирование). Направление реакций определяется отношением концентраций АМФ и АТФ, присоединяющихся не к активному центру, а к аллостерическому центру каждой субъединицы.
В работающей мышце накопление АМФ, обусловленное тратой АТФ, вызывает аденилирование и активирование фосфорилазы b. В покое, наоборот, высокие концентрации АТФ, вытесняя АМФ, приводят к аллостериче-скому ингибированию этого фермента путем деаденилирования. цАМФ и протеинкиназа играют центральную роль в гормональной регуляции синтеза и распада гликогена в печени (рис. 8.8). Подробно о химических превращениях гликогена. Третий тип – кальциевая регуляция, основанная на аллостерическом активировании киназы фосфорилазы b ионами Са2+, концентрация которых повышается при мышечном сокращении, способствуя тем самым образованию активной фосфорилазы а.
Гуанилатциклазная мессенджерная система
Довольно долгое время циклический гуанозинмонофосфат (цГМФ) рассматривался как антипод цАМФ. Ему приписывали функции, противоположные цАМФ. К настоящему времени получено много данных, что цГМФ принадлежит самостоятельная роль в регуляции функции клеток. В частности, в почках и кишечнике он контролирует ионный транспорт и обмен воды, в сердечной мышце служит сигналом релаксации и т. д. Биосинтез цГМФ из ГТФ осуществляется под действием специфической гуанилатциклазы по аналогии с синтезом цАМФ:


Рис. Схематическое выражение центральной роли цАМФ и протеинкиназы в гормональной регуляции синтеза и распада гликогена.
Адреналинрецепторный комплекс: АЦ - аденилатциклаза, G - G-белок; С и R - соответственно каталитические и регуляторные субъединицы протеинкиназы; КФ - киназа фосфорилазы b Ф - фосфорилаза; Глк-1-P - глюкозо-1-фосфат; Глк-6-P - глюкозо-6-фосфат; УДФ-Глк - ури-диндифосфатглюкоза; ГС - гликогенсинтаза.
Известны четыре разные формы гуанилатциклазы, три из которых являются мембраносвязанными и одна – растворимая открыта в цитозоле. Показано, что мембраносвязанные формы (мол. массой ~ 180000) состоят из 3 участков: рецепторного, локализованного на внешней поверхности плазматической мембраны; внутримембранного домена и каталитического компонента, одинакового у разных форм фермента. Гуанилатциклаза открыта во многих органах (сердце, легкие, почки, надпочечники, эндотелий кишечника, сетчатка и др.), что свидетельствует о широком ее участии в регуляции внутриклеточного метаболизма, опосредованном через цГМФ. Мембраносвязанный фермент активируется через соответствующие рецепторы короткими внеклеточными пептидами (18–20 аминокислотных остатков), в частности гормоном предсердным натрийуретическим пептидом (АНФ), термостабильным токсином грамотрицательных бактерий и др. АНФ, как известно, синтезируется в предсердии в ответ на увеличение объема крови, поступает с кровью в почки, активирует гуанилатциклазу (соответственно повышает уровень цГМФ), способствуя экскреции Na и воды. Гладкие мышечные клетки сосудов также содержат аналогичную рецептор-гуанилатциклазную систему, посредством которой связанный с рецептором АНФ оказывает сосудорасширяющее действие, способствуя снижению кровяного давления. В эпителиальных клетках кишечника активатором рецептор–гуанилатциклазной системы может служить бактериальный эндотоксин, который приводит к замедлению всасывания воды в кишечнике и развитию диареи.
Растворимая форма гуанилатциклазы (мол. масса 152000) является гемсодержащим ферментом, состоящим из 2 субъединиц. В регуляции этой формы гуанилатциклазы принимают участие нитровазодилататоры, свободные радикалы – продукты перекисного окисления липидов. Одним из хорошо известных активаторов является эндотелиальный фактор (EDRF), вызывающий релаксацию сосудов. Действующим компонентом, естественным лигандом, этого фактора служит оксид азота NO. Эта форма фермента активируется также некоторыми нитрозовазодилататорами (нитроглицерин, нитропруссид и др.), используемыми при болезнях сердца; при распаде этих препаратов также освобождается NO.
Оксид азота образуется из аминокислоты аргинина при участии сложной Са2+-зависимой ферментной системы со смешанной функцией, названной NO-синтазой:

Оксид азота при взаимодействии с гемом гуанилатциклазы способствует быстрому образованию цГМФ, который снижает силу сердечных сокращений путем стимулирования ионных насосов, функционирующих при низких концентрациях Са2+. Однако действие NO кратковременное, несколько секунд, локализованное – вблизи места его синтеза. Подобный эффект, но более длительный оказывает нитроглицерин, который медленнее освобождает NO.
Получены доказательства, что большинство эффектов цГМФ опосредовано через цГМФ-зависимую протеинкиназу, названную протеинкина-зой G. Этот широко распространенный в эукариотических клетках фермент получен в чистом виде (мол. масса 80000). Он состоит из 2 субъединиц – каталитического домена с последовательностью, аналогичной последовательности С-субъединицы протеинкиназы А (цАМФ-зависимой), и регуляторного домена, сходного с R-субъединицей протеинкиназы А (см. ранее). Однако протеинкиназы А и G узнают разные последовательности белков, регулируя соответственно фосфорилирование ОН-группы серина и треонина разных внутриклеточных белков и оказывая тем самым разные биологические эффекты.
Уровень циклических нуклеотидов цАМФ и цГМФ в клетке контролируется соответствующими фосфодиэстеразами, катализирующими их гидролиз до 5'-нуклеотидмонофосфатов и различающимися по сродству к цАМФ и цГМФ. Выделены и охарактеризованы растворимая кальмодулинзависимая фосфодиэстераза и мембраносвязанная изоформа, не регулируемая Са2+ и кальмодулином.
Са2+-мессенджерная система
Ионам Са2+ принадлежит центральная роль в регуляции многих клеточных функций. Изменение концентрации внутриклеточного свободного Са2+ является сигналом для активации или ингибирования ферментов, которые в свою очередь регулируют метаболизм, сократительную и секреторную активность, адгезию и клеточный рост. Источники Са2+ могут быть внутри - и внеклеточными. В норме концентрация Са2+ в цитозоле не превышает 10–7 М, и основными источниками его являются эндоплазмати-ческий ретикулум и митохондрии. Нейрогормональные сигналы приводят к резкому повышению концентрации Са2+ (до 10–6 М), поступающего как извне через плазматическую мембрану (точнее, через потенциалзависимые и рецепторзависимые кальциевые каналы), так и из внутриклеточных источников. Одним из важнейших механизмов проведения гормонального сигнала в кальций–мессенджерной системе является запуск клеточных реакций (ответов) путем активирования специфической Са2+-кальмодулин-зависимой протеинкиназы. Регуляторной субъединицей этого фермента оказался Са2+-связывающий белок кальмодулин (мол. масса 17000). При повышении концентрации Са2+ в клетке в ответ на поступающие сигналы специфическая протеинкиназа катализирует фосфорилирование множества внутриклеточных ферментов – мишеней, регулируя тем самым их активность. Показано, что в состав киназы фосфорилазы b, активируемой ионами Са2+, как и NO-синтазы, входит кальмодулин в качестве субъединицы. Кальмодулин является частью множества других Са2+-свя-зывающих белков. При повышении концентрации кальция связывание Са2+ с кальмодулином сопровождается конформационными его изменениями, и в этой Са2+-связанной форме кальмодулин модулирует активность множества внутриклеточных белков (отсюда его название).
К внутриклеточной системе мессенджеров относят также производные фосфолипидов мембран эукариотических клеток, в частности фосфорили-рованные производные фосфатидилинозитола. Эти производные освобождаются в ответ на гормональный сигнал (например, от вазопрессина или тиротропина) под действием специфической мембраносвязанной фосфо-липазы С. В результате последовательных реакций образуются два потенциальных вторичных мессенджера – диацилглицерол и инозитол-1,4,5-трифосфат.
Биологические эффекты этих вторичных мессенджеров реализуются по-разному. Действие диацилглицерола, как и свободных ионов Са2+, опосредовано через мембраносвязанный Са-зависимый фермент протеин-киназу С, которая катализирует фосфорилирование внутриклеточных ферментов, изменяя их активность. Инозитол-1,4,5-трифосфат связывается со специфическим рецептором на эндоплазматическом ретикулуме, способствуя выходу из него ионов Са2+ в цитозоль.

Таким образом, представленные данные о вторичных мессенджерах свидетельствуют о том, что каждой из этих систем посредников гормонального эффекта соответствует определенный класс протеинкиназ, хотя нельзя исключить возможности существования тесной связи между этими системами. Активность протеинкиназ типа А регулируется цАМФ, протеинкиназы G – цГМФ; Са2+-кальмодулинзависимые протеинкиназы находятся под контролем внутриклеточной [Са2+], а протеинкиназа типа С регулируется диацилглицеролом в синергизме со свободным Са2+ и кислыми фосфолипидами. Повышение уровня какого-либо вторичного мес-сенджера приводит к активации соответствующего класса протеинкиназ и последующему фосфорилированию их белковых субстратов. В результате меняется не только активность, но и регуляторные и каталитические свойства многих ферментных систем клетки: ионных каналов, внутриклеточных структурных элементов и генетического аппарата.
Известно, что эффект стероидных гормонов реализуется через генетический аппарат путем изменения экспрессии генов. Гормон после доставки с белками крови в клетку проникает (путем диффузии) через плазматическую мембрану и далее через ядерную мембрану и связывается с внутриядерным рецептором–белком. Комплекс стероид–белок затем связывается с регуляторной областью ДНК, с так называемыми гормончувствительны-ми элементами, способствуя транскрипции соответствующих структурных генов, индукции синтеза белка de novo и изменению метаболизма клетки в ответ на гормональный сигнал.
Следует подчеркнуть, что главной и отличительной особенностью молекулярных механизмов действия двух основных классов гормонов является то, что действие пептидных гормонов реализуется в основном путем посттрансляционных (постсинтетических) модификаций белков в клетках, в то время как стероидные гормоны (а также тиреоидные гормоны, ретиноиды, витамин D3-гормоны) выступают в качестве регуляторов экспрессии генов. Это обобщение, однако, не является абсолютным, и здесь возможны модификации, рассмотренные при описании отдельных гормонов.